Схема превращения и способы ее подтверждения
Необходимым условием правильно составленной схемы превращение является: при суммировании всех стадий все промежуточные частицы и комплексы должны сокращаться, давая в итоге стехиометрическое уравнение (базис реакции).
Базис реакции – кинетическое описание процесса, как системы дифференциальных уравнений для скоростей превращения ключевых веществ для совокупности элементарных реакций.
Для построения кинетических уравнений по сложному механизму, часто используют метод маршрутов реакций.
Маршрут реакции – совокупность элементарных стадий с их стехиометрическими числами, необходимыми чтобы при математических операциях с этими стадиями в результате получалось единственное стехиометрическое уравнение реакции.
Пример:
А + B = C + 2E
Элементарные стадии:
A = D + 2K
D + B = C
υK = υE
υK = υE = 1
Если:
2K = 2E
+
D + B = C
A = D + 2K
2K + D + B + A = 2E + C + D + 2K
A + B = 2E + C
Стехиометрическое число:
γE = γK = 2
Для реакций, имеющих сложный механизм, большое значение имеет метод маршрутов развитый Хориути-Тёмкиным.
Метод состоит в том, что число независимых маршрутов, описывающих механизм реакции, называется базисом маршрутов и равняется разности стехиометрически независимых стадий базиса реакции и количества промежуточных комплексов или частиц.
Метод маршрутов позволяет установить стехиометрическое уравнение реакции с точки зрения стехиометрии.
А = В или 2А = 2В
С точки зрения механизма реакции, термодинамических и кинетических расчетов, необходимо учитывать маршрут.
Если:
А = Х последовательно Х = В,
то уравнение реакции:
А = В.
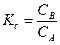 .
.
Если:
А = Х + В;
Х + А = В,
то
2А = 2В;
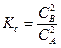 .
.
Во-первых, маршруты реакций могут состоять из линейной последовательности стадий, тогда при построении кинетических уравнений и расчете констант устраняются константы всех промежуточных частиц.
Во-вторых, маршруты реакций могут состоять из замкнутых стадий, например каталитические или цепные. Обычно в таких реакциях концентрация катализатора остается неизвестной и для ее нахождения требуется дополнительные условия: уравнения баланса по различным формам катализатора.
Дата добавления: 2015-08-14; просмотров: 963;
