Теплоемкость газов. Энтропия.
Отношение элементарного количества теплоты 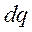 , полученное телом при бесконечно малом изменении его состояния, к изменению температуры
, полученное телом при бесконечно малом изменении его состояния, к изменению температуры 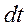 называется удельной теплоемкостью тела в данном процессе:
называется удельной теплоемкостью тела в данном процессе:
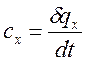 (1.13.1)
(1.13.1)
Величина  в уравнении зависит не только от интервала температур, но и от вита процесса подвода теплоты, характеризуемого некоторым постоянным параметром
в уравнении зависит не только от интервала температур, но и от вита процесса подвода теплоты, характеризуемого некоторым постоянным параметром 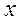 , которым может быть объем тела
, которым может быть объем тела  , давление
, давление 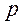 и др. общее количество теплоты, полученное в данном процессе, определяется выражением
и др. общее количество теплоты, полученное в данном процессе, определяется выражением
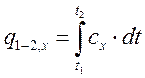 (1.13.2)
(1.13.2)
На примере идеального газа. Имеем 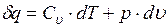 , или заменив
, или заменив 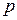 на
на 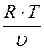 , получим
, получим 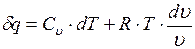
Разделив обе части последнего уравнения на 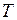 , находим
, находим
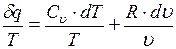 (1.13.3)
(1.13.3)
Выражение 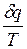 при обратимом изменении состояния газа есть полный дифференциал некоторой функции переменных
при обратимом изменении состояния газа есть полный дифференциал некоторой функции переменных 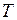 и
и 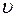 (
( 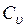 зависит только от температуры, а
зависит только от температуры, а  - величина постоянная). Клаузиус назвал эту функцию энтропия и обозначил
- величина постоянная). Клаузиус назвал эту функцию энтропия и обозначил 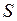 в джоулях на градус (Дж/К).
в джоулях на градус (Дж/К).
Таким образом, дифференциал энтропии для обратимого изменения состояния определяется как
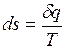 (1.13.4)
(1.13.4)
Удельная энтропия является параметром состояния, и изменение ее в любом термодинамическом процессе полностью определяется крайними состояниями тела и не зависит от пути процесса.
Интегрируя определяем
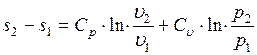 (1.13.5)
(1.13.5)
Дата добавления: 2015-08-11; просмотров: 1298;
