Природа химической связи.
Химическая связь образуется только в том случае, если при сближении атомов полная энергия системы (Екин.+Епот.) понижается.
Рассмотрим природу химической связи на примере молекулярного иона водорода H2+. (Он получается при облучении молекул водорода Н2 электронами; в газовом разряде). Для такой простейшей молекулярной системы наиболее точно решается уравнение Шредингера.
В ионе водорода Н2+ один электрон движется в поле двух ядер – протонов. Расстояние между ядрами равно 0,106 нм, энергия связи (диссоциация на атомы Н и ион Н+) составляет 255,7 кДж/моль. То есть частица прочная.
В молекулярном ионе Н2+ действуют электростатические силы двух типов – силы притяжения электрона к обоим ядрам и силы отталкивания между ядрами. Сила отталкивания проявляется между положительно заряженными ядрами НА+ и НА+, что можно представить в виде следующего рис. 3. Сила отталкивания 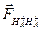
 стремится развести ядра друг от друга.
стремится развести ядра друг от друга.
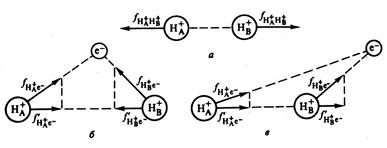
Рис. 3. Сила отталкивания (а) и притяжения (б) между двумя ядрами, возникающая при их сближении на расстояния порядка размеров атомов.
Силы притяжения действуют между отрицательно заряженным электроном е − и положительно заряженными ядрами Н+ и Н+. Молекула образуется в том случае, если равнодействующая сил притяжения и отталкивания равна нулю, то есть взаимное отталкивание ядер должно быть скомпенсировано притяжением электрона к ядрам. Такая компенсация зависит от расположения электрона е −относительно ядер (рис.3 б и в). Здесь имеется в виду не положение электрона в пространстве (что нельзя определить), а вероятность нахождения электрона в пространстве. Расположение электронной плотности в пространстве, соответствующий рис. 3.б) способствует сближению ядер, а соответствующее рис. 3.в) – расталкиванию ядер, так как в этом случае силы притяжения 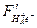 направлены в одну сторону и отталкивание ядер не компенсируется. Таким образом, имеется область связывания, когда электронная плотность распределена между ядрами и область разрыхления или антисвязывания, когда электронная плотность распределена за ядрами.
направлены в одну сторону и отталкивание ядер не компенсируется. Таким образом, имеется область связывания, когда электронная плотность распределена между ядрами и область разрыхления или антисвязывания, когда электронная плотность распределена за ядрами.
Если электрон попадает в область связывания, то химическая связь образуется. Если же электрон попадает в область разрыхления, то химическая связь не образуется.
В зависимости от характера распределения электронной плотности в области связывания различают три основных типа химической связи: ковалентную, ионную и металлическую. В чистом виде эти связи не имеют места, и обычно в соединениях присутствует комбинация этих типов связи.
Дата добавления: 2015-08-08; просмотров: 1038;
