Графическое определение константы скорости нулевого порядка.
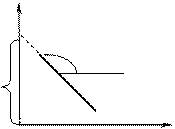 cЗдесь
cЗдесь 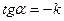
α
с0
τ
2. Реакции первого порядка.
υ = 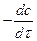 = kc1,
= kc1, 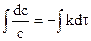 , ln c = - k×t + const,
, ln c = - k×t + const,
когда t = 0, ln c0 = const, c = c0, ln c – ln c0 = - k×t, ln c0 – ln c = k×t, 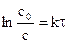 ,
, 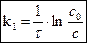 ,
,
где с0 – исходная концентрация;
с – концентрация в данный момент времени;
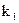 - константа скорости химической реакции 1-ого порядка.
- константа скорости химической реакции 1-ого порядка.
Дата добавления: 2015-08-08; просмотров: 1004;
