Определение процесса
Термодинамический процесс, протекающий при неизменной теплоёмкости, называется п о л и т р о п н ы м.
Название “политропный” происходит от греческих слов “поли” – много и “тропос” – направление, путь. В политропном процессе в общем случае могут изменяться все термодинамические и калорические параметры кроме теплоёмкости, которую обозначают через cп.
Вывод уравнения процесса.
Для вывода уравнения используем выражение первого закона термодинамики, записанное через энтальпию и внутреннюю энергию:
dq = di - vdp и dq = du + pdv.
Выразив через теплоемкости записанные выражения, получим:
cп dT = cp dT – vdp и cпdT = cv dT + pdv.
Отсюда
(сп – сp)dT = -vdp и (cп –cv)dT = pdv.
Разделим почленно первое уравнение на второе:

 .
.
Здесь левая часть равенства определяется только теплоемкостью рабочего
Разделим почленно первое уравнение на второе:
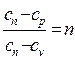 . (2.43)
. (2.43)
Проведя разделение переменных, получим:
n 
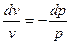 .
.
После интегрирования этого соотношения в пределах от начала до конца процесса и антилогарифмирования, будем иметь:
p1 v1n = p2 v2n.
Отсюда следует, что
р vn = const. (2.44)
 Выражение (2.44) называется у р а в н е н и е м п о л и т р о п н ог о п р о ц е с с а. Оно устанавливает связь между параметрами состояния в процессе с теплоемкостью
Выражение (2.44) называется у р а в н е н и е м п о л и т р о п н ог о п р о ц е с с а. Оно устанавливает связь между параметрами состояния в процессе с теплоемкостью
cn = const. Показатель степени n в уравнении называют п о к а з а т е - л е м п о л и р о п ы. Он принимает для каждого сn конкретное числовое значение и, как изображено на рис.2.5, может меняться от - ∞ до +∞. Здесь зависимость теплоемкости политропного процесса от показателя n получена из (2.43) в виде
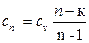 . (2.45)
. (2.45)
Рис. 2.5
Дата добавления: 2015-08-04; просмотров: 704;
