Средства детонирования 1 страница
Средства детонирования предназначаются для вызова детонации заряда бризантных веществ. К ним относятся капсюли-детонаторы и детонирующий шнур.
Капсюли-детонаторы классифицируются:
- по назначению: на артиллерийские, применяемые в боеприпасах различного действия, и подрывные, применяемые в подрывном деле;
- по устройству: на простые, состоящие из одного инициирующего вещества, и комбинированные, состоящие из нескольких взрывчатых веществ – инициирующих и бризантных; последние обладают более сильным инициирующим действием, чем простые, а также большой стойкостью к сотрясению при выстреле и меньшей опасностью в обращении;
- по отношению к начальному импульсу: на лучевые и накольные.
Для снаряжения комбинированных капсюлей-детонаторов в качестве первичного (инициирующего) вещества применяется азид свинца, обладающий высокой инициирующей способностью. Из-за недостаточной чувствительности азида свинца над ним размещают запрессовку из более чувствительного воспламенительного состава, например, для капсюлей накольного действия смесь из ТНРС, тетразена, нитрата бария и антимония.
В качестве вторичного вещества используется бризантное ВВ – тетрил, который усиливает действие капсюля-детонатора.
Капсюль-детонатор состоит из оболочки (колпачка), капсюльного состава и чашечки (рисунок 6).
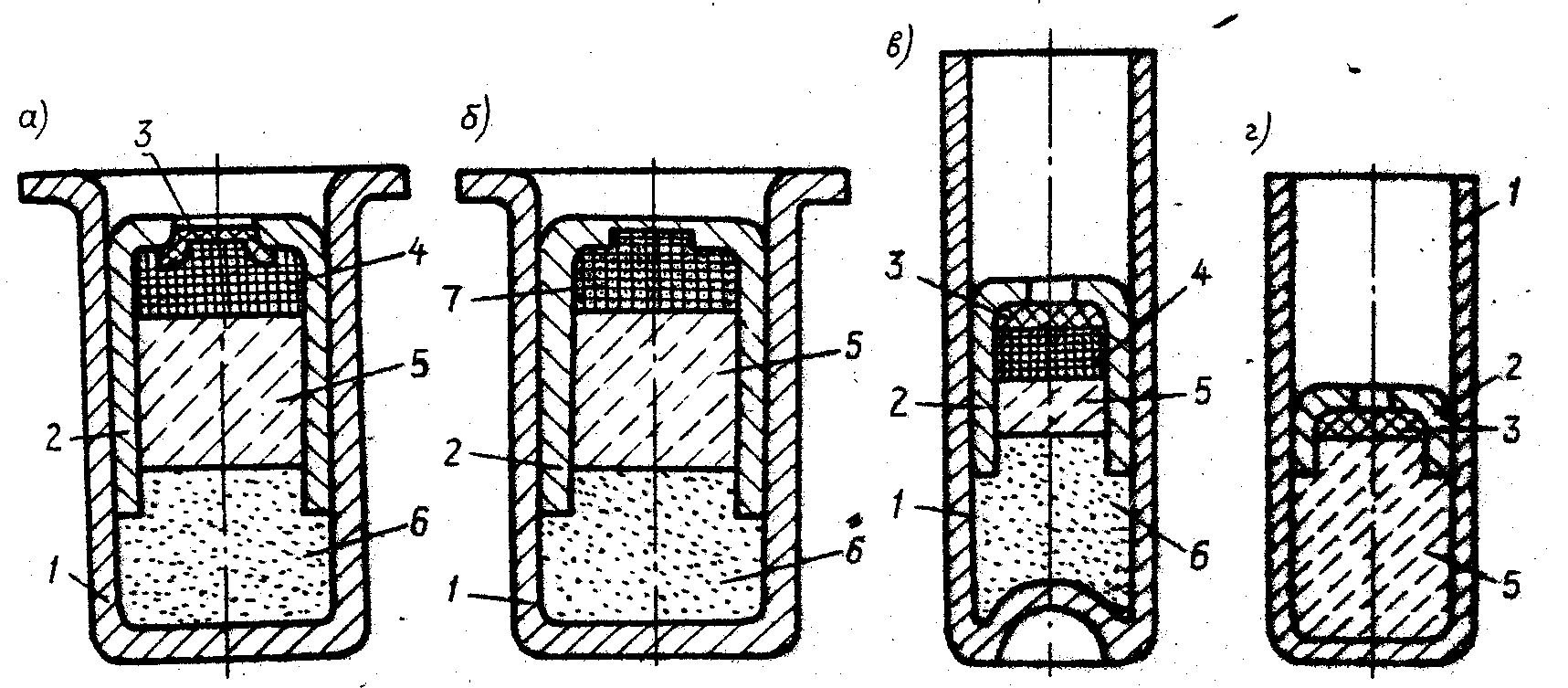
1 − колпачок; 2 – чашечка; 3 – сетка шелковая; 4 – ТНРС; 5 – азид свинца; 6 – тетрил; 7 – накольный состав
Рисунок 6 – Капсюли-детонаторы: а – лучевой; б – накольный;
в – капсюль-детонатор № 8; г – простой
Детонирующий шнур предназначен для быстрой передачи детонации на расстояние. По конструкции он подобен огнепроводному и отличается в основном сердцевиной, состоящей из бризантного взрывчатого вещества.
1.9 Бризантные взрывчатые вещества [3]
По составу бризантные ВВ разделяются на две большие группы: индивидуальные вещества и взрывчатые смеси.
Наиболее распространенные индивидуальные бризантные ВВ относятся к органическим азотистым соединениям ароматического, алифатического и гетероциклического рядов, в том числе к нитросоединениям, содержащим группу NO2 (тротил, динитронафталин, тринитро-бензол, нитрометан), нитратам спиртов, содержащим группу ОNO2 (нитроглицерин, нитрогликоли, ТЭН), нитраминам, содержащим группу N-NO2 (тетрил, гексоген, октоген). Из неорганических соединений слабые взрывчатые свойства имеют аммониевые соли азотной (аммиачная селитра) и хлорной кислот (перхлорат аммония).
Вторую группу составляют взрывчатые смеси, которые состоят либо из окислителя и горючего, либо из одного или нескольких индивидуальных ВВ и различного рода добавок.
Во взрывчатых смесях типа окислитель–горючее в качестве окислителя применяют минеральные соли, способные при разложении выделять свободный кислород. К ним относятся соли кислот: азотной (нитраты аммония, калия, натрия и др.), хлорной (перхлораты аммония, натрия, калия) и хлорноватой (хлорат калия). В качестве горючего во взрывчатых смесях используют высококалорийные органические соединения (продукты переработки нефти, производные целлюлозы и др.), металлы и их соединения (алюминий, ферросилиций и др.), индивидуальные ВВ с отрицательным кислородным балансом, выделяющие при своем разложении горючие газы – оксид углерода, водород, метан и сажу (тротил, динитронафталин и др.).
На практике часто применяют смеси индивидуальных ВВ с металлами, в которых ВВ выступает в роли окислителя по отношению к металлу, например, смесь тротила с алюминием.
Взрывчатые смеси второго типа компонуются для достижения каких-либо специальных свойств ВВ, например, для снижения температуры плавления гексогена и октогена. Их смешивают с тротилом, у которого низкая температура плавления. К многим мощным индивиду-альным ВВ для снижения их чувствительности к механическим воздействиям добавляют небольшое количество низкоплавких углеводородов (воск, парафин, церезин). Такие вещества называются флегматизаторами. В другие смеси вводят вещества, повышающие чувствитель-ность к инициирующему импульсу. В данном случае эти вещества называются сенсибилизаторами. В качестве сенсибилизатора часто применяют нитроглицерин.
К важнейшим классам взрывчатых смесей относятся:
- аммониты, или аммиачно-селитренные ВВ, состоящие из смеси аммиачной селитры с нитросоединениями;
- сплавы и смеси нитросоединений;
- нитроглицериновые ВВ (динамиты);
- хлоратные и перхлоратные ВВ – смеси солей хлорноватой и хлорной кислот с нитросоединениями;
- взрывчатые смеси на основе жидких окислителей;
- смеси твердого окислителя с горючими веществами (например, аммиачная селитра с дизельным топливом).
Бризантные ВВ широко применяются в военном деле для снаряжения артиллерийских снарядов, бомб, торпед, мин и боевых частей ракет. Также ВВ используются для приготовления твердого ракетного топлива, для возбуждения взрыва атомных бомб и др. ВВ получили широкое применение в различных отраслях народного хозяйства: горной промышленности, на гидромелиоративных работах, в сельском хозяйстве, нефтедобывающей промышленности и т.д. ВВ, используемые для этих целей, называются промышленными ВВ (ПВВ).
В качестве исходных компонентов для рецептур военных ВВ используются штатные ВВ (тротил, гексоген, октоген и др.), к которым предъявляются жесткие требования по технологии производства.
Военные ВВ должны обладать высокой мощностью, бризантностью и фугасностью, большой скоростью детонации, а компоненты, входящие в состав, иметь высокую степень очистки, необходимую химическую и физическую стойкости, обеспечивающие стабильные свойства ВВ в течение длительного времени хранения боеприпасов. Данные характеристики необходимы, чтобы гарантировать максимальный разрушающий и поражающий эффекты, надежность и безотказность, высокую воспроизводимость всех параметров боеприпасов.
К промышленным ВВ таких жестких требований не предъявляют. Большинство технических задач, связанных с применением взрывчатых технологий, может быть решено менее мощными ВВ, чем военные, обладающими значительно меньшими скоростями детонации и теплотворной способностью, относительно невысокой степенью очистки компонентов. Они могут быть менее бризантными и фугасными, а в отдельных случаях иметь лишь «мягкий» раскалывающий эффект. Для ПВВ химическая и физическая стойкости не должны определяться десятилетиями, поскольку их реализация после изготовления происходит, как правило, в течение короткого промежутка времени.
Вместе с тем к ПВВ предъявляется ряд специфических требований:
- производство должно опираться на хорошо развитую и доступную сырьевую базу;
- технология производства должна быть простой и осуществляться доступными техническими средствами;
- продукты взрыва не должны быть токсичными, должны быть экологически чистыми, чтобы не оказывать вредное воздействие на окружающую среду;
- должны обладать низкой чувствительностью к механическим и тепловым воздействиям и быть безопасными при обращении и транспортировке;
- взрыв заряда не должен являться причиной возгорания или взрыва шахтных газов (например, метана), угольной пыли;
- себестоимость не должна быть высокой.
Рассмотрим некоторые виды бризантных ВВ.
1.9.1 Нитроглицерин [3, 4, 10, 11]
Нитроглицерин, или тринитрат глицерина (ТНГ), получают обработкой глицерина смесью азотной и серной кислот (47–50 % НNO3,
49–53 % H2SO4). Реакция получения ТНГ следующая:
C3H5(OH)3 + 3HNO3 C3H5(ONO2)3 + 3H2O
Этерификация протекает последовательно в три ступени: в первой получается мононитрат, во второй – динитрат и в третьей – тринитрат глицерина. Более 60 лет нитроглицерин получали по периодической схеме (метод Нобеля и метод Натана). При получении пери-одическими способами на фазах сепарации и очистки нитроглицерина от кислот скапливалось около 2–3 тонн нитроглицерина, что в случае аварии приводило к практически полному разрушению оборудования и производственных зданий.
В настоящее время в производстве применяются в основном непрерывные методы. При непрерывном методе в процессе находится меньшее количество ВВ, благодаря чему снижается опасность производства.
Нитрование глицерина происходит в нитраторе непрерывного действия в среде отработанной кислоты (рисунок 7).
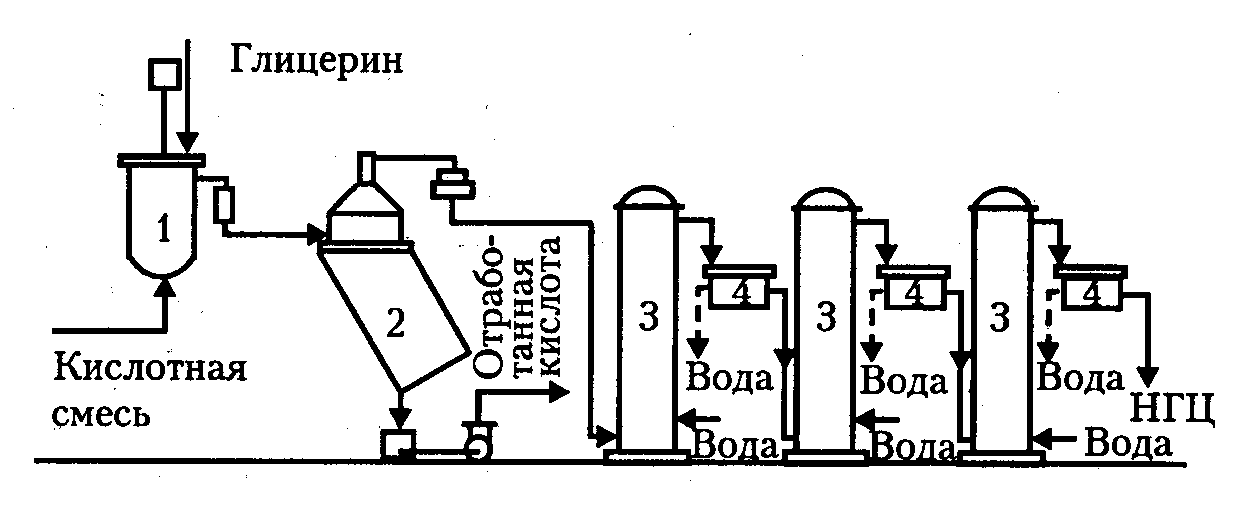
1 – нитратор; 2, 4 − сепараторы; 3 − промывные колонны
Рисунок 7 − Технологическая схема непрерывного процесса
производства нитроглицерина
После нитрации глицерина в нитраторе получается эмульсия нитроглицерина в отработанной кислоте, которую необходимо быстро отделить от отработанной кислоты. Разделение нитроглицерина и отработанных кислот основано на различии их плотностей и осущест-вляется на фазе сепарации. Возможны два способа сепарации:
1. Из концентрированных кислотных смесей, когда плотность нитроглицерина меньше плотности кислотной смеси. В этом случае нитроглицерин собирается в верхней части сепаратора и сливается через верхнюю переливную трубу за счет притока новой порции кислотной смеси. Данный способ получения нитроглицерина назван сепарационным.
2. Из разбавленной кислотной смеси. В этом случае плотность нитроглицерина оказывается больше, чем разбавленной кислотной смеси, и нитроглицерин собирается в нижней части аппарата. Этот метод получения нитроглицерина называется бессепарационным, хотя принципиально неверно, т.к. операция сепарации имеется.
Первый метод получения нитроглицерина более экономичен, т.к. отработанная кислота может быть снова использована в производстве, а второй метод является более безопасным, т.к. разбавленная отработанная кислота менее реакционноспособна.
После отделения от кислоты нитроглицерин поступает на стабилизацию для более глубокой очистки его от кислот и примесей (сульфо- и сульфонитроэфиров, неполных нитратов), которые снижают химическую стойкость основного продукта. Стабилизация заключается в проведении многократных водных и щелочных промывок.
Существует более современный метод получения нитроглицерина, который был разработан в Швеции, это инжекторный метод.
Особенностью этой технологической схемы (рисунок 8) является проведение нитрации глицерина в инжекторе при повышенной температуре (46–48 °С) под вакуумом и отделение нитроглицерина от отработанных кислот в центрифуге.
Свойства нитроглицерина.Химически чистый нитроглицерин – это маслообразная, бесцветная, прозрачная жидкость. Плотность
1600 кг/м3 (1,6 г/см3). Затвердевая, может образовывать две формы:
лабильную, с температурой затвердевания 2,1 °С, и стабильную, с температурой затвердевания 13,2 °С. Нитроглицерин частично растворим в воде: при 20 °С в одном литре воды растворяется 1,8 г нитроглицерина, а при 50 °С – 2,5 г.
Нитроглицерин хорошо растворяется во многих органических растворителях: ацетоне, диэтиловом эфире, метиловом спирте, бензоле, толуоле, ксилоле, нитробензоле и многих других. Нитроглицерин сам хорошо растворяет динитротолуол и тринитротолуол, что имеет большое значение для производства пластичных и желатинирован-
ных ВВ. В нитроглицерине растворяется нитроцеллюлоза с содержанием азота около 12 % (коллоксилин). Это свойство используется при изготовлении бездымного нитроглицеринового пороха и желатин-ди-намитов.
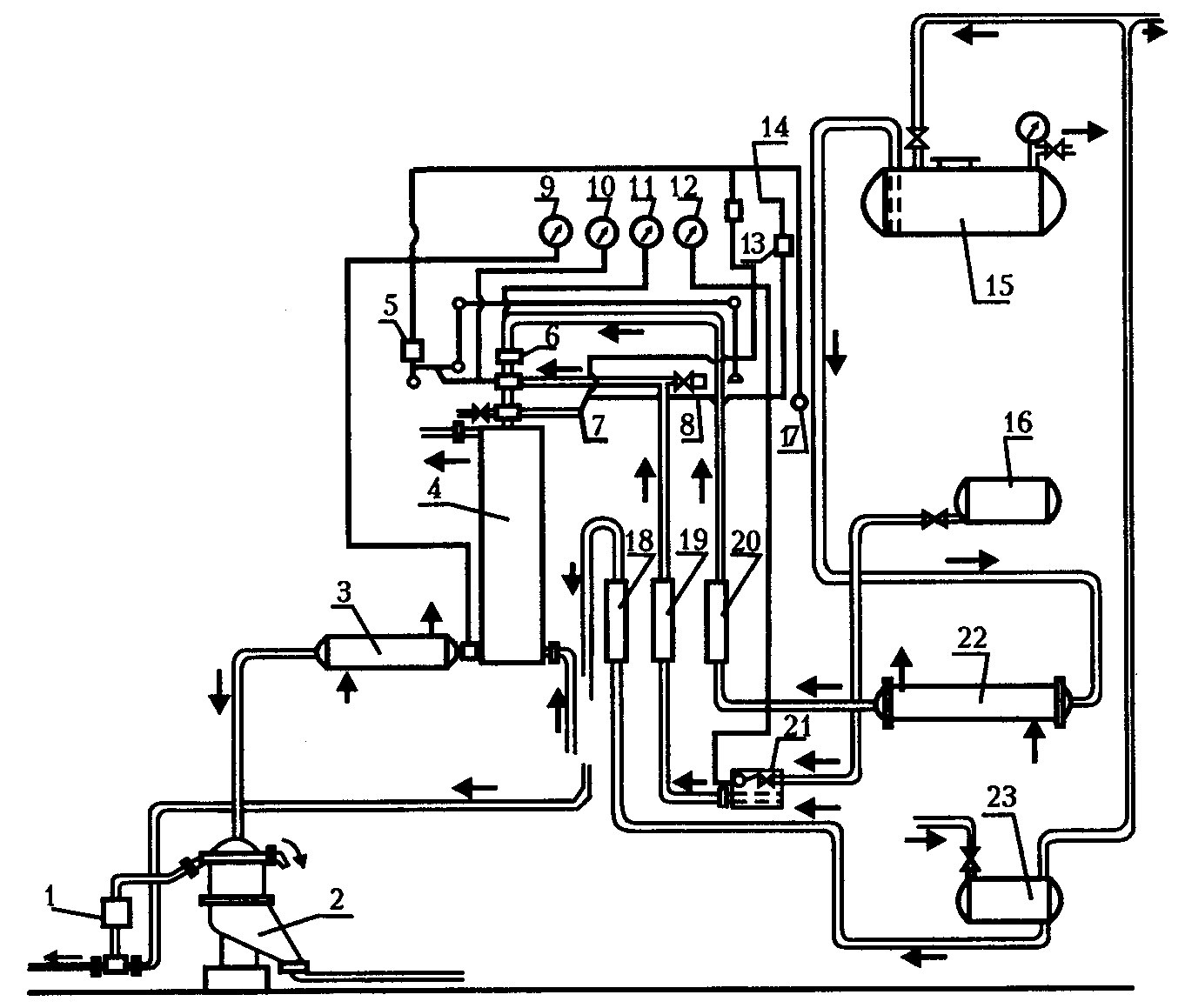
1 − инжектор для подачи водной эмульсии нитроглицерина на фазу
стабилизации в промывные колонны; 2 − центрифуга;
3, 22 − кожухотрубные теплообменники; 4 − холодильник;
5 − электромагнит; 6 − инжектор-нитратор; 7, 9, 11, 12 − термометры;
8 − игольчатый клапан для впуска воздуха в инжектор;
10 − вакуумметр; 13 − электромагнитное реле; 14 − сигнальный
колокол; 15 − хранилище кислотной смеси; 16 − хранилище глицерина; 17 − выключатель; 18 − ротамер для воды; 19 − ротамер для глицерина; 20 − ротамер для кислотной смеси; 21 − засасывающий бак
с постоянным уровнем для глицерина; 23 − хранилище воды
Рисунок 8 − Технологическая схема получения нитроглицерина
инжекторным методом (фаза нитрации и сепарации)
Нитроглицерин горит на воздухе зеленоватым пламенем со вспышками и треском. Горение большого количества нитроглицерина сопровождается взрывом. При быстром нагревании до 180 °С нитроглицерин взрывается. При медленном нагревании температура вспышки нитроглицерина 215–218 °С. Нитроглицерин очень чувствителен к удару и трению. При испытании на вертикальном копре при стандартных условиях дает 100 % взрывов. В этом случае нитроглицерин приближается к инициирующим ВВ, поэтому в чистом виде он не перевозится. Взрывчатое разложение нитроглицерина происходит по уравнению:
2C3H5(ONO2)3 = 6СО2 + 5H2O + 3N2 + 0,5О2.
Скорость детонации жидкого нитроглицерина 1100−2000 м/с. Нитроглицерин применяется в качестве пластификатора нитроцеллюлозы при изготовлении баллиститных порохов, а также для приготовления динамита, который состоит из 92−93 % нитроглицерина и 7−8 % коллоксилина. Применяется нитроглицерин для получения промышленных ВВ (угленитов). ТНГ нашел широкое применение в медицине для лечения сердечно-сосудистых заболеваний. Лекарственные препараты на его основе готовятся либо в виде таблеток, либо в виде капсул (раствор нитроглицерина в подсолнечном масле).
1.9.2 Гексоген [3,4]
Химическое название – циклотриметилентринитроамин. Химическая формула:
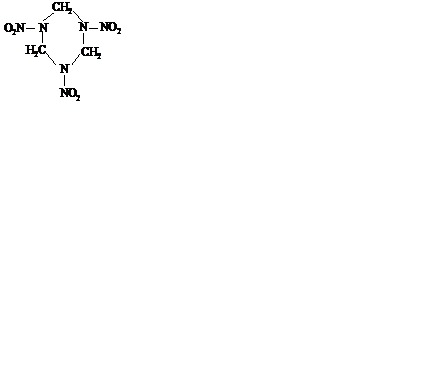
Получают гексоген нитрованием уротропина, причем существует несколько методов получения: окислительный, метод «К», уксусно-ангидридный.
Окислительный метод заключается в обработке уротропина концентрированной азотной кислотой, выделении гексогена из отработанной кислоты, фильтровании, промывке и сушке.
По методу «К» уротропин подвергается нитролизу раствором аммиачной селитры в концентрированной азотной кислоте.
Уксусно-ангидридный метод имеет несколько вариантов, один из которых (метод «КА») состоит из следующих операций: получение динитрата уротропина, получение тринитрата аммония и нитролиз динитрата уротропина тринитратом аммония в присутствии уксусного ангидрида.
Свойства и применение гексогена.Гексоген представляет собой кристаллическое белое вещество без запаха и вкуса. Он является сильным ядом, поэтому при работе с ним необходимо соблюдать правила техники безопасности. Плотность гексогена 1816 кг/м3 (1,816 г/см3), температура плавления 204,5–205 °С. При нагревании гексоген начинает разлагаться при 203 °С, причем при данной температуре отмечается повышенная чувствительность его к удару и трению. Поэтому снаряжение им боеприпасов производят не заливкой, а только прессованием. Для уменьшения чувствительности к удару и трению его флегматизируют парафином, воском, церезином и другими веществами.
Гексоген является мощным бризантным веществом. Скорость детонации при плотности 1700 кг/м3 (1,7 г/см3) равна 8380 м/с.
Чистый гексоген применяется для изготовления капсюлей-дето-наторов и как энергетическая добавка в некоторых составах баллиститных порохов. Гексоген в смеси с другими ВВ находит применение для снаряжения артиллерийских снарядов, авиационных бомб, морских мин, торпед.
1.9.3 Октоген [3,4]
Химическое название циклотетраметилентетранитрамин. Химическая формула:
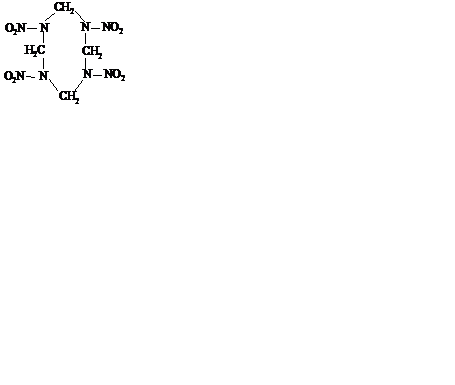
Октоген существует в четырех кристаллических модификациях (α, β, γ, δ). Получают октоген нитролизом уротропина нитратом аммония в азотной кислоте в присутствии уксусного ангидрида и параформальдегида. Мольное соотношение компонентов подбирают так, чтобы обеспечивался максимальный выход октогена при минимальном выходе гексогена. Получают продукт, который содержит 30–40 % гексогена и 60–70 % октогена. Затем октоген отделяют от гексогена. Разделение основано на значительно большей (в четыре раза) растворимости гексогена в ацетоне, чем октогена. Проводят обработку продукта трехкратным количеством ацетона, при этом почти весь октоген отфильтровывают.
Гексоген выделяют путем разбавления ацетонового раствора водой (гексоген выпадает в осадок).
Выход чистого октогена составляет 50–55 % по уротропину.
Свойства октогена и его применение.Октоген – это высокоплавкое белое кристаллическое вещество. На практике нашла применение β-форма октогена, температура плавления которой 270 °С. По сравнению с гексогеном он более термостоек. Температура начала разложения 220 °С, поэтому октоген плавится с разложением. Скорость детонации при плотности 1900 кг/м3 (1,9 г/см3) составляет 9124 м/с.
Высокая термостойкость октогена позволяет использовать его в зарядах, подверженных воздействию высоких температур, например, при проведении взрывных работ в глубоких и сверхглубоких скважинах, в боеприпасах для сверхзвуковой авиации. По сравнению с гексогеном у октогена более высокая скорость детонации, большая бризантность и мощность.
Применяют октоген в качестве энергетической добавки в твердых ракетных топливах и артиллерийских порохах, также используют как в виде самостоятельных зарядов, так и в смеси с тротилом (октолы).
1.9.4 Нитраты целлюлозы [4, 11–16]
Нитраты целлюлозы (НЦ) получают действием на целлюлозу азотно-серной кислотной смеси с небольшим добавлением воды. Реакция протекает по следующей схеме:
[C6H7O2(OH)3]m+mnHNO3  [C6H7O2(OH)3(ONO2)n]m+mnH2O,
[C6H7O2(OH)3(ONO2)n]m+mnH2O,
где n – степень этерификации;
m – степень полимеризации.
Серная кислота необходима для активации азотной кислоты и связывания воды, выделяющейся во время реакции.
Изменяя состав кислотной смеси, можно получить нитраты целлюлозы с разной степенью этерификации, то есть с разным содержанием азота. Важными показателями являются также растворимость нитратов целлюлозы в органических растворителях (определяет расход растворителей при их переработке) и вязкость (определяет механическую прочность пленок или каких-либо изделий).
В зависимости от содержания азота в них, растворимости в спиртово-эфирной смеси и вязкости 2%-ных растворов НЦ в ацетоне выпускают марки нитратов целлюлозы, представленные в таблице 1.
Таблица 1 − Технические характеристики нитратов целлюлозы
| Вид нитрата целлюлозы | Техническое название | Содержание азота | Условная вязкость, мПа·с (оЭ − градус Энглера) | Область применения | |
| N, % | мл NO/г | ||||
| Лаковый высоковязкий коллоксилин | Коллоксилин ВВ | 11,91− 12,29 | 190−196 | 8,5−10,6 (1,9−2,2) | Авиалаки, изоляционные лаки |
| Лаковый средневязкий коллоксилин | Коллоксилин СВ | 11,91− 12,29 | 190−196 | 3,8−8,4 (1,31−1,89) | Лаки для дерева, искусственной кожи, клеящие составы |
| Лаковый низковязкий коллоксилин | Коллоксилин НВ | 11,91− 12,29 | 190−196 | 1,9−3,7 (1,11−1,30) | Эмали, грунтовки, шпаклевки, клеящие составы |
| Лаковый весьма низковязкий коллоксилин | Коллоксилин ВНВ | 11,91− 12,29 | 190−196 | 1,1−1,8 (1,03−1,10) | Лаки для металла, эмали для машин |
| Лаковый полусекундной вязкости коллоксилин | Коллоксилин ПСВ | 11,91− 12,29 | 190−196 | 0,6−1,0 (0,98−1,02) | Лаки для мебели, бумаги, нитропленки |
| Лакомастичный коллоксилин | Коллоксилин ЛМ | 10,66− 12,41 | 170−198 | 3,7−15,8 (1,3−3,0) | Мастика для изготовления технических тканей |
| Целлулоидный коллоксилин | Коллоксилин ЦК | 10,97− 11,22 | 175−179 | 6,2−10,6 (1,6−2,2) | Мячи для нас-тольного тенниса |
| Коллоксилин «Н» | Коллоксилин НХ, НД | 11,85− 12,29 | 189−196 | 8,5−15,8 (1,9−3,0) | Для баллиститных порохов |
Продолжение таблицы 1
| Пироксилин №1 | Пироксилин 1П | не менее 13,10 | не менее 209 | 8−12 | Для пироксилиновых порохов |
| Пироксилин №2 | Пироксилин 2П1, 2П2, 2П3 | 11,79−12,41 | 188−198 | 6−10 | Для пироксилиновых порохов |
1.9.4.1 Влияние некоторых факторов на процесс нитрования
целлюлозы
Влияние свойств целлюлозы на процесс этерификации.Реакционная способность полимеров в значительной мере зависит от доступности реакционноспособных функциональных групп. Для целлюлозы, ректификация которой протекает гетерогенно, определяющей ско-рость реакции стадией является проникновение нитрующего агента (азотной кислоты) внутрь волокна. Скорость реакции также зависит от величины и характера внутренней поверхности целлюлозы (от величины внутренней поверхности зависит количество сорбированной в начальный момент нитросмеси). Скорость капиллярной пропитки зависит от поверхностного натяжения нитрационной смеси, от ее способ-ности удержаться на стенках капилляров, а также от впитывающих свойств целлюлозы.
Образцы целлюлозы могут отличаться по характеру и величине своей поверхности. Целлюлоза - гидрофильный материал, однако в зависимости от метода обработки (в частности, от условий сушки), а также от характера примесей она способна гидрофобизоваться. Образцы целлюлозы, высушенные при температурах более 120 °С, обладают малой реакционной способностью. При нагревании может происходить смыкание макромолекулярных цепей, особенно при наличии на поверхности гидрофобных примесей: сорбированных смол, лигнина и продуктов их распада. Этим объясняется более низкая, как правило, реакционная способность древесной целлюлозы. По сравнению с хлопковой древесная целлюлоза впитывает в начальный момент времени меньшее количество нитрационных смесей. При обработке образцов древесной целлюлозы поверхностно-активными веществами (ПАВ) улучшается ее впитывающая способность за счет экранирования ими гидрофобных участков.
На реакционную способность влияет удельная поверхность целлюлозы. При ее увеличении скорость реакции возрастает. Для образцов микрокристаллической целлюлозы (МКЦ) с развитой поверхностью этерификация заканчивается за 1,5–2,0 мин. Микрокристаллическая целлюлоза получается при кислотном гидролизе древесной и хлопковой целлюлозы. Увеличения скорости этерификации можно достигнуть, предварительно измельчив целлюлозу. Для измельченных образцов древесной целлюлозы реакция практически заканчивается через
2–5 мин. Для образцов с большой удельной поверхностью процесс этерификации можно проводить при малых модулях, поскольку для окончания реакции достаточно поглощенной за счет капиллярного впитывания кислоты.
Этерификация целлюлозы – гетерогенный процесс, скорость которого определяется массопередачей. Особенностью протекания такой реакции является увеличение диффузного сопротивления во времени. Скорость реакции зависит от толщины слоя целлюлозного материала, через который проникает нитрующий агент, особенно при этерификации образцов бумаги с различной плотностью.
Наиболее легко этерификация протекает для рыхлых бумаг, в которых целлюлозные волокна находятся на большом расстоянии друг от друга. Образцы бумаги с меньшей средней плотностью нитруются быстрее, и наиболее удобной для этерификации физической формой является папка. Однако рыхлая бумага и папка нетехнологичны: уменьшается загрузка нитрационных аппаратов, и ухудшаются расходные коэффициенты кислотных смесей из-за сложности их рекуперации. Но бумага при соответствующей плотности является наиболее удобной физической формой целлюлозы для нитрации, так как возможно более равномерное протекание реакции и получение более однородных продуктов. Существенна при этом однородность бумаги по толщине и плотности.
Применяемая для нитрации древесная целлюлоза в форме рулонной бумаги (РБ) не всегда удовлетворяет этим требованиям. Более плотные слои бумаги хуже впитывают нитросмесь, медленнее нитруются, и это приводит к неоднородности нитратов целлюлозы. Хорошей реакционной способностью обладают образцы композиционной бумаги (КБ), полученной из смеси древесной и хлопковой целлюлозы. Хлопковая целлюлоза, благодаря своей более развитой капиллярной системе, облегчает проникновение нитрующего агента в КБ. Новый вид КБ для нитрации был получен из древесной целлюлозы и короткоштапельного линта аэрохимического съема, применение которого позволяет получить образцы бумаги с хорошими впитывающими свойствами и высокой реакционной способностью.
РБ и КБ - наиболее перспективные виды целлюлозного сырья для этерификации по своим физико-химическим характеристикам и технологическим свойствам. Причем использование целлюлозы в форме РБ позволит перейти к единой форме целлюлозы для получения ее нитратов.
Повысить реакционную способность целлюлозных материалов можно за счет химической активности. Наиболее эффективна активация аммиаком или простейшими аминами (метиламином, этиламином и др.). При обработке аммиаком диаметр капилляров может увеличиваться в 2–3 раза, что облегчает стадию проникновения нитрующего агента. Наиболее эффективна для этерификации целлюлозы низкотемпературная (при минус 50 °С) активация аммиаком. Поскольку при удалении аммиака диаметр капилляров уменьшается до первоначального значения, активизацию целесообразно проводить непосредственно перед этерификацией целлюлозы. Как уже отмечалось, для данной нитрационной смеси скорость реакции зависит от вида целлюлозного материала, характера примесей, физической формы. Собственно химическая реакция протекает очень быстро, и скорость реакции определяется условиями протекания диффузной стадии.
Влияние модуля этерификации.Модулем этерификации называется массовое соотношение между нитрующей смесью и нитруемой целлюлозой. Сапожников полагал, что для получения однородных нит-ратов целлюлозы необходим большой избыток азотной кислоты или кислотной смеси по отношению к целлюлозе, и состав их во время нитрации должен оставаться постоянным.
Шмидт также считал, что однородный по составу нитрат целлюлозы можно получить, если нитрационная смесь в процессе этерификации мало меняется по составу, в частности, при большом количестве нитрационных смесей.
Состав нитрационных смесей к концу этерификации изменяется вследствие вступления азотной кислоты в реакцию этерификации и выделения реакционной воды. Это изменение тем больше, чем меньше модуль нитрации. Но так как степень этерификации целлюлозы определяется не первоначальным состоянием нитрационной смеси, а составом, который установится в конце этерификации при равновесии процессов, то модуль оказывает определенное влияние на степень этерии-фикации и свойства получаемых нитратов целлюлозы. При существующих методах нитрации для ускорения смачивания целлюлозы количество азотной кислоты и кислотной смеси должно в 10–12 раз превышать теоретически необходимое. Избыток кислотных смесей по отношению к целлюлозе необходим также для протекания диффузионных процессов выравнивания.
Для большей однородности нитратов целлюлозы желательно применять большой модуль этерификации, однако это снижает производительность аппаратуры и приводит к большому количеству находящихся в обороте кислотных смесей.
В существующих производствах нитратов целлюлозы этерификацию целлюлозы осуществляют при модулях 1:25–1:40 в зависимости от марки сырья.
Температура этерификации. Повышение температуры этерификации ускоряет процесс начального накопления азота в НЦ. Опытными данными Лунге показано, что если за 30 минут нитрования при 0 °С содержание азота в нитрате целлюлозы достигает 10,71 %, то при 19°С – 12,72 % и при 40°С – 13,1 %. Из этого следует, что изменение температуры незначительно влияет на степень этерификации. Согласно диффузионной теории Малахова, скорость этерификации целлюлозы определяется не скоростью химической реакции, а суммой скоростей про-цессов диффузии и массопередачи. Температура в какой-то степени ускоряет реакцию этерификации, но практически не влияет на конечный результат степени этерификации целлюлозы.
Дата добавления: 2015-08-01; просмотров: 3872;
