Строение, структура и дефекты материалов пар трения
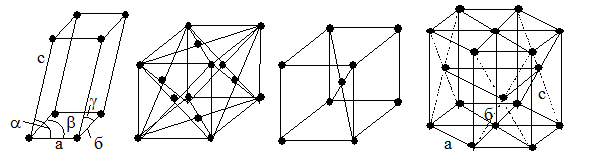
Конструкционные материалы, применяемые в узлах трения, делятся на кристаллические и аморфные. С физической точки зрения твердыми телами считаются только кристаллы. Их атомы располагаются в узлах регулярной пространственной структуры - кристаллической решетки, структурной единицей которой является элементарная ячейка. Примеры ряда структурных схем кристаллов приведены на рис. 3.1.
В общем случае элементарная ячейка имеет вид косоугольного параллелепипеда (рис. 3.1,а), характеризуемого значениями сторон а, б, с и углов a, b, g. По соотношению сторон и углов выделяют 7 кристаллических систем. Наиболее распространенными являются решетки кубические (рис.3.1,б,в) и гексагональные (рис.3.1,г). Если в центрах граней куба располагаются дополнительные атомы, то решетка называется гранецентрированной (ГЦК), если атом внедряется в центр куба - решетка объемноцентрированная (ОЦК). Гексагональная плотноупакован-
|
| а б в г |
| Р и с. 3.1. Схемы элементарных ячеек |
ная решетка имеет ячейку с основанием в виде правильного шестиугольника. Кубические решетки типа ГЦК и ОЦК характерны для сталей. Между атомами в решетке возможны связи 3-х типов: ионная, ковалентная, металлическая. В первом случае в узлах находятся положительные и отрицательные ионы, во втором - нейтральные атомы, валентные электроны которых образуют пары, движущиеся в поле соседних ядер. Связь имеет квантово-механическую природу. Металлическая связь возникает между атомами металлов. Валентные электроны в этом случае обобществляются, покидают свои атомы и совершают хаотическое тепловое движение в общем поле атомных остатков, находящихся в узлах решетки (свободные электроны).
Между молекулами в молекулярных решетках действуют силы Ван-дер-Ваальса, энергия которых примерно на 2 порядка ниже, чем у атомных связей. Особым видом молекулярного взаимодействия является водородная связь. Слабоэкранированное одним электроном ядро атома водорода, участвующего в ковалентной связи, может притягиваться к сильноэлектроотрицательным атомам (кислород, фтор) и образовывать с ними вторую связь. Водородная связь прочнее других межмолекулярных. Она характерна для взаимодействия молекул углеводородов, в частности полимеров, с кислородом окислов металлов, является важнейшей формой связи между молекулами воды в жидком состоянии и в виде льда. В таблице 3.1. представлены величины энергии перечисленных видов связей и указаны характерные свойства кристаллов.
Потенциальная энергия взаимодействия между парой изолированных атомов E выражается формулой:
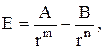 (3.1)
(3.1)
где А, В, m, n - коэффициенты. Первый член уравнения характеризует энергию сил отталкивания, второй - сил притяжения. Поскольку сила взаимодействия выражается в виде
 (3.2)
(3.2)
то
| Таблица 3.1. | |||
| Энергия связи и некоторые свойства кристаллов | |||
| Тип связи | Примеры кристаллов | Энергия связи, кДж/моль | Некоторые свойства кристаллов |
| Ионная | NaCl LiF MgO | ~ 1000 | Малая электропроводность при низких и хорошая ионная проводимость при высоких температурах. Высокие прочность, твердость и температура плавления, хрупкое разрушение |
| Ковалентная | C(алмаз), Si, Ge, TiN, WC, SiC | ~ 700 | Высокая твердость, низкая электропроводность при малых температурах, хрупкость. Некоторые материалы являются полупроводниками |
| Металлическая | Fe, Cu, Al, Ag, Na | ~ 400 | Высокая электропроводность и пластичность |
| Молекулярная | Молекулы в полимерах Ar, CH4 | ~ 10 | Низкая температура плавления, сильная сжимаемость, пластичность, ползучесть, вязкая упругость |
| Водородная | H2O, HF | ~ 50 | Склонность к образованию разветвленных многомолекулярных структур |
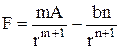 . (3.3)
. (3.3)
На рис. 3.2,а показаны функции En(r), F(r). Имеется в виду, что один атом помещен в начале отсчета, второй можно перемещать вдоль оси r. При этом r0 - положение устойчивого равновесия, в котором находятся атомы при Т=О К. Если вещество нагрето, то второй атом будет колебаться относительно первого, и чем выше температура, тем больше размах колебаний. Если же кинетическая энергия превысит высоту потенциального барьера на DEn, то данный атом может оторваться от первого и произойдет диссоциация. Пунктиром показан график зависимости силы от расстояния между атомами. При r = r0 сила взаимодействия равна нулю. Левая крутая ветвь характеризует силы отталкивания, а правая пологая - силы притяжения. Часто ro принимают за условный диаметр атома, хотя истинное среднее расстояние между центрами атомов, как следует из сказанного, увеличивается с ростом температуры из-за асимметрии потенциальной кривой, что и является причиной теплового расширения.
Когда атомы объединяются в кристалл, то потенциальные кривые накладываются и у расположившихся в цепочку атомов (рис. 3.2,б) результирующая кривая имеет периодический характер. Периодический характер имеет и зависимость силы от координаты, график которой изображен тонкой линией. Исходя из этого, напряжение, вызывающее сдвиг одной части кристалла относительно другой вдоль плоскости параллельной оси Х, так же, как и сила, препятствующая смещению атома А в положение А1, может быть представлено в виде
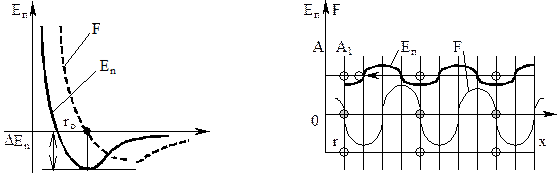
|
| а б |
Р и с. 3.2. Силовые и энергетические характеристики межатомного взаимодействия
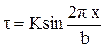 . (3.4)
. (3.4)
С другой стороны, по закону Гука 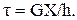 Здесь G - модуль сдвига, b и h - параметры решетки. Поскольку сдвиговые деформации начинаются при Х<< b (в алюминии при Х/b @ 0,002), то
Здесь G - модуль сдвига, b и h - параметры решетки. Поскольку сдвиговые деформации начинаются при Х<< b (в алюминии при Х/b @ 0,002), то 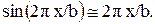
Тогда 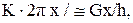 следовательно,
следовательно, 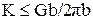 , а сдвиговое напряжение
, а сдвиговое напряжение
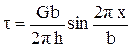 . (3.5)
. (3.5)
Максимального значения сила сопротивления достигает при сдвиге, равном b/4 (рис. 3.2,б), поэтому
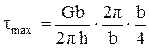 . (3.6)
. (3.6)
Считая h @ b, получаем, чтотеоретическое значение сопротивления сдвигу tmax @ G/4. Это весьма большая величина. В частности, для стали G @ 80 ГПа, следовательно, tmax @ 20 ГПа. В действительности сопротивление сдвигу конструкционной стали, по крайней мере, на 2 порядка ниже.
Причиной столь большого расхождения между теоретической и истинной прочностью являются дефекты кристаллической решетки. Из-за дефектов сдвиг происходит не одновременно по всей атомной плоскости, а скольжение начинается на одном или нескольких участках, а затем распространяется по всей плоскости с конечной скоростью, как это происходит при разрыве бумаги, ткани. Наименьшее сопротивление сдвигу наблюдается при скольжении вдоль наиболее плотно заселенных атомами плоскостей.
Дефекты кристаллов делят на нульмерные (точечные), одномерные и двумерные. К точечным относятся энергетические, электронные и атомные. Наиболее распространены энергетические дефекты - фононы - кванты волн растяжения-сжатия и сдвига (звуковые волны). Тепло в кристалле распространяется также в виде механических волн со звуковой скоростью. В квантовой механике распространение звуковых волн, как и электромагнитных, рассматривается как движение частиц - фононов. Энергия фонона, как и фотона, по формуле Планка равна hv. К электронным дефектам относятся избыточные электроны, дырки, экситоны. Последние представляют собой пару электрон-дырка, связанную кулоновскими силами.
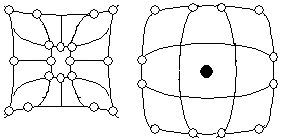
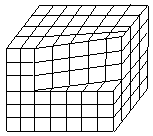
Основные виды атомных дефектов включают вакансии (рис. 3.3,а), атомы в межузлиях (рис. 3.3,б), чужеродные атомы в узлах. Расстояния между атомами в разных направлениях решетки (рис. 3.3,в) различны (АА, АБ, АВ). Поскольку от межатомного расстояния зависят физические свойства кристаллов: прочность, электропроводность, показатель преломления и др., то идеальные кристаллы являются анизотропными средами (в разных направлениях различные свойства).
 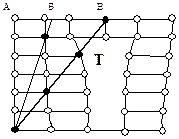 
| |||
| а | б | в | г |
| Р и с. 3.3. Дефекты решетки | |||
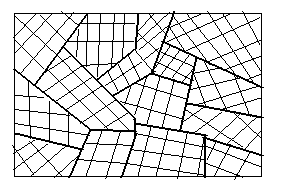
Анизотропия свойств характерна для идеальной кристаллической решетки - монокристалла. Монокристаллы выращиваются при строго контролируемых температуре и давлении из тщательно очищенного от примесей материала. Их прочность близка к идеальной. Если при отливке изделия такие меры не соблюдаются, то кристаллизация начинается одновременно на множествах центров, которыми являются примесные атомы и другие дефекты. В результате возникает множество произвольно ориентированных монокристаллов с размерами порядка десятков микрометров (рис. 3.4). В то время, как каждый кристаллит обладает анизотропией, твердое тело, состоящее из многих тысяч кристаллов, в среднем однородно, практически изотропно и называется поликристаллом. Обычные конструкционные материалы являются поликристаллами.
Одномерные дефекты - дислокации - играют огромную роль в поведении кристаллов при деформации. Простейшая линейная дислокация представляет собой отсутствующий ряд атомов (см. рис. 3.3,в). Более сложной является винтовая дислокация (рис. 3.3,г), которая возникает в результате поворота одной части кристалла относительно другой. Пластическая деформация кристаллов осуществляется при сдвиговых напряжениях, во много раз меньших, чем теоретические, благодаря движению дислокаций, которое начинается при сравнительно небольшой относительной деформации порядка 10-4 - 10-3. Когда дислокация проходит через весь кристалл, одна часть последнего смещается относительно другой на величину межатомного расстояния. Учитывая то, что плотность дислокаций велика (составляет в начале сдвига ~ 106 - 108 см-3), то сдвиг приводит к однородному скольжению множества блоков кристалла относительно друг друга с выходом дислокаций и образованием ступенек на границах тела. Подвижность дислокаций, а следовательно скорость пластической деформации, экспоненциально повышаются с ростом температуры.
На рис. 3.5 показана зависимость прочности от плотности дефектов r. Сначала рост числа дефектов (дислокаций) приводит к падению прочности. После достижения минимума прочность нарастает. В этом случае проявляется взаимодействие дислокаций друг с другом и другими дефектами, приводящее к затормаживанию движения дислокаций. Поэтому существуют два способа упрочнения материалов: снижение числа дефектов, тогда прочность стремится к теоретической (участок 1 на кривой прочности), либо увеличение плотности дефектов (участок 2). Оба пути реализованы в промышленности. В строго контролируемых условиях получают высокопрочные волокна (например из бора), близкие по строению к бездефектным монокристаллам. На основе этих волокон изготавливают металло-композиционные материалы с огромной прочностью на разрыв. Из таких легких и прочных материалов начато изготовление кузовов гоночных автомобилей. Другим примером получения изделий из металлов, содержащих наименьшее число дефектов, является технология изготовления лопаток турбин турбореактивных двигателей. В настоящее время лопатку выращивают как монокристалл в специальных формах при строго контролируемых условиях.
| 
|
| Р и с. 3.4. Схема поликристалла | Р и с. 3.5. Кривая прочности |
Второй путь заключается в насыщении кристалла дефектами за счет закалки, легирования или механического наклепа. Легирование приводит к появлению в решетке инородных атомов. Закалка вызывает измельчение зерен поликристалла, причем границы зерен являются двумерными дефектами. На них рассеиваются дислокации. Деформационное упрочнение - наклеп приводит к образованию огромного количества новых дислокаций, которые препятствуют их взаимному перемещению.
Аморфные вещества, в отличие от кристаллических, имеют ближний порядок в расположении молекул, который становится хаотическим при удалении от данной молекулы на несколько диаметров. У таких веществ отсутствует точка плавления. Они изотропны. Течение, как и у жидкостей, происходит при любой нагрузке и резко интенсифицируется с повышением температуры, поэтому они не обладают пределом текучести. Напряжения и деформации являются функциями нагрузки, времени и температуры. К таким веществам относятся многие полимеры. Макромолекулы полимеров имеют цепь из сотен и тысяч атомов углерода, к которой боковыми связями присоединены группы OH, COOH, NH2, атомы водорода, хлора, фтора. В молекулы могут входить бензольные кольца и другие сочетания атомов. Между макромолекулами действуют силы Ван-дер-Ваальса. В качестве конструкционных материалов используются термопластичные и термореактивные полимеры. К термопластичным относятся полиэтилен, винипласт, капрон, нейлон и др. Они размягчаются под действием температуры. В них, наряду с аморфными, имеются и кристаллические области. Примером практически полностью кристаллического полимера является фторопласт - уникальный химически инертный теплостойкий материал с чрезвычайно низким коэффициентом трения.
Термореактивные полимеры имеют пространственную сетчатую структуру. Макромолекулы соединяются поперечными ковалентными связями. К ним относятся пластмассы на основе фенол-формальдегидных, эпоксидных и других смол. Такие пластики термостойки, сохраняют прочность до температуры 300¸400 0С.
Особую группу составляют эластомеры, обладающие способностью к большим, порядка сотен процентов относительным упругим деформациям (резины, полиуретаны). Большие деформации связаны с особой формой макромолекул, скрученных в клубки и распрямляющихся при растяжении. За счет введения различных наполнителей из полимеров создают композиции, обладающие заданным комплексом физико-механических и химических свойств.
Дата добавления: 2015-07-06; просмотров: 1748;
