Зависимость между сродством химической реакции и константами равновесия
Из выражений (7 - 5) и (7 - 11) следует
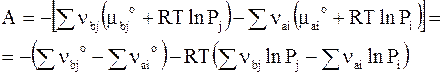
или
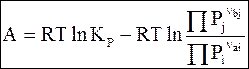 (7 - 24)
(7 - 24)
Уравнение (7 - 24) устанавливает зависимость между константой равновесия и сродством химической реакции для идеальных газов.
Для идеальных и реальных конденсированных систем аналогичные уравнения соответственно имеют следующий вид:
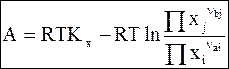 (7 - 25)
(7 - 25)
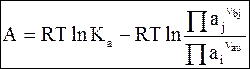 (7 - 26)
(7 - 26)
Уравнения (7 - 24) - (7 - 26) называются уравнениями изотермы химической реакцииили уравнениями максимальной работы химической реакции.
Так как сродство имеет смысл максимальной полезной работы реакции при практически неизменном ее составе, то, зная константу равновесия и действующие парциальные параметры (давления, летучести, молярные доли, активности), можно рассчитать, чему равна максимальная полезная работа при количествах превращаемых или образующихся веществ, равных стехиометрическим коэффициентам.
Отметим, что парциальные величины, входящие в уравнения (7 - 24) - (7 - 26), являются действующими(неравновесными), а величины, входящие в уравнения (7 - 11), (7 - 12), (7 - 13) и др., являются равновесными, т.е. отвечающими только условию равновесия.
Если все вещества, вступающие в реакцию и образующиеся в ходе ее, находятся в стандартном состоянии, то сродство, отвечающее этому условию, называется стандартным сродствоми как все величины, относящиеся к стандартному состоянию, обозначается Ао.
Напомним, что стандартное давление (а для реальных газовых систем стандартная летучесть) равно 1,01325×105 Па и активности или молярные доли в стандартном состоянии (чистого вещества в устойчивой форме) равны 1. Подстановка этих значений в уравнения (7 - 24) - (7 - 26) приводит к следующим уравнениям для стандартного сродства:
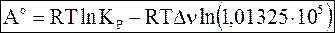 (7 - 27)
(7 - 27)
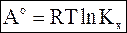 (7 - 28)
(7 - 28)
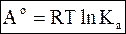 (7 - 29)
(7 - 29)
С понятием стандартного сродства связано понятие стандартного изменения энергии Гиббса DGo, определение которому дается равенством
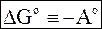 (7 - 30)
(7 - 30)
Из уравнений (7 - 27) - (7 - 29) следует
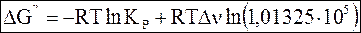 (7 - 31)
(7 - 31)
 (7 - 32)
(7 - 32)
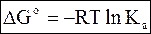 (7 - 33)
(7 - 33)
Дата добавления: 2015-07-24; просмотров: 729;
