УСТОЙЧИВОСТЬ АТОМОВ
Представления об атомах, как о неделимых частицах материи, возникло еще в древности (Демократ, Эпикур, Лукреций). К началу 18 века атомистическая теория строения вещества приобретает все большую популярность, поскольку к тому времени была доказана реальность существования атомов (работы А.Лавуазье, Д.Дальтона, М.Ломоносова), однако в то время не возникало вопроса о внутреннем строении атомов, - они по прежнему считались неделимыми.
К концу 19 века начали накапливаться факты, указывающие на сложную структуру атомов: открытие рентгеновских лучей, радиоактивности, электрона. В 1903 году Э.Резерфорд и Ф.Содди истолковали радиоактивность как превращение химических элементов, а в 1911 году Резерфорд предложил планетарную (ядерную) модель атома. Эта модель была разработана на основе тщательного анализа экспериментальных результатов по рассеянию альфа-частиц тонкими (~ 1 мкм) металлическими пленками. В соответствии с планетарной моделью, в центре атома находится ядро, несущее положительный заряд Z·½e½, (Z - порядковый номер элемента в таблице Менделеева, e - элементарный заряд – заряд электрона). В ядре сосредоточена почти вся масса атома. Вокруг ядра движутся по замкнутым орбитам отрицательно заряженные электроны, образующие электронную оболочку атома. Размер атома
Ra~10-10м, размер ядра Rя~ (10-15 - 10-14м).
Правильность этой модели была доказана экспериментально, однако теоретические следствия из нее, базирующиеся на законах классической физики, оказались в противоречии с действительностью.
Основное противоречие состояло в том, что по законам классической электродинамики ускоренно движущийся вокруг ядра электрон должен непрерывно излучать электромагнитные волны, теряя энергию и, в конце концов, «упасть» на ядро. Кроме того, спектр излучения планетарного атома должен быть непрерывным, поскольку центростремительное ускорение электрона создается кулоновской силой
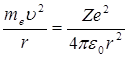 , (2.3)
, (2.3)
где Z- заряд ядра,
me - масса электрона,
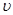 - его скорость,
- его скорость,
r - радиус его орбиты,
То есть, классическая физика не накладывает никаких ограничений на величину скорости 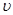 электрона и радиус r его орбиты, а значит и на изменение энергии атома.
электрона и радиус r его орбиты, а значит и на изменение энергии атома.
Таким образом, по классической теории спектр излучения планетарного атома должен быть сплошным, а любой атом неустойчивым, что противоречит действительности, поскольку
1) атом является стабильной системой,
2) атом излучает энергию лишь при определенных условиях,
3) излучение атома имеет линейчатый спектр, связанный со свойствами его электронной оболочки.
Значит, в природе существует какой-то универсальный механизм, незнакомый классической физике, который обеспечивает указанные свойства атомов. Для преодоления возникших противоречий потребовалось создание новой теории.
Дата добавления: 2015-07-24; просмотров: 1553;
