Газовые электроды
Газовые электроды представляют собой разновидность окислительно-восстановительных электродов, на которых протекают реакции с участием газов. Наибольший интерес из этой группы представляют водородный и кислородный электроды.
Водородный электрод. Этот электрод содержит платинированную платину, погруженную в водный раствор и одновременно контактирующую с пузырьками водорода. Платинированная платина (используются другие названия: черненная платина, серая платина) покрыта электролитическим способом мельчайшими частицами платины, имеет высокую удельную поверхность и обладает каталитическими свойствами, что ускоряет наступление равновесия реакции с участием газообразного водорода.
На водородном электроде протекает реакция:
2H+ + 2e = H2.
Условно водородный электрод записывается следующим образом:
H+ôH2, Pt или H+ôH2 (Pt).
Замечательной особенностью водородного электрода является то, что по предложению В.Нернста стандартный водородный электрод был принят в качестве стандартного электрода сравнения. Следовательно, стандартный потенциал водородного электрода равен 0. Напомним, что стандартным условиям отвечают: активность ионоводорода равна 1 и давление водорода, рассматриваемого как идеальный газ, равно 1 атм или 1,01325×105 Па. Следовательно, если давление водорода выражать в атмосферах, то выражение для электродного потенциала принимает следующий вид:
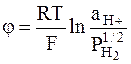 . (2 - 7)
. (2 - 7)
Если же давление выражается в Паскалях, то формула для расчета электродного потенциала может быть записана так:
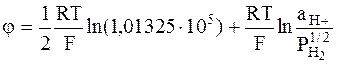 .
.
При постоянном давлении водорода потенциал водородного электрода зависит только от водородного показателя среды:
j = -b×pH.
В связи с этим водородный электрод является главным рН‑ метрическим электродом.
Кислородный электрод. Существуют два варианта рассмотрения кислородного электрода. Первому из них отвечают следующие характеристики:
1/2O2 + H2O + 2e = 2OH-,
OH-ôO2, Pt,
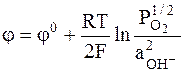 ,
,
j0 = + 0,401 В,
а второй характеризуется следующим:
1/2O2 + 2H+ + 2e = H2O,
H+ôO2, Pt,
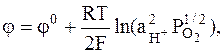
j0 = +1,228 B.
Кроме приведенных реакций на кислородном электроде могут протекать реакции с образованием пероксида водорода и пероксид-ионов. В связи с этим воспроизводимый кислородный электрод реализовать не удается.
Дата добавления: 2015-07-22; просмотров: 1986;
