Злокачественные опухоли
Рак желудка
Актуальность проблемы и распространенность заболевания
В настоящее время заболеваемость раком желудка остается традиционно высокой, хотя в последние годы прослеживается тенденция к снижению показателей заболеваемости. Ежегодно на земном шаре заболевает раком желудка более 1 млн. человек. В России эта патология составляет до 40 больных на 100 тыс. населения, в Японии – 59, Финляндии – 49, США – 7,2. В нашей стране удельный вес рака желудка в структуре всех онкологических заболеваний составляет 12,3 %, а частота смертности – 16,3 %. Наиболее часто его выявляют у лиц в возрасте 45–59 лет, хотя основной пик заболеваемости приходится на возрастную группу 70–74 года. Мужчины болеют почти в 2 раза чаще, чем женщины, причем эта разница увеличивается с возрастом. Максимальный уровень заболеваемости раком желудка в России отмечается на территориях Северного, Северо‑Западного, Центрального и Центрально‑Черноземного районов (Чиссов В. П., Дарьялова С. Л., 2000).
Анатомия и физиология желудка
Большая часть желудка расположена в левом подреберье, а антральный отдел находится в собственно надчревной области. Таким образом, при нормальном расположении желудка пальпации доступен только его антральный отдел.
Желудок граничит с левой и правой долями печени, желчным пузырем справа, селезенкой слева, диафрагмой сверху, поперечной ободочной кишкой снизу и поджелудочной железой сзади.
В желудке различают следующие части: место входа пищевода в желудок называется ostium cardiacum; прилежащая часть желудка – pars cardiaca; место выхода – привратник; его отверстие, ostium pyloricum, прилежащая часть желудка – пилорическая часть; куполообразная часть желудка влево от ostium cardiacum называется сводом. Тело желудка простирается от свода до пилорической части. Pars pylorica разделяется, в свою очередь, на antrum pyloricum – ближайший к телу желудка участок – и canalis pyloricus – более узкую, трубкообразную часть, прилежащую непосредственно к pylorus (рис. 47).
Желудок располагается в эпигастральной области, большая часть желудка (около 5/6) находится влево от срединной плоскости; большая кривизна желудка при его наполнении проецируется в region umbilicalis. Своей длинной осью желудок направлен сверху вниз, слева направо и сзади наперед. Различают малую и большую кривизны желудка. Следует отметить, что желудок полностью покрыт брюшиной, за исключением небольшой полоски по задней поверхности в области дна на уровне желудочно‑поджелудочной связки.
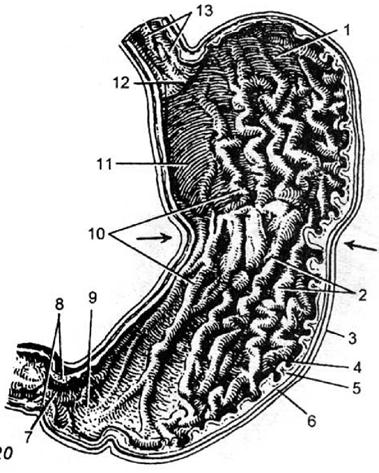
Рис. 47. Желудок (вскрыт). 1 – дно желудка; 2 – складки слизистой оболочки желудка; 3 – большая кривизна; 4 – слизистая оболочка желудка; 5 – подслизистая основа желудка; 6 – мышечная оболочка желудка; 7 – valvula pylorica; 8 – пилорический жом; 9 – пилорическая часть; 11 – кардиальная часть желудка; 12 – ostium cardiacum; 13 – слизистая оболочка пищевода, стрелками показана зона перистальтической волны
Стенка желудка состоит из серозного, мышечного, подслизистого и слизистого слоев. Наиболее выражен мышечный слой в области антрального отдела желудка, где мышечная оболочка в 1,5–2 раза толще, чем в области дна желудка. Это важно при наложении швов на стенку желудка. Необходимо подчеркнуть, что подслизистый слой обладает наибольшей механической прочностью, содержит сосуды, здесь осуществляют их лигирование при наложении на желудок однорядного шва. Слизистая оболочка желудка выстлана однослойным цилиндрическим железистым эпителием, клетки которого выделяют «видимую слизь» – тягучую жидкость желеобразной консистенции. Эта жидкость в виде пленки плотно покрывает всю поверхность слизистой оболочки, защищает ее от механических и химических повреждений, самопереваривания желудочным соком, облегчает прохождение пищи. В 1982 г. введено понятие слизисто‑бикарбонатный барьер. Этот «барьер» препятствует обратной диффузии ионов водорода.
В слизистой оболочке желудка различают три железистые зоны.
1. Зона кардиальных желез, выделяющих слизь.
2. Зона фундальных (главных) желез, содержащих 4 вида клеток: главные (выделяют профермент пепсина – пепсиноген); париетальные, или обкладочные (на их мембране имеются рецепторы для гистамина, ацетилхолина, гастрина; выделяют соляную кислоту, бикарбонат‑ион и внутренний фактор Кастля); добавочные (выделяют растворимую слизь, обладающую буферными свойствами); недифференцированные клетки являются исходными для всех остальных клеток слизистой оболочки.
3. Зона антральных желез, выделяющих растворимую слизь с pH, близким к pH внеклеточной жидкости, и эндокринных G‑клеток, вырабатывающих гормон гастрин.
Угол, под которым пищевод соединяется с желудком, называют углом Гиса. Соответственно этому углу в полости желудка расположена складка слизистой оболочки – клапан Губарева. Этот анатомический механизм наряду с физиологическим обладает антирефлюксными свойствами.
Желудок удерживается в своем положении не только за счет пищевода и пилорического отдела, но и за счет связочного аппарата, которому принадлежит немаловажная роль при операциях на желудке. Основные связки желудка: желудочно‑ободочная связка соединяет желудок с поперечной ободочной кишкой; желудочноселезеночная связка соединяет ворота селезенки с верхними отделами большой кривизны желудка; желудочно‑диафрагмальная и диафрагмально‑пищеводная связки представляют собой дупликатуры брюшины, переходящие с диафрагмы на пищевод и желудок; печеночно‑желудочная связка, или малый сальник, связывает нижнюю поверхность печени с малой кривизной желудка; желудочноподжелудочная связка образуется при переходе брюшины с верхнего края поджелудочной железы на заднюю стенку желудка вблизи его дна. Правый свободный край связки содержит левые желудочные сосуды и лимфатические узлы, собирающие лимфу из бассейна левой желудочной артерии.
Артериальные сосуды желудка происходят из чревного ствола и селезеночной артерии. По малой кривизне располагается анастомоз между левой желудочной артерией (из чревного ствола) и правой желудочной артерией (из общей печеночной артерии), по большой – левая желудочно‑сальниковая артерия (из селезеночной артерии) соединяется с правой желудочно‑сальниковой артерией (из желудочно‑дуоденальной артерии). Важно отметить, что левая желудочная артерия является единственной, которая при перевязке всех остальных желудочных сосудов может обеспечить полноценное кровоснабжение желудка. Ко дну желудка подходят короткие артерии желудка (3–6) из селезеночной артерии. Вены, соответствующие по ходу артериям, впадают в воротную вену.
Кровоснабжение желудка и двенадцатиперстной кишки представлено на рисунке 48.
Лимфатическая система желудка (рис. 49, 50) представлена капиллярами и сосудами, расположенными во всех слоях его стенки. Особенно густая сеть капилляров и сосудов имеется в подслизистом и подсерозном слоях.
Сосуды, отводящие лимфу от желудка, тянутся по ходу питающих артерий. Так, от 2/3 дна и тела желудка они идут вместе с левыми желудочными кровеносными сосудами, от латеральной левой части дна и большой кривизны – по ходу левых желудочно‑сальниковых и коротких желудочных сосудов. От правой половины большой кривизны желудка лимфа оттекает по лимфатическим сосудам, сопровождающим правые желудочно‑сальниковые сосуды. От пилорической части лимфа оттекает по лимфатическим путям, сопровождающим желудочно‑двенадцатиперстные кровеносные сосуды. От малой кривизны, прилежащих участков кардии и тела желудка лимфатические сосуды идут по ходу левых желудочных артерий.
Нервы желудка – это ветви n. vagus и truncus sympathicus. Они образуют желудочное сплетение. Правый блуждающий нерв разветвляется в передней стенке желудка, а левый – в задней. Симпатические нервы отходят от чревного сплетения и идут по ходу артерий желудка.
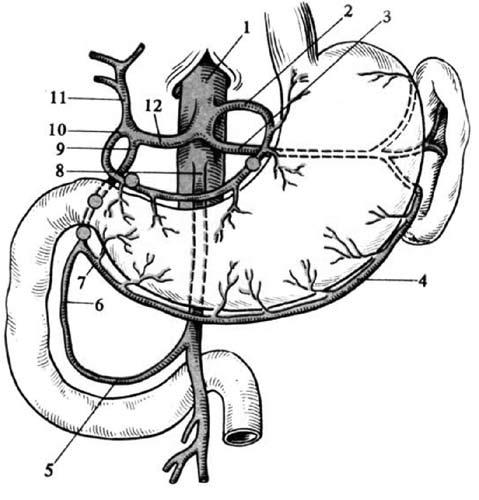
Рис. 48. Артериальное кровоснабжение желудка и двенадцатиперстной кишки. I – чревный ствол, 2 – левая желудочная артерия, 3 – селезеночная артерия, 4 – левая желудочно‑сальниковая артерия, 5 – нижняя передняя панкреатодуоденальная артерия, 6 – верхняя передняя панкреатодуоденальная артерия, 7 – правая желудочно‑сальниковая артерия, 8 – верхняя брыжеечная артерия, 9 – желудочно‑дуоденальная артерия, 10 – правая желудочная артерия, II – собственная печеночная артерия, 12 –общая печеночная артерия.
Этиология и патогенез
К этиологическим факторам, вызывающим рак желудка, относят многообразную группу веществ, физических или химических соединений, называемую канцерогенами, среди которых выделяют канцерогены экзогенные и эндогенные. Установлено, что абсолютных канцерогенов не существует.
Известно, что в регионах с кислой, богатой органическими веществами почвой, отмечается увеличение показателей заболеваемости. К этиологическим факторам, оказывающим воздействие на возникновение рака желудка в промышленной сфере, относят производство резины, асбеста, винилхлорида, минеральных масел, хрома и т. д.
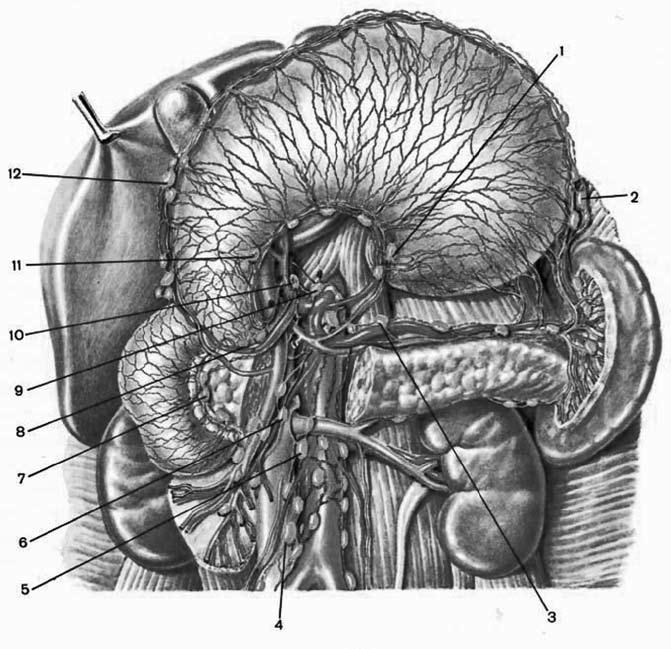
Рис. 49. Лимфатическая система желудка. 1 – чревные лимфатические узлы; 2 – печеночные лимфатические узлы; 3 – кардиальные лимфатические узлы; 4 – желудочные лимфатические узлы (правые); 5 – желудочные лимфатические узлы (левые); 6 – пилорические лимфатические узлы; 7 – панкреатодуоденальные лимфатические узлы; 8 – желудочно‑сальниковые лимфатические узлы (левые); 9 – желудочно‑сальниковые лимфатические узлы (правые)
Окончательно не изучено влияние ионизирующего излучения на развитие рака желудка, однако высокий уровень радиационного фона и содержание радионуклидов в пище и воде считаются факторами риска. Поскольку слизистая оболочка желудка постоянно подвергается контакту с пищей, значительное место в гипотезе об этиологии рака желудка отводят алиментарному фактору, злоупотреблению алкоголем и курению.
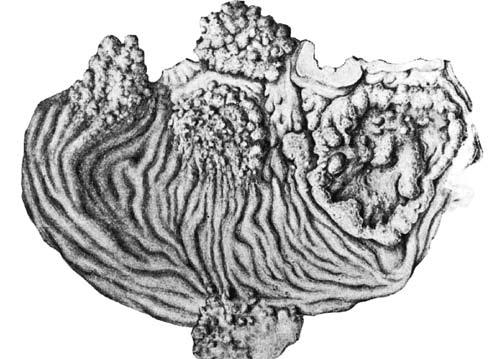
Рис. 50. Лимфатическая система желудка (желудок оттянут кверху). 1 – желудочные лимфатические узлы (левые), 2 – желудочно‑сальниковые узлы (левые), 3 – верхние панкреатические лимфатические узлы, 4 – поясничные лимфатические узлы, 5 – нижние брыжеечные лимфатические узлы, 6 – верхние брыжеечные лимфатические узлы, 7 – панкреатодуоденальные лимфатические узлы, 8 – пилорические лимфатические узлы, 9 – чревные лимфатические узлы, 10 – печеночные лимфатические узлы, 11 –желудочные лимфатические узлы (правые), 12 – желудочно‑сальниковые правые лимфатические узлы
Совершенно очевидно, что на величину показателя заболеваемости населения раком желудка оказывает влияние характер и режим питания. Наличие в рационе питания достаточного количества растительной пищи и фруктов, микроэлементов и витаминов, в частности витаминов А, Е и С, животных и растительных белков существенно снижает риск возникновения рака желудка. Наиболее наглядный в этом пример США, где за последние 70 лет пропаганды рационального питания многократно снизилась заболеваемость населения раком желудка. В последние годы особое значение в канцерогенезе отводят некоторым химическим веществам. Наиболее активными из них являются N‑нитрозосоединения. Экспериментально доказано, что добавление в пищу нитрозосоединений в 90 % наблюдений вызывает у лабораторных мышей развитие рака желудка. Синтез в желудке человека канцерогенных соединений, поступающих с пищей и водой, может происходить как в кислой, так и в слабокислой и нейтральной среде.
В настоящее время все больше внимания уделяют влиянию Helicobacter pylori (HP) на возникновение рака желудка. Это обусловлено сообщениями отечественных и зарубежных исследователей, которые отмечают увеличение уровня заболеваемости у лиц, инфицированных данным микроорганизмом.
После того, как в 1983 г. Marshall, исследуя биоптаты слизистой оболочки желудка больных язвенной болезнью, обнаружил и описал микроорганизм, классифицированный как Helicobacter pylori , впоследствии признанный ведущим в этиологии хронического неиммунного антрального гастрита, исследователей заинтересовали его связи в возникновении рака желудка.
В США и Англии исследования показали, что риск возникновения рака желудка у инфицированных пациентов в 3,8 раза выше по сравнению с неинфицированными больными (Фишелева Е. Л., 1996). По классификации ВОЗ HP относится к группе I (явные канцерогены).
На основании изучения разнообразных эпидемиологических данных P. Correa (1975) была сформулирована патогенетическая модель рака желудка. Суть ее состоит в том, что в течение значительного промежутка времени избыточное потребление соли и других раздражающих слизистую оболочку пищевых факторов приводит к разрушению защитного слизистого барьера, острому воспалению, некрозу, повторяющейся регенерации слизистой оболочки. Этому же может способствовать рефлюкс дуоденального содержимого в желудок. Также следует отметить роль аутоиммунных процессов с повреждением главных и обкладочных клеток. Повторяющиеся воздействия этих факторов наряду с поступлением и синтезом нитрозосоединений приводят к формированию хронического гастрита с неравномерной атрофией специализированных желез. В подавляющем большинстве случаев эти изменения не сопровождаются клиническим проявлением заболевания. Помимо атрофических изменений желез появляется кишечная метаплазия, которую можно рассматривать как неспецифическую приспособительную или регенераторную реакцию эпителия. Появление этих изменений может приводить к снижению желудочной секреции: сначала кислотопродукции, затем пепсина. Недостаточное поступление веществ, снижающих эффективность реакции нитрозирования аминосоединений, особенно витаминов А, С и Е, а также иммунодепрессия в этих условиях обеспечивает канцерогенное воздействие нитрозосоединений, появление и постепенное нарастание атипических реакций с переходом в преинвазивный и далее инвазивный рак.
Совещание экспертов ВОЗ признало, что с морфологической точки зрения предрак существует, причем следует различать предраковые состояния и предраковые изменения.
Предраковое (или фоновое) состояние – понятие клиническое и характеризуется теми заболеваниями желудка, которые наиболее часто предшествуют развитию рака. Предраковые изменения – это сумма морфологических признаков, называемых дисплазией, предшествующих и сопутствующих раку.
Дисплазия – понятие, которое включает в себя клеточную атипию, нарушение дифференциации и структуры слизистой оболочки. В большинстве случаев слабая и умеренная дисплазия подвергается обратному развитию или остается стабильной, хотя несомненна возможность ее трансформации в рак. Тяжелая степень дисплазии также способна подвергаться обратному развитию, однако вероятность ее озлокачествления достаточно велика и может достигать 75 % (Чиссов В. И., 2000).
Считается, что только у 60 % больных начальным раком желудка в анамнезе имеется указание на хронические заболевания: ведущими среди них являются хронический гастрит – 76,7 %, у 12,4 % больных ранее была диагностирована язвенная болезнь 12‑перстной кишки, у 7 % – язвенная болезнь желудка, у 0,8 % – полипы, у 3,1 % – оперированный желудок (Чиссов В. И., Вашакмадзе Л. А., 2000).
Морфологическое исследование установило, что основным предраковым заболеванием при начальном раке желудка является хронический гастрит (около 90 %), в том числе и в оперированном желудке. Менее значимы аденомы (до 8‑10 %), гиперпластические полипы (около 3 %), язва желудка (до 1–2%).
К ранней онкологической патологии желудка Б. Е. Петерсон и со‑авт. (1985) относят предраковые изменения слизистой оболочки, рак in situ и инвазивный рак (опухоль диаметром до 1 см, которая не прорастает в подслизистый слой).
Специалисты Японского общества гастроэнтерологов‑эндоскопистов (1962) под термином «ранний» предлагают определять рак, расположенный в границах слизистой оболочки желудка без проникновения в мышечный слой, независимо от наличия или отсутствия метастазов в лимфатические узлы. При этом принципиально важным является четкое разграничение понятий «карцинома in situ» (поражение эпителия слизистой), опухолевое поражение слизистой оболочки и под слизистого слоя.
По данным японских авторов, при расположении рака желудка в границах слизистой оболочки выживаемость больных после радикальной операции достигает 100 %; при прорастании опухоли в подслизистый слой этот показатель снижается до 75 %; при инвазии рака в мышечную и серозную оболочки желудка выживаемость составляет не более 25 %.
Сочетание предраковых состояний с предраковыми изменениями повышает риск развития рака желудка.
К предраковым заболеваниям, на основе которых может развиться рак желудка, относят: хронический атрофический и гипертрофический гастрит, ригидный антральный гастрит, язвенную болезнь желудка, полипы и полипоз желудка, болезнь Менетрие (складчатый гастрит), пернициозную анемию, атрофический гастрит культи желудка.
Следует отметить, что рак желудка, который развивается на фоне хронического атрофического гастрита, всегда сопровождается гипохлоргидрией или ахлоргидрией. Больные хроническим гастритом должны находиться под постоянным врачебным наблюдением и проходить не менее 2 раз в год профилактические осмотры с целью возможного выявления ранних форм рака желудка.
Малигнизация язвы желудка, по данным большинства авторов, колеблется от 1 до 17 % случаев. Как предраковую рассматривают чаще каллезную язву, хотя правильнее расценивать каждую язву желудка (любых размеров) как потенциально злокачественную.
Большинство исследователей рекомендуют в качестве дифференциально‑диагностического приема проводить курс терапии на протяжении 4–6 недель. Если язва желудка на протяжении указанного срока не рубцуется, необходимо предлагать пациентам операцию. Вместе с тем необходимо помнить, что и небольшие раковые язвы могут временно эпителизироваться под действием противоязвенных препаратов.
Менее значимы в структуре начального рака желудка малигнизированные полипы, при этом потенциал малигнизации у различных типов полипов неодинаков: аденомы (аденоматозные) озлокачествляются в 36 %, а гиперпластические полипы – в 3,5 % случаев.
У больных пернициозной анемией (обусловленной недостаточностью в организме витамина В12) постоянно наблюдается хронический атрофический гастрит. Во многих случаях он протекает с кишечной метаплазией эпителия желудка. Рак желудка при пернициозной анемии встречается в 3–5 раз чаще, чем у здоровых людей (Бондарь Г. В. и соавт., 2003).
Болезнь Менетрие – своеобразное и редкое заболевание желудка, которое характеризуется гиперплазией эпителия и резким утолщением складок слизистой оболочки. Клиническая картина при этом характеризуется болями в эпигастральной области, похудением и тошнотой. Заболевание имеет хроническое течение. Иногда наблюдается спонтанное выздоровление или переход в хронический атрофический гастрит. Рак возникает примерно у 10 % заболевших.
Хронический гастрит культи желудка нередко сопровождается дисплазией и кишечной метаплазией эпителия. Патологические изменения с течением времени прогрессируют, частота их возрастает. Создаются условия для возникновения рака культи желудка.
Рак культи желудка возникает у 2–6 % из числа оперированных по поводу доброкачественных заболеваний желудка. Мужчины болеют в 4–5 раз чаще женщин. Заболеваемость раком культи резецированного желудка в последние годы возрастает. Опухоль чаще возникает через 10–20 лет после операции. Риск повышается у людей, которым резекция желудка выполнена в молодом возрасте. То, что ранее именовалось термином «поздние рецидивы рака оперированного желудка», по мнению Я. Д. Витебского (1991), есть новая опухоль, которая возникла вследствие рефлюкса желчи в культю желудка.
Больные, которые перенесли резекцию желудка 10 и более лет тому назад, должны ежегодно проходить осмотр врача с обязательным эндоскопическим или рентгенологическим обследованием.
Классификация
В зависимости от локализации выделяют рак кардиального отдела, рак тела (малая и большая кривизны, передняя и задняя стенки) и рак антрального отдела желудка. Чаще всего рак поражает антральный отдел желудка (60 % наблюдений). На малой кривизне карцинома развивается у 20–25 % больных, на передней и задней стенках – в 2–5% наблюдений, в проксимальных отделах – у 10–15 %, тотальное поражение регистрируют у 5 % пациентов, а большая кривизна желудка поражается у 1–3 % больных.
Макроскопически различают три типа роста рака желудка (экзофитный, эндофитный и смешанный). С ними можно связать особенности клинической симптоматики заболевания и характер метастазирования. Экзофитный (полиповидный, грибовидный, блюдцеобразный, бляшковидный) рост опухоли характеризуется четкими границами (рис. 51).
При экзофитном раке новообразование имеет вид полипа, бляшки или гриба. При изъязвлении такой опухоли ее центр принимает вид блюдца. На расстояние более 2–3 см от видимого края опухоли раковая инфильтрация обычно не распространяется. Наиболее злокачественно протекает рак желудка, отличающийся эндофитным (инфильтративным) типом роста.
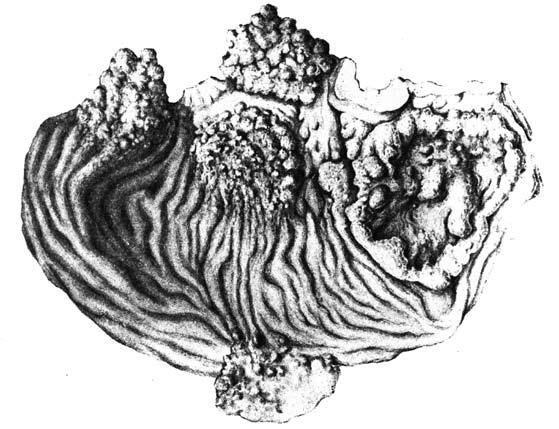
Рис. 51. Множественный рак желудка. Препарат рассечен по большой кривизне после его экстирпации. Слева видны три полипозных рака желудка (в виде куста), справа– блюдцеобразный рак средней трети. Между двумя полипообразными опухолями виден участок пищевода
Эти опухоли не вдаются в просвет органа и не имеют четких границ. Инфильтративные карциномы распространяются вдоль стенки желудка, главным образом по подслизистому слою, богатому лимфатическими сосудами, и чаще метастазируют. Складки слизистой оболочки желудка при этом расправляются, сглаживаются. При микроскопическом исследовании удаленного препарата клетки рака можно обнаружить на расстоянии 5–7 см от предполагаемой границы опухоли. При смешанном типе сочетаются признаки экзо– и эндофитного роста. В этих случаях течение заболевания определяет инфильтративный компонент опухоли. Международная гистологическая классификация, принятая ВОЗ в 1977 году, подразделяет рак желудка на:
1. Аденокарциному: а) папиллярную, б) тубулярную, в) муцинозную, г) перстневидноклеточную.
2. Железисто‑плоскоклеточный рак.
3. Плоскоклеточный рак.
4. Недифференцированный рак.
5. Неклассифицируемый рак.
По степени дифференцировки опухолевых клеток международная классификация предусматривает высоко‑, умеренно‑и низкодифференцированные виды аденокарцином. Следует отметить, что в пределах одной опухоли могут обнаруживаться участки различного строения и разной степени дифференцировки. Это объясняется сложностью строения слизистой оболочки желудка, способностью ее камбиальных клеток дифференцироваться в морфологически и функционально различные клеточные элементы.
Кроме традиционной классификации ВОЗ, широкое распространение при эпидемиологических исследованиях получила классификация К. Lauren (1965), которая делит карциномы желудка на опухоли с кишечным и диффузным типами строения. Рак желудка кишечного типа часто возникает на фоне кишечной метаплазии слизистой оболочки желудка и в большинстве случаев характеризуется экзофитной формой роста. Диффузный тип рака чаще встречается при низкодифференцированных аденокарциномах, перстневидноклеточном и анапластическом раках и характеризуется распространенной диффузной инфильтрацией желудочной стенки.
Эндоскопическая классификация ранних форм рака желудка (по данным Японского общества эндоскопистов) выделяет три типа раннего рака: I – выбухающий; II – поверхностный; III – язвенный.
Выбухающий тип: опухоль выступает над окружающей поверхностью слизистой оболочки более чем на 5 мм; поверхностный тип подразделяют на 3 формы: а) приподнятый: опухоль выступает до
5 мм над окружающей поверхностью слизистой оболочки; б) плоский: опухоль в виде эрозии находится на уровне окружающей поверхности слизистой оболочки; в) вогнутый: опухоль углубляется в виде язвы ниже уровня слизистой оболочки до 5 мм; подрытый, язвенный тип характеризуется углублением более чем на 5 мм.
Для характеристики типа роста опухоли широко применяют классификацию по Борману (Borrmann, предложенную еще в 1926 году), которая позволяет прогнозировать течение процесса и планировать адекватный объем хирургического вмешательства. По этой классификации различают 4 типа роста опухоли (рис. 59).
I. Полипозный – хорошо отграниченный с относительно благоприятным прогнозом, встречается в 5 % случаев.
II. Язвенный – с блюдцеобразно приподнятыми краями и менее экспансивным ростом, составляет 35 % всех заболеваний раком желудка.
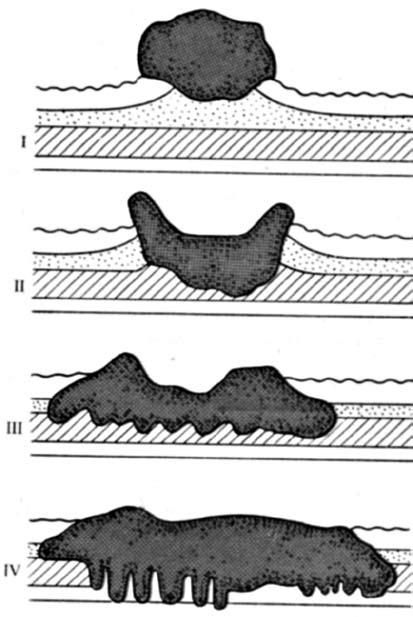
Рис. 59. Макроскопические формы роста рака желудка (по Борману). I – полипозный тип;
II – язвенный тип;
III – инфильтративно‑язвенный тип;
IV – диффузно‑инфильтративный тип (скиррозный).
III.Инфильтративно‑язвенный – с прорастанием глубоких слоев стенки без четкого отграничения от здоровых тканей и ранним метастазированием, частота 50 %. Прогноз неблагоприятный. IV. Скиррозная диффузно‑инфильтративная опухоль, которая часто оставляет интактным поверхностный слой слизистой оболочки (растет в подслизистой основе), поэтому ее трудно распознать при гастроскопии, составляет 10 % случаев рака желудка; прогноз неблагоприятный.
Рак желудка метастазирует преимущественно лимфогенным путем. Возможны также гематогенный, контактный или имплантационный пути распространения опухоли. Чаще отмечается следующая последовательность метастазирования: сначала поражаются регионарные лимфатические барьеры (лимфатические узлы, расположенные в связках желудка), затем лимфатические узлы (л/у), сопровождающие крупные артерии, питающие желудок, потом забрюшинные и органы брюшной полости. Пути распространения рака желудка представлены на рисунке 60.
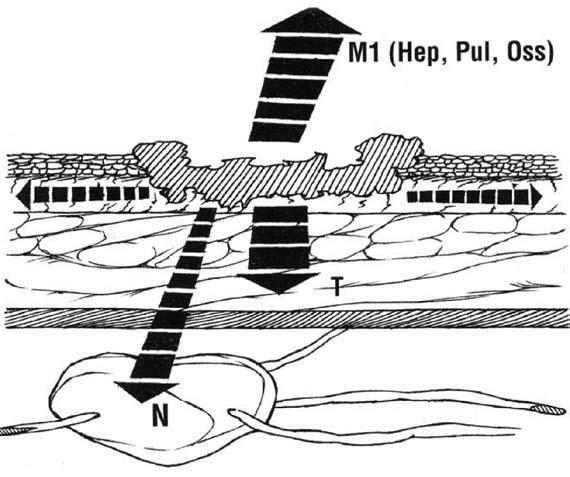
Рис. 60. Пути распространения рака желудка
В настоящее время, на основании работ Японского общества по изучению рака желудка (1998) детально описаны 20 групп регионарных лимфатических узлов, формирующих три последовательные (не в истинном понимании последовательности) этапа метастазирования от различных отделов желудка – N1 до N3: (рис. 61). Первый этап: перигастральные лимфоколлекторы, расположенные в связочном аппарате желудка (№ 1–6);
Второй этап: забрюшинные лимфатические узлы, расположенные по ходу ветвей чревного ствола (лимфатические узлы по ходу левой желудочной артерии (№ 7), общей печеночной артерии (№ 8а+р), чревного ствола (№ 9), в воротах селезенки (№ 10), по ходу селезеночной артерии (№ 11 p + d)).
Третий этап: лимфатические узлы гепатодуоденальной связки (№ 12а+р+Ь), ретропанкреатодуоденальные (№ 13), лимфатические узлы по ходу верхней брыжеечной артерии (№ 14a+v), в корне брыжейки поперечной ободочной кишки по ходу средней ободочной артерии (№ 15), парааортальные лимфатические узлы, расположенные на различном уровне брюшной аорты (№ 16 а1‑а2, Ь1‑Ь2).
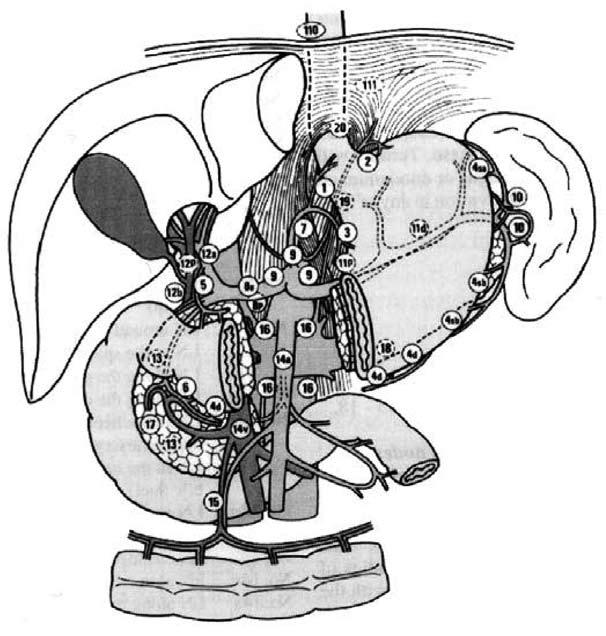
Рис. 61 . Схема регионарных лимфатических узлов желудка (JGCA, 1998)
На основании этой классификации и показателей выживаемости, вовлечение лимфатических коллекторов N1 – N2 рассматривают как регионарное метастазирование, тогда как вовлечение лимфатических узлов N3 – как отдаленное метастазирование. Карцинома желудка имеет склонность в большей степени распространяться вверх по желудочной стенке соответственно преимущественному току лимфы в сторону малой кривизны желудка и желудочно‑поджелудочной связки, где расположен главный коллектор лимфооттока от желудка.
Гематогенно наиболее часто рак желудка метастазирует в печень. Реже метастазы обнаруживают в легких, надпочечниках, костях.
Для рака желудка характерными отдаленными метастазами считаются: метастаз Вирхова, или вирховская железа (в лимфатических узлах левой надключичной области), метастаз сестры Мэри Джозеф (ретроградные метастазы, распространяющиеся по лимфатическим сосудам круглой связки печени, в пупке), Шницлера (в пространство Дугласа, или параректальной клетчатке тазового дна), метастаз Крукенберга (в яичниках).
Следует сделать ремарку, что на сегодняшний день метастазы Крукенберга рассматриваются не как гематогенные или имплантационные, а как лимфогенные метастазы, косвенно свидетельствующие о широком поражении парааортального лимфатического коллектора. Этим также обусловлено обязательное двустороннее поражение яичников. Учитывая такой механизм поражения, метастазы Крукенберга не рассматриваются как противопоказание к хирургическому лечению.
Дата добавления: 2015-08-26; просмотров: 1597;
