Кинетика восстановления оксидов в доменной печи
Протекание реакций восстановления в доменной печи определяется не только термодинамическими закономерностями, но и закономерностями кинетики. Скорости реакций восстановления оксидов железа газообразными восстановителями оказывают существенное влияние на показатели работы доменной печи. Чтобы говорить о скорости реакций, необходимо знать механизм протекания этих реакций.
В настоящее время общепринятой теорией восстановления является адсорбционно-автокаталитическая теория, предложенная Г.И. Чуфаровым. По этой теории соединение восстановителя с кислородом происходит не в газовой фазе, а на поверхности или внутри, в порах куска твердого вещества, т.е. на границе фаз оксид-газ.
Согласно этой теории, собственно химический акт реакции восстановления металлов газами состоит из трех последовательных стадий:
1. адсорбция газа-восстановителя на поверхности восстанавливаемого твердого оксида (реакционной поверхности);
2. отрыв кислорода от решетки оксида и соединение его с адсорбированными молекулами газа-восстановителя, в результате чего происходит образование оксида восстановителя и перестройка кристаллической решетки оксид металла в кристаллическую решетку металла. В результате чего образуется новая твердая фаза;
3. десорбция газообразных продуктов восстановления в газовую фазу.
Длительность восстановительного процесса определяется протеканием самого медленного звена, которым обычноявляется вторая стадия, связанная с перестройкой кристаллической решетки.
Автокаталитический характер процесса восстановления проявляется в том, что скорость реакции в кинетической области (вторая стадия) изменяется во времени. С ростом числа зародышей новой фазы и увеличением реакционной поверхности скорость реакции резко возрастает. При этом химическая реакция ускоряется под действием катализатора - свежевосстановленного железа, а иногда и оксидов железа. При сливании отдельных поверхностей раздела фаз в одну фазу, которая по ходу процесса уменьшается в размерах, происходит постепенное убывание скорости реакции.
Скорость реакции восстановления зависит не только от скорости кристаллохимического превращения на реакционной поверхности (оксида), но и от подвода за счет диффузии газа-восстановителя к реакционной зоне и отвода продуктов реакции в газовую среду. В куске или слое рудного материала образующийся наружный слой восстановленного металла или низшего оксида оказывает существенное влияние на скорость диффузии. Чем больше толщина этого слоя, тем в большей степени затруднена диффузия.
Температура по-разному влияет на константу скорости химической реакции и на коэффициент диффузии. Согласно уравнению Аррениуса, константа скорости химической реакции зависит от температуры экспоненциально:
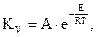 (2.1‑14)
(2.1‑14)
а коэффициент диффузии зависит от температуры следующим образом:
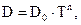 (2.1‑15)
(2.1‑15)
где Е - энергия активации (величина, определяющая минимальный запас энергии в частицах, необходимый для начала реакции); е - основание натурального логарифма; R - газовая постоянная; T – температура; n - постоянная величина, равная 1,5 - 2,0; A - предэкспоненциальный множитель; D0 - постоянная.
С повышением температуры константа скорости реакции KV возрастает в большей степени, чем коэффициент диффузии, т.е. лимитирующим процессом становится диффузия. Следовательно, иногда процесс, находящийся в кинетической области при низких температурах, при возрастании температуры может перейти в диффузионную область (рис. 9).
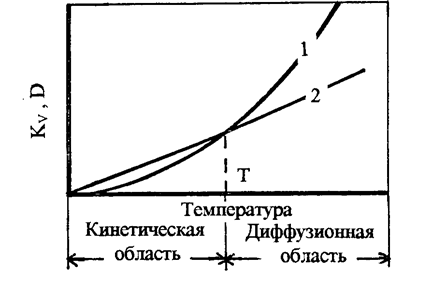
Рис. 9. Изменение константы скорости реакции КV – (1) и коэффициента диффузии D – (2) от температуры.
Диффузия может быть внутренняя и внешняя. При внутренней диффузии имеет место движение ионов или восстановительного газа и газообразных продуктов реакции восстановления через слой исходного или восстановленного твердого вещества, зависящее от свойств твердых веществ (исходных оксидов или продуктов реакции).
Скорость этого этапа восстановительного процесса зависит от соотношения между диаметром мельчайших каналов, образуемых порами исходного материала и восстановленного вещества и длиной свободного пробега молекул, а также от физического взаимодействия между молекулами газа и поверхностями пор и каналов.
В кинетической области в связи с низкой скоростью реакции процесс протекает по всей массе внутри слоя или куска рудного материала. При увеличении размеров кусков рудного материала и уменьшении скорости газового потока затрудняются процессы подвода газа-восстановителя к реакционной поверхности и отвод от нее продуктов реакции. Процесс восстановления переходит в диффузионную область, где скорость реакции в сравнении с коэффициентом диффузии возрастает настолько, что процесс протекает по мере подвода газа-восстановителя и отвода продуктов реакции, т.е. фронтально.
В реальных условиях доменной печи до температур 900-1000 оС процесс лимитируется кинетическим звеном. Выше указанных температур лимитирующим звеном становится диффузия ионов в кристаллической решетке, затрудняемая непрерывно утолщающимся слоем восстановленного железа и начинающимся спеканием, которое снижает пористость рудного материала. При этом, чем больше диаметр восстанавливаемого куска, тем в большей степени процессы внутренней диффузии лимитируют скорость восстановления. Поэтому размеры кусков рудного материала и его восстановимость должны быть оптимальными.
Дата добавления: 2015-06-22; просмотров: 2118;
