Теплоемкость. Удельная теплоемкость вещества – величина, равная количеству теплоты, необходимому для нагревания 1 кг вещества на 1 К:
Удельная теплоемкость вещества – величина, равная количеству теплоты, необходимому для нагревания 1 кг вещества на 1 К:
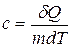 (7.9)
(7.9)
Единица удельной теплоемкости — джоуль деленный на килограмм-кельвин (Дж/(кг×К)).
Молярная теплоемкость – величина, равная количеству теплоты, необходимому для нагревания 1 моль вещества на 1 К:
Cm=  ,(7.10)
,(7.10)
где: v=m/M – количество вещества.
Единица молярной теплоемкости — джоуль деленный на моль·кельвин (Дж/(моль·К)). Удельная теплоемкость с связана с молярной Сm соотношением
Сm = сМ (7.11)
Различают молярные теплоемкости при постоянном объеме СV и постоянном давлении Ср, если в процессе нагревания вещества его объем или давление поддерживается постоянным.
Запишем выражение первого начала термодинамики (7.6) для 1 моля газа
CmdT = dUm + pdVm.(7.12)
Молярная теплоемкость газа при постоянном объеме СV равна изменению внутренней энергии 1 моль газа при повышении его температуры на 1 К
CV =iR/2 (7.13)
Молярная теплоемкость при постоянном давлении:
Сp = СV+R (7.14)
Выражение (7.14) называется уравнением Майера; оно показывает, что Ср всегда больше СV на величину молярной газовой постоянной. Это объясняется тем, что при нагревании газа требуется еще дополнительное количество теплоты на совершение работы расширения газа, так как постоянство давления обеспечивается увеличением объема газа.
Сp= 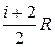 (7.15)
(7.15)
При рассмотрении термодинамических процессов важно знать характерное для каждого газа отношение Ср к СV:
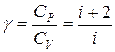 (7.16)
(7.16)
Из формул следует, что молярные теплоемкости определяются лишь числом степеней свободы и не зависят от температуры.
Дата добавления: 2015-06-17; просмотров: 1118;
