Основное уравнение молекулярно-кинетической теории идеальных газов
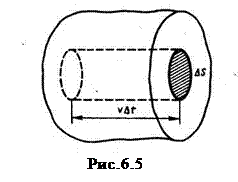 Рассмотрим одноатомный идеальный газ. Предположим, что молекулы газа движутся хаотически, число взаимных столкновений между молекулами газа мало по сравнению с числом ударов о стенки сосуда, а соударения молекул со стенками сосуда абсолютно упругие. Выделим на стенке сосуда некоторую элементарную площадку ΔS и вычислим давление на эту площадку. При каждом соударении молекула, движущаяся перпендикулярно площадке, передает ей импульс m0υ -(- m0υ) = 2m0υ, где: т0– масса молекулы, υ – ее скорость.
Рассмотрим одноатомный идеальный газ. Предположим, что молекулы газа движутся хаотически, число взаимных столкновений между молекулами газа мало по сравнению с числом ударов о стенки сосуда, а соударения молекул со стенками сосуда абсолютно упругие. Выделим на стенке сосуда некоторую элементарную площадку ΔS и вычислим давление на эту площадку. При каждом соударении молекула, движущаяся перпендикулярно площадке, передает ей импульс m0υ -(- m0υ) = 2m0υ, где: т0– масса молекулы, υ – ее скорость.
За время Δt площадки ΔS достигнут только те молекулы, которые заключены в объеме цилиндра с основанием ΔS и высотой υΔt. Число этих молекул равно nΔSυΔt (n - концентрация молекул).
Для упрощения расчетов хаотическое движение молекул заменяют движением вдоль трех взаимно перпендикулярных направлений, так что в любой момент времени вдоль каждого из них движется 1/3 молекул, причем половина молекул, т.е. 1/6 часть, движется вдоль данного направления в одну сторону, половина — в противоположную. Тогда число ударов молекул, движущихся в заданном направлении, о площадку ΔS будет 1/6 nΔSυΔt. При столкновении с площадкой эти молекулы передадут ей импульс
ΔP=2m0υ∙ 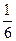 nΔSυΔt =
nΔSυΔt = 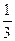 nm0υ2 ΔSΔt
nm0υ2 ΔSΔt
Тогда давление газа, оказываемое им на стенку сосуда,
p=ΔΡ/(ΔSΔt)= 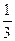 nm0υ2 (6.7)
nm0υ2 (6.7)
Если газ в объеме V содержит N молекул, движущихся со скоростями υ1, υ2,..., υN, то целесообразно рассматривать среднеквадратную скорость
υcк= 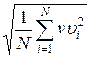 (6.8)
(6.8)
характеризующую всю совокупность молекул газа. Уравнение (6.7) с учетом (6.8) примет вид
p= 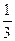 nm0υcк2 (6.9)
nm0υcк2 (6.9)
Выражение (6.9) называется основным уравнением молекулярно-кинетической теории идеальных газов.
Учитывая, что n=N/V,получим
pV= 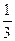 Nm0υcк2,
Nm0υcк2,
или
pV= 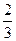 N
N 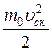 =
= 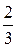 W, (6.10)
W, (6.10)
где W – суммарная кинетическая энергия поступательного движения всех молекул газа.
Так как масса газа m=Nm0, то уравнение (6.9) можно переписать в виде
pV= 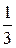 mυcк2.
mυcк2.
Для одного моля газа т=М (М — молярная масса), поэтому
pVm= 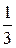 Mυcк2,
Mυcк2,
где Vm – молярный объем. С другой стороны, по уравнению Клапейрона - Менделеева, pVm=RT. Таким образом,
RT = 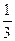 Mυcк2
Mυcк2
Откуда υcк = 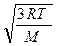 . (6.11)
. (6.11)
Так как М= NА m0, где m0 – масса одной молекулы, а NА – постоянная Авогадро, то из уравнения (6.11) следует, что
υcк= 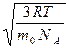 =
= 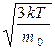 , (6.12)
, (6.12)
где: k=R/NA – постоянная Больцмана. Отсюда найдем, что при комнатной температуре молекулы кислорода имеют υcк =480 м/с, водорода – 1900 м/с. При температуре жидкого гелия те же скорости будут соответственно 40 и 160 м/с.
Средняя кинетическая энергия поступательного движения одной молекулы идеального газа
<w0> = 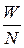 =
= 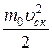 =
= 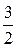 kТ (6.13)
kТ (6.13)
пропорциональна термодинамической температуре и зависит только от нее.
Дата добавления: 2015-06-17; просмотров: 1099;
