Способы изменения скорости простых и сложных реакций
Как указывалось, скорость химической реакции зависит от большого числа различных факторов. Из кинетических уравнений следует, прежде всего, что скорость простой реакции пропорциональна концентрациям веществ, являющихся реагентами в данной реакции. Следовательно, для простых реакций увеличение концентрации исходных веществ практически всегда приводит к увеличению скорости (за исключением реакций нулевого порядка, скорость которых не зависит от концентрации).
Если реакция, описываемая стехиометрическим уравнением (I), характеризуется различающимися частными порядками по компонентам А и В, наибольшее влияние на скорость реакции будет оказывать изменение концентрации реагента, имеющего больший частный порядок. Например, если кинетическое уравнение реакции, в которой участвуют два реагента, имеет вид 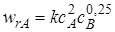 , то увеличение концентрации реагента А в 2 раза вызовет рост скорости в 4 раза, а двукратное повышение концентрации реагента В приведет к возрастанию скорости лишь в 1,19 раза.
, то увеличение концентрации реагента А в 2 раза вызовет рост скорости в 4 раза, а двукратное повышение концентрации реагента В приведет к возрастанию скорости лишь в 1,19 раза.
Для сложных реакций, в частности для параллельных, вопрос о выборе концентраций реагентов для управления процессом также не является однозначным. Рассмотрим для примера систему из двух параллельных реакций разного порядка (при постоянной температуре):
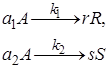 (II)
(II)
Говоря об увеличении скорости такой реакции, нужно сначала решить, какая реакция более важна, т. е. какая реакция приводит к образованию нужного целевого продукта. Нас интересует чаще всего не то, насколько быстро израсходуется реагент А, а насколько быстрее будет образовываться целевой продукт по сравнению с побочным.
Пусть в рассматриваемом примере целевым является продукт первой реакции R, а побочным – продукт S.
Для анализа соотношения скоростей целевого и побочных процессов пользуются мгновенной, или дифференциальной, селективностью, равной отношению скорости расходования реагента А на целевую реакцию к общей скорости расходования реагента и на целевую, и на побочные реакции.
Значение дифференциальной селективности в ходе процесса в общем случае не остается постоянным, так как оно определяется отношением скоростей реакций, а скорость реакции по мере ее протекания меняется. Таким образом, дифференциальная селективность характеризует эффективность целевой реакции в некоторый момент времени при некотором значении концентраций реагентов и продуктов и при заданной температуре. Лишь в том случае, когда параметры процесса во времени и пространстве не меняются (это возможно при проведении процесса в стационарном реакторе идеального смешения), φ' остается постоянной величиной.
При протекании химической реакции меняются концентрации реагентов и продуктов. Рассмотрим, как при изменении концентрации исходного реагента А для системы параллельных реакций (II) при постоянной температуре процесса меняется дифференциальная селективность φ'.
Пусть целевая реакция имеет по исходному реагенту А порядок n1, а побочная реакция – п2,тогда
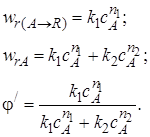 (3.5)
(3.5)
Проанализируем зависимость φ' от концентрации реагента А. Для удобства преобразуем выражение (3.5):
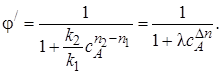 (3.6)
(3.6)
Здесь 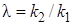 t – величина, не зависящая от концентрации реагента A; n = п2 – п1– разность порядков побочной и целевой реакций по исходному реагенту А.
t – величина, не зависящая от концентрации реагента A; n = п2 – п1– разность порядков побочной и целевой реакций по исходному реагенту А.
Очевидно, что φ' может быть как возрастающей, так и убывающей функцией от концентрации. Определим характер функции φ'(сА) по знаку первой производной:
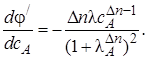 (3.7)
(3.7)
Как видно из уравнения (3.7), знак первой производной зависит от знака 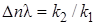 – всегда положительного, сA в любой степени также положительная величина. Если ∆n < 0, т. е. если n1 > п2(порядок целевой реакции по исходному реагенту больше порядка побочной реакции), то φ'(са) – возрастающая функция; скорость целевой реакции с ростом концентрации исходного реагента возрастает значительно быстрее скорости побочной реакции и доля скорости целевой реакции в суммарной скорости возрастает (рис. 3.1, кривая 2).
– всегда положительного, сA в любой степени также положительная величина. Если ∆n < 0, т. е. если n1 > п2(порядок целевой реакции по исходному реагенту больше порядка побочной реакции), то φ'(са) – возрастающая функция; скорость целевой реакции с ростом концентрации исходного реагента возрастает значительно быстрее скорости побочной реакции и доля скорости целевой реакции в суммарной скорости возрастает (рис. 3.1, кривая 2).
В этом случае желаемый результат – увеличение скорости образования целевого продукта R по сравнению со скоростью образования побочного продукта S (увеличение дифференциальной селективности φ') – достигается при использовании исходного реагента высокой концентрации.
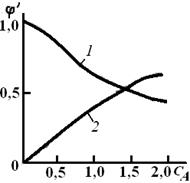
Рис. 3.1. Зависимость дифференциальной селективности от концентрации исходного реагента А для параллельных реакций при различных соотношениях порядков реакций n1 и п2: 1 – п1= 1, k1 = 10 ч–1 n2 = 2,5, k2 = 15 м4,5/(кмолъ1,5·ч);
2 – n1 = 2,5, k1 =154,5/(кмолъ1,5·ч); n2 = 1; k2 = 10 ч–1
При ∆n > 0 (n1 < п2)характер зависимости φ' от концентрации исходного реагента противоположный: dφ'/dcA < 0, следовательно, φ'(сА) – убывающая функция (кривая 1),и более высокая дифференциальная селективность по целевому продукту достигается при низкой концентрации исходного реагента. Следовательно, не всегда выгодно стремиться увеличивать концентрацию реагента. Правда, при низких концентрациях реагента небольшим будет абсолютное значение скорости при прочих равных условиях. Тогда нужно искать другие пути увеличения скорости реакции при сохранении высокого значения дифференциальной селективности. При ∆n = 0 дифференциальная селективность, как это видно из уравнения (3.7), остается постоянной величиной при любых значениях концентрации исходных реагентов, и изменить φ' можно, лишь изменив соотношение k2/k1.
Проще всего можно повлиять на это соотношение, изменив температуру проведения реакции, так как температура является одним из технологических параметров, в наибольшей степени влияющим на скорость химической реакции. Рассмотрим влияние температуры на скорость химической реакции более подробно.
Экспериментально при изучении кинетики химических реакций было обнаружено, что при увеличении температуры на 10 градусов скорость реакции возрастает в 2–4 раза. Более строго эта зависимость выражается в виде уравнения Аррениуса
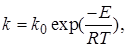 (3.8)
(3.8)
где k – константа скорости реакции; k0– предэкспоненциальный множитель; Е – энергия активации реакции; R – универсальная газовая постоянная; Т – температура.
Энергия активации элементарной реакции Е – это минимальный избыток энергии над средней внутренней энергией молекул, необходимый для того, чтобы произошло химическое взаимодействие (энергетический барьер, который должны преодолеть молекулы при переходе из одного состояния реакционной системы в другое).
Для обратимых реакций разность энергий активации прямой (E1) и обратной (Е2)реакций равна тепловому эффекту реакции.
Предэкспоненциальный множитель k0 учитывает число соударений, вероятность распада активированного комплекса реакции на исходные реагенты без образования продуктов реакции, пространственную ориентацию молекул реагентов, а также ряд других факторов, влияющих на скорость реакции и не зависящих от температуры. При более строгом рассмотрении следует учесть, что k0также зависит от температуры, но при температурах, когда RT<<Е,с достаточно хорошим приближением этой зависимостью можно пренебречь.
Часто уравнение Аррениуса представляют в виде линейной зависимости логарифма константы скорости от обратной температуры: ln k = f(l/T). В таком виде удобно провести его анализ.
Из анализа зависимости ln k = f(l/T),приведенной на рис. 3.2, можно сделать следующие выводы.
Во-первых, из неравномерности температурной шкалы следует, что химические реакции более чувствительны к изменениям температуры в области более низких температур. На прямой 1,соответствующей химической реакции с энергией активации 165 кДж/моль, выбраны два участка I и II, характеризующиеся одинаковым изменением температуры (∆T = 100 К), но в разных температурных интервалах: участок I – в области температур, близких к комнатной температуре, участок II – в области более высоких температур (~600 К). Для участка I при изменении температуры на 100 градусов константа скорости реакции k1увеличивается в 1,9·107 раз, для участка II при той же ∆T наблюдается увеличение константы скорости лишь в 820 раз, примерно на четыре порядка ниже, чем на участке I.
Второй важный вывод вытекает из сравнения температурных зависимостей скоростей реакций с различными значениями энергии активации. Чем выше энергия активации реакции, тем более чувствительна она к изменениям температуры.
При изменении температуры от 500 до 600 К скорость первой реакции (Е = 165 кДж/моль) увеличивается в 820 раз (участок II), а скорость второй реакции (E = 40 кДж/моль) – лишь в 5,3 раза (участок III).
Последний вывод чрезвычайно важен при выборе условий проведения сложных (параллельных и последовательных) реакций.
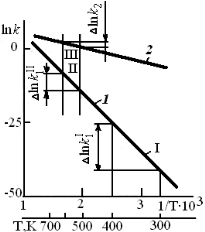
Рис. 3.2. Зависимость константы скорости химической реакции от температуры для реакций с энергиями активации 165 кДж/моль (1) и 40 кДж/моль (2): участок I – изменение ln k при росте температуры с 300 до 400 К; участок II – то же, при росте температуры с 500 до 600 К; участок III – изменение ln k для реакции с низкой энергией активации при изменении температуры с 500 до 600 К
Рассмотрим, например, влияние температуры на дифференциальную селективность для параллельных реакций (II):
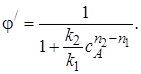
Для того чтобы выделить только влияние температуры на селективность, примем, что целевая и побочная реакции имеют одинаковый порядок (n1= п2). Преобразуем уравнение (3.6) с учетом уравнения (3.8):
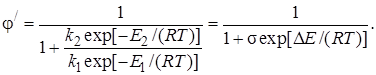
Пренебрегая слабым влиянием температуры на предэкспоненциальные множители в уравнении Аррениуса, считаем, что σ= k2,0/k1,0 от температуры не зависит. Производная положительна, если ∆Е=Е1–Е2>0, и отрицательна, если ∆Е < 0:
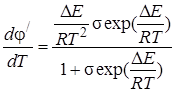 .
.
Таким образом, если энергия активации целевой реакции превышает энергию активации побочной реакции, то с ростом температуры наблюдается возрастание дифференциальной селективности, т. е. относительно более быстрое увеличение скорости целевой реакции по сравнению с ростом скорости побочной реакции и суммарной скорости процесса. Наоборот, если E1 < Е2,для увеличения дифференциальной селективности φ' нужно понижать, а не повышать температуру.
Из уравнения Аррениуса видно, что принципиально возможен еще один путь управления скоростью химической реакции – изменение величины Е – энергии активации реакции. Высота энергетического барьера реакции тесно связана с ее механизмом. Если изменить путь реакции, направив ее к конечным продуктам через некоторые новые промежуточные комплексы, то можно изменить и значение энергии активации. Такой путь возможен при применении катализаторов.
Из приведенного выше рассмотрения влияния температуры на скорость реакции с различной энергией активации следует, что в случае применения катализатора для ускорения целевого процесса при проведении параллельных реакций, возможна такая ситуация, когда энергия активации побочной реакции окажется выше энергии активации целевой реакции. Тогда повышение температуры, часто применяемое для интенсификации химико-технологических процессов, приведет к снижению селективности по целевому продукту.
Вопросы и упражнения для повторения и самостоятельной работы
1. Чем различаются определения скорости гомогенной и гетерогенной химических реакций?
2. Как взаимосвязаны между собой реальные скорости образования или расходования отдельных участников реакции aA + bB 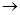 rR + sS?
rR + sS?
3. В чем заключается различие между микрокинетикой и макрокинетикой?
4. Что такое частный порядок реакции по компоненту J? Как взаимосвязаны частные порядки по разным компонентам и общий порядок реакции?
5. Какие реакции называют простыми, формально простыми, сложными?
6. Как составляют кинетические уравнения простых реакций?
7. Как составляют кинетические уравнения сложных реакций:
а) с известным механизмом реакции;
б) с неизвестным механизмом реакции?
8. Используя правило составления кинетических уравнений сложных реакций (см. § 3.2), запишите кинетические уравнения для расчета скорости по веществам А, В, R и М для сложной реакции
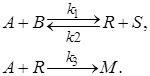
9. При постоянной температуре протекают две параллельные реакции:
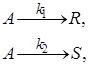
характеризующиеся значениями констант скорости k1 = 10–3 с–1, k2 = 10–2 с–1. Перед началом реакции сA,0 = 2 кмоль/м3, cR,0 = CS,0 = 0. Определите значения скорости химической реакции по исходному реагенту А (w > rА) и продукту S в момент времени, когда cR = 0,05 кмоль/м3, CS = 0,5 кмоль/м3.
10. Протекает сложная реакция
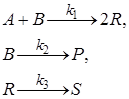
при температуре, когда константы скоростей отдельных элементарных реакций имеют следующие значения: k1= 0,02 м3/(кмоль·с), k2= 0,0015 с–1, k3 = 0,0028 c–1. Начальный состав реакционной смеси: сА,0 = 0,1 кмоль/м3, сB,0 = 0,3 кмоль/м3, cR,0 = cS,0 = сР,0 = 0. В реакторе установились концентрации продуктов: cR = 0,028 кмоль/м3, ср = 0,05 кмоль/м3; степень превращения исходного реагента хА = 0,2. Определите значения скоростей химической реакции по веществам R и Р.
11. Протекает сложная реакция
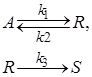
при температуре, когда константы скоростей отдельных элементарных реакций имеют следующие значения: k1 = 0,0028 c–1, k2 = 0,051 c–1, k3 = 0,0032 c–1. Начальная концентрация исходного реагента сА,0=1,65 кмоль/м3; фактическая степень превращения исходного реагента хА составляет 30 % от равновесной степени превращения хА,e; концентрация продукта RcR = 0,15 кмоль/м3. Определите значение скорости реакции по продукту R (wrR).
12. От каких микрокинетических факторов зависит скорость химической реакции?
13. В гомогенной химической реакции участвуют два реагента А и В. Реакция имеет первый порядок по реагенту А и второй порядок по реагенту В. Увеличение концентрации какого реагента даст больший эффект увеличения скорости реакции?
14. Выведите уравнение зависимости дифференциальной селективности от концентрации реагента А для параллельных реакций, имеющих разный порядок по реагенту А.
15. Вещества А и В участвуют в двух параллельных реакциях, причем частный порядок по реагенту А выше в целевой реакции, а частный порядок по реагенту В выше в побочной реакции. Какие можно сделать рекомендации по изменению концентраций реагентов для обеспечения высокой дифференциальной селективности? Как можно эти рекомендации выполнить при технологическом оформлении процесса?
16. Запишите уравнение Аррениуса в дифференциальной, интегральной и логарифмической формах. В чем суть уравнения Аррениуса?
17. Определите энергию активации реакции, если при изменении температуры с 450 до 500 °С ее скорость возрастет в 2,73 раза.
18. При температуре 748 К константа скорости реакции составляет 3,2·105 ч–1.Определите константу скорости этой реакции при температуре 793 К, если ее энергия активации Е = 87,9 кДж/моль.
19. При проведении кинетических экспериментов определены следующие значения константы скорости химической реакции (м3/(кмоль·ч)) при различных температурах (К):
Т 298 323 348 373 398 м3/(кмоль·ч).
K 0,51 0,82 1,35 1,92 2,62 К.
Определите энергию активации реакции.
20. Для реакции n-го порядка
nА 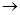 Продукты
Продукты
экспериментально получена зависимость концентрации реагента (кмоль/м3) от времени проведения реакции (мин) в периодическом реакторе при постоянной температуре:
τ, мин 0 1 2 3 4 5;
сА, кмоль/м3 2,00 0,96 0,63 0,47 0,39 0,31.
Определите порядок реакции и вычислите константу скорости.
21. Почему эффективность повышения температуры, как средства относительного увеличения скорости реакции, выше при низких температурах, чем при высоких температурах?
22. Проанализируйте зависимость дифференциальной селективности от температуры для двух параллельных реакций одинакового порядка.
23. Две параллельные реакции
а1А + b1В 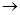 rR + sS (целевая реакция);
rR + sS (целевая реакция);
a2А + b2В  yY + zZ (побочная реакция)
yY + zZ (побочная реакция)
характеризуются кинетическими уравнениями
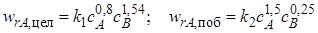
и энергиями активации E1 = 45 кДж/моль, Е2= 65 кДж/моль.
Проанализируйте зависимость дифференциальной селективности для такой системы реакций:
а) от концентрации реагента А;
б) от концентрации реагента В;
в) от температуры.
Какие можно дать рекомендации по выбору технологического режима для этого процесса на основе проведенного анализа?
24.Две параллельные реакции характеризуются одинаковым порядком и различными значениями энергии активации: энергия активации целевой реакции равна 84 кДж/моль, энергия активации побочной реакции – 45 кДж/моль. Как повлияет увеличение температуры на дифференциальную селективность? Во сколько раз изменится дифференциальная селективность φ' при увеличении температуры проведения реакции от 100 до 500 °С?
Дата добавления: 2015-06-17; просмотров: 4769;
