Классификация химических реакций, лежащих в основе промышленных химико-технологических процессов
ХИМИКО-ТЕХНОЛОГИЧЕСКИЙ ПРОЦЕСС И ЕГО СОДЕРЖАНИЕ
Химико-технологический процесс представляет собой совокупность операций, позволяющих получить целевой продукт из исходного сырья. Все эти операции входят в состав трех основных стадий, характерных практически для каждого химико-технологического процесса.
На первой стадии проводят операции, необходимые для подготовки исходных реагентов к проведению химической реакции. Реагенты переводят, в частности, в наиболее реакционноспособное состояние. Например, известно, что скорость химических реакций сильно зависит от температуры, поэтому часто реагенты до проведения реакции нагревают. Газообразное сырье для повышения эффективности процесса и уменьшения размеров аппаратуры подвергают компримированию до определенного давления. Чтобы устранить побочные явления и получить продукт высокого качества, исходное сырье подвергают очистке от посторонних примесей, пользуясь методами, основанными на различии физических свойств (растворимость в различных растворителях, плотность, температуры конденсации и кристаллизации и т. д.). При очистке сырья и реакционных смесей широко применяют явления тепло- и массообмена, гидромеханические процессы. Могут быть использованы и химические методы очистки, основанные на химических реакциях, в результате которых ненужные примеси превращаются в легко отделимые вещества.
Соответствующим образом подготовленные реагенты на следующей стадии подвергают химическому взаимодействию, которое может состоять из нескольких этапов. В промежутках между этими этапами иногда необходимо вновь использовать тепломассообменные и другие физические процессы. Например, при производстве серной кислоты диоксид серы частично окисляют до триоксида, затем реакционную смесь охлаждают, извлекают из нее путем абсорбции триоксид серы и вновь направляют ее на окисление.
В результате химических реакций получают смесь продуктов (целевых, побочных, попутных) и не прореагировавших реагентов. Заключительные операции последней стадии связаны с разделением этой смеси, для чего вновь применяют гидромеханические, тепло- и массообменные процессы, например: фильтрование, центрифугирование, ректификацию, абсорбцию, экстракцию и т. д. Продукты реакции направляют на склад готовой продукции или на дальнейшую переработку; не прореагировавшее сырье вновь используют в процессе, организуя его рецикл.
На всех этапах, а особенно на заключительных, проводят также рекуперацию вторичных материальных и энергетических ресурсов. Потоки газообразных и жидких веществ, попадающих в окружающую среду, подвергают очистке и обезвреживанию от опасных примесей. Твердые отходы либо направляют на дальнейшую переработку, либо размещают для хранения в безопасных для окружающей среды условиях.
Таким образом, химико-технологический процесс в целом – это сложная система, состоящая из единичных связанных между собой процессов (элементов) и взаимодействующая с окружающей средой.
Элементами химико-технологической системы являются перечисленные выше процессы тепло- и массообмена, гидромеханические, химические и т. д. Их рассматривают как единичные процессы химической технологии.
Важной подсистемой сложного химико-технологического процесса является химический процесс.
Химический процесс представляет собой одну или несколько химических реакций, сопровождаемых явлениями переноса теплоты, массы и импульса, оказывающих влияние как друг на друга, так и на протекание химической реакции.
Анализ единичных процессов, их взаимного влияния позволяет разработать технологический режим.
Технологическим режимом называется совокупность технологических параметров (температуры, давления, концентраций реагентов и т. д.), определяющих условия работы аппарата или системы аппаратов (технологической схемы).
Оптимальные условия ведения процесса – это сочетание основных параметров (температуры, давления, состава исходной реакционной смеси и т. д.), позволяющее получить наибольший выход продукта с высокой скоростью или обеспечить наименьшую себестоимость при соблюдении условий рационального использования сырья и энергии и минимизации возможного ущерба окружающей среде.
Единичные процессы протекают в различных аппаратах – химических реакторах, абсорбционных и ректификационных колоннах, теплообменниках и т. д. Отдельные аппараты соединены в технологическую схему процесса.
Технологическая схема – рационально построенная система единичных аппаратов, соединенных различными видами связей (прямых, обратных, последовательных, параллельных), позволяющая получить заданный продукт заданного качества из природного сырья или полуфабрикатов.
Технологические схемы бывают открытыми и закрытыми, могут содержать байпасные (обводные) потоки и рециклы, позволяющие повышать эффективность функционирования химико-технологической системы в целом.
Разработка и построение рациональной технологической схемы – важная задача химической технологии.
Классификация химических реакций, лежащих в основе промышленных химико-технологических процессов
В современной химии известно большое число различных химических реакций. Многие из них осуществляются в промышленных химических реакторах и, следовательно, становятся объектом изучения химической технологии.
Чтобы облегчить изучение близких по природе явлений, в науке принято их классифицировать по общим признакам. В зависимости от того, какие признаки взяты при этом за основу, существует несколько видов классификации химических реакций.
Важным видом классификации является классификация по механизму осуществления реакции. Различают простые (одностадийные) и сложные (многостадийные) реакции, в частности параллельные, последовательные и последовательно-параллельные.
Простыми называют реакции, для осуществления которых требуется преодоление лишь одного энергетического барьера (одна стадия).
Сложные реакции включают в себя несколько параллельных или последовательных стадий (простых реакций).
Реальные одностадийные реакции встречаются чрезвычайно редко. Однако некоторые сложные реакции, проходящие через ряд промежуточных стадий, удобно считать формально простыми. Это возможно в тех случаях, когда промежуточные продукты реакции в условиях рассматриваемой задачи не обнаруживаются.
Классификация реакций по молекулярности учитывает, сколько молекул участвует в элементарном акте реакции; различают моно-, би- и тримолекулярные реакции.
Вид кинетического уравнения (зависимости скорости реакции от концентраций реагентов) позволяет проводить классификацию по порядку реакции. Порядком реакции называется сумма показателей степеней у концентраций реагентов в кинетическом уравнении. Существуют реакции первого, второго, третьего, дробного порядков.
Химические реакции различают также по тепловому эффекту. При протекании экзотермических реакций, сопровождающихся выделением теплоты (Q > 0), происходит уменьшение энтальпии реакционной системы (∆H < 0); при протекании эндотермических реакций, сопровождающихся поглощением теплоты (Q < 0), происходит увеличение энтальпии реакционной системы (∆H > 0).
Для выбора конструкции химического реактора и способов управления проведением процесса существенное значение имеет фазовый состав реакционной системы.
В зависимости от того, сколько (одну или несколько) фаз образуют исходные реагенты и продукты реакции, химические реакции делят на гомофазные и гетерофазные.
Гомофазными называют реакции, в которых исходные реагенты, стабильные промежуточные вещества и продукты реакции находятся в пределах одной фазы.
Гетерофазными называют реакции, в которых исходные реагенты, стабильные промежуточные вещества и продукты реакции образуют более чем одну фазу.
В зависимости от зоны протекания реакции делятся на гомогенные и гетерогенные реакции.
Понятия «гомогенная» и «гетерогенная» реакции не совпадают с понятиями «гомофазный» и «гетерофазный» процессы. Гомогенность и гетерогенность реакции отражает в определенной степени ее механизм: протекает ли реакция в объеме какой-то одной фазы или на поверхности раздела фаз. Гомофазность и гетерофазность процесса позволяют лишь судить о фазовом составе участников реакции.
В случае гомогенных реакций реагенты и продукты находятся в одной фазе (жидкой или газообразной) и реакция протекает в объеме этой фазы. Например, окисление оксида азота кислородом воздуха в производстве азотной кислоты – газофазная реакция, а реакции этерификации (получение эфиров из органических кислот и спиртов) – жидкофазные.
При протекании гетерогенных реакций, по меньшей мере, один из реагентов или продуктов находится в фазовом состоянии, отличающемся от фазового состояния остальных участников, и при ее анализе обязательно должна учитываться поверхность раздела фаз. Например, нейтрализация кислоты щелочью – это гомофазный гомогенный процесс. Каталитический синтез аммиака – это гомофазный гетерогенный процесс. Окисление углеводородов в жидкой фазе газообразным кислородом представляет собой гетерофазный процесс, но протекающая химическая реакция является гомогенной. Гашение извести СаО + Н2О 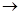 Са(ОН)2, при котором, все три участника реакции образуют отдельные фазы, а реакция идет на границе раздела воды и оксида кальция, является гетерофазным гетерогенным процессом.
Са(ОН)2, при котором, все три участника реакции образуют отдельные фазы, а реакция идет на границе раздела воды и оксида кальция, является гетерофазным гетерогенным процессом.
В зависимости от того, применяются или не применяются для изменения скорости реакции специальные вещества – катализаторы, различают каталитические и некаталитические реакции и соответственно химико-технологические процессы. Подавляющее большинство химических реакций, на которых основаны промышленные химико-технологические процессы, – это каталитические реакции.
Дата добавления: 2015-06-17; просмотров: 6110;
