Витамин Н (биотин)
Биотин – это первое вещество, которое было определено как необходимый ростовой фактор для микроорганизмов. Позже было показано токсическое действие сырого яичного белка на крыс. Употребление печени или дрожжей снимало этот эффект. Фактор, предотвращающий развитие токсикоза, был назван витамином Н или биотином (от греч. bios – жизнь).
1. Структура. Молекула биотина состоит из имидазольного и тиофенового колец и боковой цепи, представленной остатком валериановой кислоты. В пище биотин представлен биоцитином, который высвобождается путем протеолиза.
 |
2. Метаболизм
1)Биотин не модифицируется в организме, но ковалентно связывается с ферментами, в которых выполняет функцию простетической группы.
2)Биотин связывается через свободную карбоксильную группу с остатком лизина апофермента. Комплекс биотин-фермент взаимодействует с СО2 в присутствии АТФ (источник энергии) с образованием комплекса карбоксибиотин-фермент.
3)Биотинидаза катализирует удаление биотина от фермента во время метаболизма белков, что позволяет использовать биотин повторно.
3.Биологическая роль.Биотин действует как кофермент реакций промежуточного карбоксилирования, в которых служит переносчиком СО2. В отличие от фотосинтезирующих клеток, клетки животных не могут связывать СО2. Биотин участвует в реакциях временной фиксации углекислоты с выделением ее через несколько реакций. В организме 4 фермента используют биотин как кофермент.
1) Пируваткарбоксилаза. В результате карбоксилирования пирувата образуется оксалоацетат (ЩУК), который используется в глюконеогенезе и ЦТК.
2) Ацетил-КоА-карбоксилаза катализирует карбоксилирование ацетил-КоА с образованием малонил-КоА. Реакция используется при биосинтезе высших жирных кислот.
3) Пропионил-КоА-карбоксилаза превращает пропионил-КоА в D-метилмалонил-КоА, который превращается в сукцинат (вступает в ЦТК).
4) β-метил-кротонил-КоА-карбоксилаза, участвующая в катаболизме лейцина и веществ, имеющих в составе изопреноидные структуры
4.Источники.Биотин в достаточном количестве синтезируется микрофлорой кишечника. Пищевые источники: печень, сердце, яичный желток, отруби, бобы, соя, цветная капуста и др.
5.Суточная потребность.150-200 мкг.
6.Дефицит. Причинами гиповитаминоза являются:
а) применение антибиотиков, которые подавляют рост кишечной микрофлоры;
б) поступление в организм большого количества авидина – гликопротеина присутствующего в куриных яйцах, который нарушает всасывание биотина из-за образования нерастворимого комплекса;
в) нахождение длительное время на парэнтеральном питании.
г) наследственный дефект фермента, который присоединяет биотин к лизиновым остаткам апофермента.
Симптомы гиповитаминоза включают себоррейный дерматит, тошноту, выпадение волос, боли в мышцах.
Пантотеновая кислота (витамин В3)
Витамин В3 широко распространен в природе, отсюда и его название – пантотеновая кислота (от panthos – повсюду). Витамин открыт Р.Вильямсом в 1933 г., спустя десятилетие от уже был синтезирован химическим путем.
1. Структура. Пантотеновая кислота состоит из пантоевой кислоты (α,γ,-дигидрокси-β,β-диметилмасляная кислота) и β-аланина.
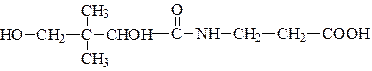
Пантотеновая кислота представляет собой вязкую светло-желтую жидкость, хорошо растворимую в воде. Она малоустойчива и легко гидролизуется по месту пептидной связи под действием слабых кислот и щелочей.
2.Метаболизм. Всасываясь на всем протяжении тонкого кишечника и в толстой кишке, в зависимости от концентрации путем простой диффузии или активного транспорта, пантотеновая кислота с током крови поступает в ткани. Пантотеновая кислота фосфорилируется с использованием АТФ до 4’-фосфопантотената. Присоединение цистеина и декарбоксилирование приводит к образованию тиоэтаноламина, из которого образуется 4’-фосфопантотеин – простетическая группа кофермента А (HS-КоА) и ацилпереносящего белка (АПБ).
3.Биологическая роль.Тиоловая группа в НS-КоА и АПБ действует как переносчик ацильных радикалов.
HS-КоА участвует в важнейших метаболических процессах:
а) обмен углеводов – окислительное декарбоксилирование пирувата в ацетил-КоА и α-кетоглутарата в сукцинил-КоА;
б) β-окисление жирных кислот на этапах активации до образования ацил-КоА и тиолитическом расщеплении с выделением ацетил-КоА и укороченного на 2 углеродных атома ацил-КоА;
в) в форме ацетил-КоА переносится остаток ацетила на холин с образованием медиатора ацетилхолина;
г) сукцинил-КоА участвует в синтезе порфиринов;
д) биосинтез жирных кислот – переносчик метаболитов в пальмитатсинтазном комплексе выполняет 4-фосфопантетеин;
ж) ацетил-КоА используется для синтеза кетоновых тел, холестерина и стероидных гормонов.
Ацетил-КоА занимает центральное место в процессах взаимосвязи обменов углеводов, аминокислот и жирных кислот.
4. Источники. Пантотеновая кислота широко распространена в продуктах животного (печень, почки, яйца, мясо, молоко и др.) и растительного (картофель, капуста, фрукты и др.) происхождения. Синтезируется кишечной микрофлорой.
5. Суточная потребность. 10-15 мг
6.Гиповитаминоз.В связи с широким распространением витамина в продуктах питания авитаминоз В3 не встречается. Симптомы гиповитаминоза: дерматиты, невриты, язвы слизистых пищеварительного тракта, нарушения продукции стероидных гормонов.
Фолиевая кислота (фолацин, витамин В9, витамин Вс)
Витамин обнаружили в 1930 г., когда было показано, что люди с определенным типом мегалобластической анемии могли быть излечены принятием в пищу дрожжей или экстракта печени. В 1941 г. фолиевая кислота была выделена из зеленых листьев (лат. folium - лист, отсюда и название витамина). Витамином Вс это соединение назвали из-за его способности излечивать анемию у цыплят (от англ. chicken – цыпленок)
1. Структура. Фолиевая кислота состоит из птеридина, связанного с p-аминобензойной кислотой (ПАБК) и глутаминовой кислотой.
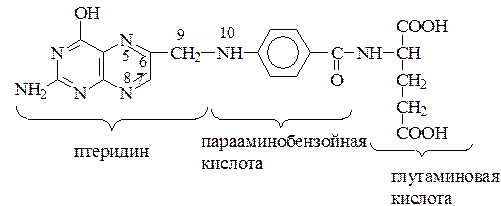
Фолиевая кислота плохо растворима в воде и органических растворителях, но хорошо в щелочных растворах. Разрушается под действием света, при обработке и консервировании овощей.
2.Метаболизм. Фолат в пище присутствует в форме полиглутамата. Внешние остатки глутамата удаляются в кишечнике до всасывания, главным образом, в тонком кишечнике. Коферментной формой фолиевой кислоты является 5,6,7,8-тетрагидрофолиевая кислота (ТГФК), которая образуется из фолиевой кислоты под действием фермента дигидрофолатредуктазы и с использованием НАДФН как донора атомов водорода
3.Биологическая роль
1) Фолиевая кислота является переносчиком одноуглеродных радикалов: метильного(-СН3), метиленового (=СН2), метинильного (≡СН), формильного (-СНО) и формиминового (-СН=NH). Одноуглеродные фрагменты связываются с ТГФК в положениях N5 или N10. Присоединение формильного радикала в 5 положении приводит к образованию N5-формилТГФК, которая известна как фолиниковая кислота. МетиленТГФК образуется при взаимодействии ТГФК с глицином, серином или холином.
2) Фолат необходим для синтеза пуриновых нуклеотидов (2 и 8 атомы углерода) и синтеза тимина. N5,N10-метиленТГФК вводит метильную группу при синтезе тимидилата, необходимого для синтеза ДНК и образования эритроцитов.
3) Участвует в метаболизме глицина, серина и этаноламина.
4) N-формилметионин является инициирующей аминокислотой в биосинтезе белка.
5) В крови ТГФК присутствует как N5-метилТГФК. Витамин В12 необходим для превращения N5-метилТГФК в ТГФК в реакции превращения гомоцистеина в метионин. Эта реакция необходима для освобождения свободной ТГФК и повторного использования в одноуглеродном метаболизме. При дефиците витамина В12 блокируется превращение N5-метилТГФК в ТГФК.
4. Источники: кишечная микрофлора, свежие овощи – салат, капуста, морковь, помидоры, лук.
5.Суточная потребность: 50-200 мкг.
6.Дефицит. При дефиците ТГФК снижается синтез пуринов и тимина, что приводит к нарушению синтеза ДНК. Это проявляется развитием мегалобластической анемии, которая характеризуется появлением в крови незрелых ядросодержащих форм эритроцитов.
Витамин В12 (кобаламин, антианемический витамин)
Злокачественная анемия (болезнь Аддисона-Бирмера) оставалась смертельным заболеванием до 1926 г., когда впервые для ее лечения применили сырую печень. Поиски содержащегося в печени антианемического фактора привели к успеху и в 1955 г. Дороти Ходжкин расшифровала структуру этого фактора и его пространственную конфигурацию с помощью метода рентгеноструктурного анализа.
1. Структура. Структура витамина В12 отличается от строения всех других витаминов наличием в молекуле иона металла – кобальта. Кобальт связан координационными связями с атомами азота, входящими в состав четырех пиррольных колец, которые образуют планарную (плоскую структуру), называемую коррином. I, II, III пиррольные кольца связаны через метиленовые мостики, IV и I – непосредственно. Перпендикулярно плоскости коррина расположен нуклеотид, содержащий 5,6-диметилбензимидазол, α-D-рибозу и остаток фосфорной кислоты, который связан координационной связью с атомом кобальта (рис. 15.1). В пище кобаламин содержит атом кобальта в окисленной форме (III). Для образования активных коферментных форм атом кобальта восстанавливается до Со (I).
В витамине В12 атомы углерода пиррольных колец замещены метильными, ацетамидными и пропионамидными радикалами. Пропионамидный радикал в IV кольце через изопропиловый спирт связан с фосфатным остатком нуклеотида.
Атом кобальта трехвалентен и ковалентно связан с группой CN-.Вся структура получила название цианокобаламина или кобаламина, поскольку считают, что цианид-ион является артефактом, зависящим от способа выделения.
Кобаламины растворимы в воде, термостабильны и устойчивы в присутствии растворов кислот при рН 4,0.
2.Метаболизм
1)Витамин В12, содержащийся в пище, называют внешним фактором Кастла. Всасывается витамин в тонком кишечнике в комплексе с внутренним фактором Кастла (гликопротеин, секретируемый париетальными клетками желудка).
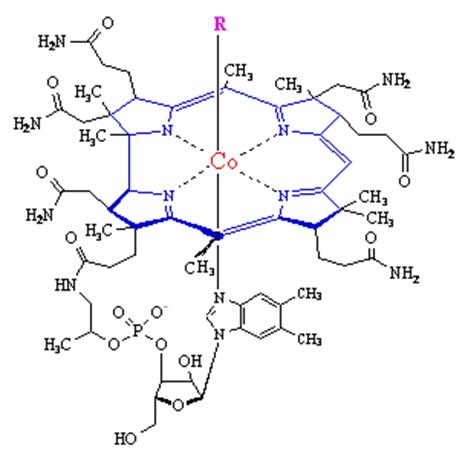
Рис. 15.1. Витамин В12
Витамин В12 находится в пище в комплексе с белками. В желудке под действием соляной кислоты и пепсина витамин В12 высвобождается из комплекса с белками и связывается с кобалофилином (R-протеин, гаптокоррин) – белком, секретируемым слюной. В двенадцатиперстной кишке комплекс распадается, кобалофилин гидролизуется панкреатическими протеазами, витамин В12 связывается с внутренним фактором Кастла. Комплекс витамин В12-внутренний фактор Кастла всасывается в дистальной части подвздошной кишки через рецепторы (кубилины), которые связывают комплекс, но не связывают свободный фактор или свободный витамин. Другой белок – мегалин – связан с кубилином и обеспечивает процесс эндоцитоза для всасывания комплекса
2) Витамин транспортируется в крови в комплексе с белками, называемыми транскобаламинами и превращается в метилкобаламин и 5-дезоксиаденозилкобаламин в печени, клетках костного мозга и ретикулоцитах. Транскобаламин I участвует в хранении и резервировании водорастворимого витамина в печени и плазме крови (циркулирующий резерв). Транскобаламин II транспортирует витамин в крови. Комплекс транскобаламин II-витамин В12 поступает в периферические клетки путем эндоцитоза. В лизосомах клеток транскобаламин II разрушается, витамин высвобождается в виде гидроксикобаламина, который либо превращается в цитозоле в метилкобаламин, либо в митохондриях – в 5-дезоксиаденозилкобаламин. В печени запасается около 4-5 мг витамина и этих запасов достаточно для обеспечения организма витамином в течение 4-6 лет.
3.Биологическая роль
1) В организме человека витамин необходим для 2-х важнейших реакций:
а) 5-дезоксиаденозилкобаламин является коферментом метилмалонил-КоА-мутазы, который превращает метилмалонил-КоА в сукцинил-КоА. Метилмалонил-КоА образуется как промежуточный продукт катаболизма валина и карбоксилирования пропионил-КоА, синтезирующегося при катаболизме изолейцина, холестерола, жирных кислот с нечетным числом атомов углерода или прямо из пропионовой кислоты (продукт микробиологической ферментации в кишечнике). В результате этой реакции метилмалонил-КоА превращается в сукцинил-КоА.
б) Метилкобаламин является коферментом гомоцистеинметилтрансферазы, которая катализирует метилирование гомоцистеина в метионин. Кобаламин забирает метильные группы от N5-метилтетрагидрофолиевой кислоты и превращает ее в тетрагидрофолат. Метаболическое значение этой реакции состоит в том, что сохраняются запасы метионина и тетрагидрофолата, что необходимо для синтеза пуриновых, пиримидиновых нуклеотидов и синтеза нуклеиновых кислот. При дефиците витамина В12 фолат постоянно находится в форме N5-метил-ТГФК («фолатная» или метильная ловушка).
в) Витамин В12 требуется для превращения D-рибонуклеотидов в дезокси-D-рибонуклеотиды. Эту реакцию у прокариот катализирует специфическая рибонуклеотид-редуктаза.
4.Источники. Основным источником витамина являются микроорганизмы. В растительной пище витамин В12 отсутствует. В небольших количествах витамин образуется бактериями на поверхности фруктов. Значительное количество витамина содержится в печени, дрожжах, молоке, яичном желтке.
5.Дефицит
а) Энтеропеченочная циркуляция витамина В12 обеспечивает организм достаточным количеством витамина и дефицит может развиваться при отсутствии витамина в диете в течение нескольких лет. При заболеваниях желудка или подвздошной кишки дефицит витамина может развиваться быстрее.
б) Пернициозная анемия является следствием дефицита витамина В12 и характеризуется нарушением синтеза ДНК, образования эритроцитов и появлением незрелых ядерных форм эритроцитов (мегалобластов).
в) длительное вегетарианство может приводить к дефициту витамина В12.
6. Суточная потребность. 2-5 мкг.
Дата добавления: 2015-06-12; просмотров: 1969;
