Водорастворимые витамины
К водорастворимым витаминам относят витамины группы В, С, Р, Н.
Витамин С (аскорбиновая кислота, антискорбутный витамин)
1.Структура.Витамин С по структуре представляет собой g-лактон, имеющий 2 ассиметричных атома углерода. Биологически активной является L-форма аскорбиновой кислоты.
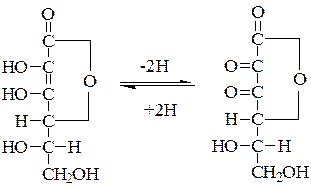
Аскорбиновая кислота Дегидроаскорбиновая кислота
Кислые свойства аскорбиновой кислоты обусловлены наличием 2-х енольных гидроксильных групп. L-аскорбиновая кислота обратимо подвергается окислению с образованием дегидроаскорбиновой кислоты под действием фермента аскорбатоксидазы. Восстановление дегидроаскорбиновой кислоты в аскорбиновую осуществляется с участием редуктазы и восстановленного глутатиона. Аскорбиновая и дегидроаскорбиновая кислоты являются биологически активными формами витамина. При гидратации в присутствии кислорода дегидроаскорбиновая кислота необратимо окисляется в 2,3-дикетогулоновую кислоту, которая не обладает биологической активностью и распадается до щавелевой и треоновой кислот. Скорость разрушения витамина возрастает с повышением температуры, в щелочной среде, под действием УФ-лучей, в присутствии солей тяжелых металлов (например, меди). Аскорбиновая кислота разрушается в процессе приготовления пищи и хранения продуктов.
2.Метаболизм.Аскорбиновая кислота всасывается путем простой диффузии на всем протяжении желудочно-кишечного тракта, но преимущественно в тонком кишечнике. В организме не накапливается.
3.Биологическая роль.
1) Окислительно-восстановительные реакции. Аскорбиновая кислота является сильным восстановителем с окислительно-восстановительным потенциалом +0,08 в и участвует в восстановлении молекулярного кислорода, нитратов и цитохромов а и с.
2) Витамин С участвует в гидроксилировании остатков пролина и лизина в процессе биосинтеза коллагена. ОН-группы гидроксипролина необходимы для стабилизации структуры коллагена, формируя водородные связи между цепями триплетной спирали зрелого коллагена. Гидроксилизин в коллагене служит для образования участков связывания с полисахаридами. Витамин С необходим для формирования костной ткани, поскольку основными компонентами костной ткани являются органический матрикс, коллаген, неорганический кальций и фосфаты.
3) Витамин С участвует в метаболизме тирозина. При синтезе катехоламинов норадреналина и адреналина из тирозина в надпочечниках и центральной нервной системе происходит окисление Cu+ в Cu2+; для обратного процесса восстановления меди необходима аскорбиновая кислота. Кроме того, аскорбиновя кислота требуется для окисления p-гидроксифенилпирувата в гомогентизиновую кислоту.
4) Витамин С необходим для гидроксилирования триптофана в гидрокситриптофан при биосинтезе серотонина.
5) Витамин С участвует в биосинтезе желчных кислотиз холестерина.
6) Синтез кортикостероидных гормонов. В коре надпочечников содержится высокая концентрация витамина С, особенно в период стресса. Предполагают, что витамин С необходим для синтеза кортикостероидов.
7) Метаболизм железа и гемоглобина. Аскорбиновая кислота повышает всасывание железа из кишечника путем его восстановления в Fe2+. Витамин С участвует в образовании ферритина и высвобождение железа из связи его с транспортным белком крови трансферрином. Витамин С способствует восстановлению метгемоглобина в гемоглобин и участвует в деградации гемоглобина до желчных пигментов.
8) Метаболизм фолиевой кислоты. Активной формой фолиевой кислоты является тетрагидрофолиевая кислота (ТГФК). Витамин С необходим для образования ТГФК. Вместе с ТГФК аскорбиновая кислота участвует в созревании эритроцитов.
9) Витамин С является водорастворимым антиоксидантом и защищает клетки от повреждения свободными радикалами. Антиоксидантная функция аскорбиновой кислоты объясняется ее способностью легко отдавать два атома водорода, используемых в реакциях обезвреживания свободных радикалов.
4.Источники. В организме человека, обезьян, морских свинок и некоторых птиц витамин С не синтезируется. Источником витамина С служит растительная пища. Особенно им богаты перец, черная смородина, укроп, петрушка, капуста, щавель, цитрусовые, земляника.
5.Суточная потребность70-120 мг.
6.Гиповитаминозпроявляется повышенным утомлением, снижением аппетита, сниженной устойчивостью к простудным заболеваниям, кровоточивость десен. Авитаминоз приводит к заболеванию цингой (скорбутом). Главными симптомами цинги являются нарушение проницаемости капилляров, обусловленное недостаточностью гидроксилирования пролина и лизина в коллагене, расшатывание и выпадение зубов, отеки и боли в суставах, поражение костей, нарушение заживления ран. Смерть обычно наступает от кровоизлияния в полость перикарда. При гиповитамизозе С развивается железодефицитная анемия из-за нарушения всасывания железа и использования его запасов при синтезе гемоглобина.
Витамин В1 (тиамин, антиневритный витамин)
1.Структура.Витамин В1 был первым витамином, выделенным в кристаллическом виде К.Функом в 1912 г. Позже был осуществлен его химический синтез. Свое название – тиамин – получил из-за наличия в составе его молекулы атома серы и аминогруппы. Тиамин состоит из 2-х гетероциклических колец – аминопиримидинового и тиазолового. Последнее содержит каталитически активную функциональную группу – карбанион (относительно кислый углерод между серой и азотом).
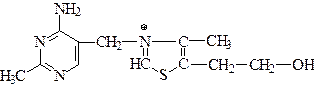
Тиамин устойчив в кислой среде и выдерживает нагревание до высокой температуры. В щелочной среде витамин быстро разрушается.
2.Метаболизм.В желудочно-кишечном тракте различные формы витамина гидролизуются с образованием свободного тиамина. Большая часть тиамина всасывается в тонком кишечнике с помощью специального механизма активного транспорта, остальное количество расщепляется тиаминазой кишечных бактерий. С током крови всосавшийся тиамин попадает вначале в печень, где фосфорилируется, а затем переносится в другие органы и ткани.
тиаминпирофосфаткиназа
 АТФ + тиамин тиаминпирофосфат + АМФ
АТФ + тиамин тиаминпирофосфат + АМФ
Витамин В1 присутствует в различных органах и тканях как в форме свободного тиамина, так и его фосфорных эфиров: тиаминмонофосфата, тиаминдифосфата и тиаминтрифосфата. Основной коферментной формой (60-80% от общего внутриклеточного) является тиаминпирофосфат (ТПФ).
После распада коферментов свободный тиамин выделяется с мочой и определяется в виде тиохрома.
3.Биологическая роль
1. ТПФ является коферментом 3-х полиферментных комплексов, которые катализируют окислительное декарбоксилирование кетокислот.
а) Пируватдегидрогеназный комплекс участвует в окислительном декарбоксилировании пирувата, что является одной из ключевых реакций в обмене углеводов. В результате этой реакции образуется ацетил-КоА, который включается в цикл трикарбоновых кислот, где окисляется до углекислоты и воды. Благодаря этой реакции создаются условия для полного окисления углеводов и утилизации всей заключенной в них энергии. Кроме того, образующийся ацетил-КоА служит источником для синтеза многих биологических продуктов: жирных кислот, холестерина, стероидных гормонов, кетоновых тел и т.д.
б) α-Кетоглутаратдегидрогеназный комплекс входит в состав ЦТК и катализирует окислительное декарбоксилирование α-кетоглутарата с образованием сукцинил-КоА.
в) Дегидрогеназа кетокислот с разветвленным углеродным радикалом участвует в метаболизме валина, изолейцина и лейцина.
2. ТПФ является коферментом транскетолазы – фермента пентозофосфатного пути окисления углеводов, основными продуктами которого являются НАДФН и рибоза.
3. Витамин В1 принимает участие в синтезе ацетилхолина, катализируя в пируватдегидрогеназной реакции образование ацетил-КоА.
4.Источники. Довольно много витамина содержится в пшеничном хлебе из муки грубого помола, в оболочке семян хлебных злаков, в сое, фасоли, горохе, дрожжах. Из продуктов животного происхождения наиболее богаты тиамином печень, нежирная свинина, почки, мозг, яичный желток.
5.Суточная потребность составляет 2-3 мг.
6.Гиповитаминоз проявляется слабостью, снижением аппетита, тошнотой, нарушением периферической чувствительности, онемением пальцев, ощущением ползанья «мурашек», болями по ходу нервов. При авитаминозе развивается заболевание бери-бери, что в переводе с индийского означает овца, т.к.походка больного человека напоминает поступь овцы. Характерно поражение сердечно-сосудистой и нервной систем. Особая чувствительность нервной ткани к недостатку тиамина объясняется тем, что коферментная форма этого витамина необходима нервным клеткам для усвоения глюкозы.
Витамин В2 (рибофлавин)
1.Структура. Витамин В2 отличается от других витаминов желтым цветом (flavus – желтый). Рибофлавин впервые был выделен из кисломолочной сыворотки. Молекула рибофлавина состоит из гетероциклического изоаллоксазинового ядра, к которому в 9-м положении присоединен спирт рибитол (производное D-рибозы). Термином флавины обозначаются многие производные изоаллоксазина, обладающие Вв-витаминной активностью.
Биосинтез флавинов осуществляется растительными и многими бактериальными клетками, а также плесневыми грибками и дрожжами. Благодаря микробному биосинтезу рибофлавина в желудочно-кишечном тракте жвачные животные не нуждаются в этом витамине. У других животных и человека синтезированных в кишечнике флавинов недостаточно для предупреждения гиповитаминозов. Витамин В2 хорошо растворим в воде, устойчив в кислой среде, но легко разрушается в нейтральной и щелочной, в также под действием видимого и УФ-света. Витамин В2 легко подвергается обратимому восстановлению, присоединяя водород по месту двойных связей (1 и 10), превращаясь из оранжево-желтого раствора в бесцветную лейкоформу.
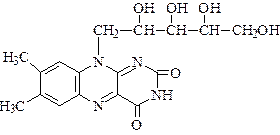
2.Метаболизм. В пище витамин В2 находится преимущественно в составе своих коферментных форм, связанных с белками – флавопротеинов. Под влиянием пищеварительных ферментов витамин высвобождается и всасывается путем простой диффузии в тонком кишечнике. В клетках слизистой кишечника, крови, печени и других тканях рибофлавин фосфорилируется до флавинмононуклеотида (ФМН) и флавинадениндинуклеотида (ФАД).
3. Биологическая роль.Основное значение витамина В2 состоит в том, что он входит в состав флавиновых коферментов – ФМН и ФАД. Различают два типа реакций, катализируемых флавопротеинами:
1)Простые дыхательные системы – это прямое окисление субстрата с участием кислорода, перенос на него атомов водорода с образованием Н2О2 и выделением энергии в виде тепла: оксидазы L- и D-аминокислот, ксантиноксидаза (разрушение пуриновых азотистых оснований), альдегиддегидрогеназа (деградация альдегидов).
2)Участие в сложных дыхательных системах (полная и укороченная цепи переноса электронов во внутренней мембране митохондрий): сукцинатдегидрогеназа и ацил-КоА-дегидрогеназа (дегидрирование метаболита ЦТК сукцината и ацил-КоА при окислении жирных кислот и направление протонов и электронов в укороченную дыхательную цепь); НАДН-дегидрогеназа (перенос протонов и электронов от НАДН+Н+ матрикса митохондрий в полную цепь переноса протонов и электронов во внутренней мембране митохондрий, разделение потоков протонов и электронов); дигидролипоилдегидрогеназа (фермент окислительного декарбоксилирования α-кетокислот, переносящий протоны и электроны с восстановленного ФАД на НАД+ и последующем введении их в полную цепь переноса электронов внутренней мембраны митохондрий).
4.Источники.Основными источниками рибофлавина являются печень, почки, желток куриного яйца, творог. В кислом молоке витамина содержится больше, чем в свежем. В растительных продуктах витамина В2 мало (исключение – миндальные орехи). Частично дефицит рибофлавина восполняется кишечной микрофлорой.
5.Суточная потребность 2-3 мг.
6.Гиповитаминоз. Недостаток витамина В2, как и других витаминов, проявляется слабостью, повышенной утомляемостью, склонностью к простудным заболеваниям. К специфическим проявлениям недостаточности рибофлавина относятся воспалительные процессы в слизистых оболочках. Слизистая губ и полости рта становится сухой, язык приобретает ярко-красный цвет, в углах рта появляются трещины. Отмечается повышенное шелушение эпителия кожи, особенно на лице.
Витамин РР (витамин В5, никотиновая кислота, никотинамид, ниацин; антипеллагрический витамин)
1.Структура.Витамин РР выделен К.Эвельгеймом в 1937 г. Его введение предохраняло от заболевания пеллагра или излечивало ее. РР означает противопеллагрический (preventive pellagra).
Никотиновая кислота является пиридин-3-карбоновой кислотой, никотинамид – ее амидом. Оба соединения в организме легко превращаются друг в друга и поэтому обладают одинаковой витаминной активностью.
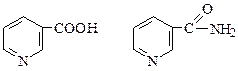
Витамин РР плохо растворим в воде, но хорошо в водных растворах щелочей.
2.Метаболизм.Поступающий с пищей витамин РР быстро всасывается в желудке и кишечнике в основном путем простой диффузии. С током крови никотиновая кислота попадает в печень и другие органы, несколько медленнее проникает в них никотинамид. В тканях оба соединения преимущественно используются для синтеза коферментных форм НАД+ и НАДФ+. Часть никотинамидных коферментов синтезируется в организме животных из триптофана. Однако этот путь, в который вовлекается до 2% метаболического пула триптофана, значительно уступает по эффективности первому (т.е. из прямого витаминного предшественника).
3.Биологическая роль.Значение витамина РР определяется ролью коферментов НАД+ и НАДФ+.
1) НАД+ входит в состав дегидрогеназ, катализирующих окисительно-востановительные превращения пирувата, изоцитрата, α-кетоглутарата, малата и др. Эти реакции чаще локализованы в митохондриях и служат для освобождения энергии в сопряженных митохондриальных цепях переноса протонов и электронов.
2) НАДФ+ входит в состав дегидрогеназ (редуктаз), которые чаще локализованы в цитозоле или эндоплазматическом ретикулуме и служат для восстановительных синтезов (НАДФ-зависимые дегидрогеназы пентозофосфатного пути, синтеза жирных кислот и холестерина, микросомальные и митохондриальные монооксигеназные системы для синтеза желчных кислот, кортикостероидных гормонов).
3) НАД+ иНАДФ+ - аллостерические регуляторы ферментов энергетического обмена
4.Источники. Продукты животного (печень, мясо) и растительного происхождения (рис, хлеб, картофель). Молоко и яйца содержат следы ниацина, но в них содержится триптофан, что может компенсировать недостаточное поступление никотинамида с пищей.
5.Суточная потребность составляет 15-25 мг.
6.Гиповитаминоз. Характерным признаком недостаточности витамина РР является симптомокомплекс «три Д»: дерматит, диарея и деменция. В основе заболевания лежит нарушение пролиферативной активности и энергетики клеток. Дерматит чаще всего отмечается на открытых участках кожи, которая под действием солнечных лучей краснеет, покрывается пигментными пятнами (на лице в виде крыльев бабочки) и шелушится. Язык становится ярко-красным и болезненным, утолщается, на нем появляются трещины. Расстройство пищеварения проявляется тошнотой, отсутствием аппетита, болями в животе. Нарушается функция периферических нервов и центральной нервной системы.
Симптомы гиповитаминоза развиваются:
а) У лиц с недостатком белка в диете. Объясняется это тем, что животные белки содержат оптимальное количество аминокислоты триптофана, витамина В6 и некоторые другие компоненты, необходимые для синтеза ниацина.
б)При постоянном питании маисом, где ниацин находится в связанной форме
в) При постоянном питании сорго, зерна которого содержат высокую концентрацию лейцина – ингибитора ключевого фермента превращения триптофана в НАД.
г) При дефиците витамина В6 и его коферментных форм пиридоксальфосфата, необходимого для синтеза из триптофана коферментных форм.
Витамин В6 (пиридоксин, антидерматитный витамин)
1.Структура. Витамин В6 включает три природных производных пиридина, обладающих одинаковой витаминной активностью: пиридоксина, пиридоксаля, пиридоксамина, отличающихся друг от друга наличием соответственно спиртовой, альдегидной или аминогруппы. Витамин В6 открыт в 1934 г. А.Сент-Дьердьи. Пиридоксин хорошо растворяется в воде и этаноле, устойчив в кислой и щелочной среде, но легко разрушается под действием света при рН=7,0.
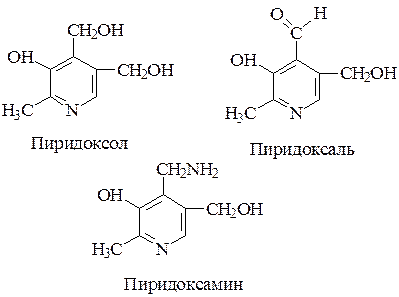
2Метаболизм.Всосавшись в тонком кишечнике, все формы витамина с током крови разносятся к тканям и, проникая в клетки, фосфорилируются с участием АТФ. Коферментные функции выполняют два фосфорилированных производных пиридоксина: пиридоксальфосфат и пиридоксаминфосфат.
3.Биологическая роль. Витамин В6 характеризуется широким спектром биологического действия. Он принимает участие в регуляции белкового, углеводного и липидного обмена, биосинтезе гема и биогенных аминов, гормонов щитовидной железы и других биологически активных соединений. Коферментные формы витамина В6 входят в состав следующих ферментов:
1) Аминотрансфераз аминокислот, катализирующих обратимый перенос NH2-группы от аминокислоты на α-кетокислоту (образование заменимых аминокислот, непрямое дезаминирование и восстановительное аминирование аминокислот).
2) Декарбоксилаз аминокислот, отщепляющих карбоксильную группу аминокислот, что приводит к образованию биогенных аминов.
3) Ферментов, осуществляющих неокислительное дезаминирование серина, треонина, триптофана, серусодержащих аминокислот.
4) Мышечной фосфорилазы (распад гликогена).
4.Источники. Витамином В6 богаты бобовые, зерновые культуры, мясные продукты, рыба, картофель. Он синтезируется кишечной микрофлорой, частично покрывая потребность организма в этом витамине.
5.Суточная потребность. 2-3 мг
6.Гиповитаминоз. Основными проявлениями недостаточности витамина В6 являются гипохромная анемия и судороги. Отмечается развитие сухого себорейного дерматита, стоматита и глоссита. Чаще всего пиридоксиновая недостаточность:
а) наблюдается у маленьких детей при искусственном вскармливании стерилизованным молоком (разрушается витамин В6), у беременных при токсикозах;
б) групповой недостаточности витаминов группы В;
в) подавлении микрофлоры антибиотиками;
г) у алкоголиков, поскольку ацетальдегид стимулирует дефосфорилирование пиридоксальфосфата
Дата добавления: 2015-06-12; просмотров: 1993;
