Металлы d-блока периодической системы
который имеет такое же расположение атомов металла и хлора, а атом углерода находится в центре октаэдра.
Трихлорид рения состоит из кластеров Re3Cl9, слабо связанных мостиковыми атомами хлора ( рис. 9.19 ). Это вещество является исходным продуктом для получения хорошо изученных соединений, содержащих кластер из трех атомов. Как и в случае хлорида молибдена ( П ), мостики между кластерами в твердом состоянии могут быть разрушены при реакции с подходящими лигандами. Например, взаимодействие Re3Cl9 с хлорид-ионами приводит к образованию дискретного комплекса [ Re3Cl12 ]3-. Нейтральные лиганды, например алкилфосфины, также могут занимать эти координационные позиции и образовывать кластеры с общей формулой Re3Cl9L3.
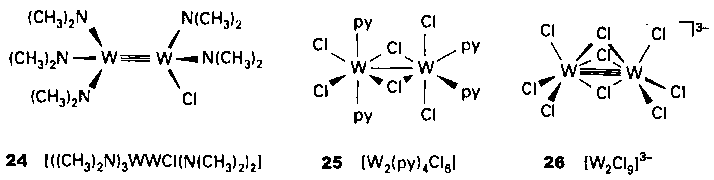
Известно много соединений, имеющих связь между двумя атомами металла. Наиболее обычными фрагментами таких структур являются этаноподобные структуры (24), два октаэдра, соединенные ребрами (25) или гранями (26), и тетрагональная призма, которая уже упоминалась для [Re2Cl8]2- (18). Далее основное внимание будет сконцентрировано на связи, образующейся в структурах последнего типа, ее порядок может быть от единицы до четырех.
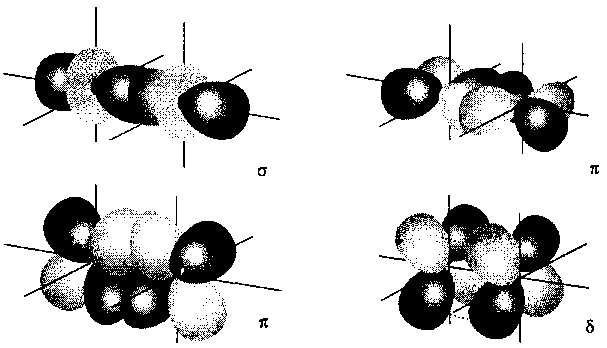
Рис. 9.20. Происхождение ó-, π- и (б-связывания между двумя атомами d-металла, расположенными вдоль оси z. Показаны только связывающие комбинации.
Как показано на рис. 9.20, ó-связь между двумя атомами металла может образовываться при перекрывании dz2-орбиталей каждого атома, π-связи образуются при перекрывании dxz- или dyz-орбиталей (возможны обе такие π-связи), и, наконец, б-связь осуществляется при перекрывании двух находящихся друг против друга dxy-орбиталей.
Дата добавления: 2015-05-30; просмотров: 762;
