Уравнение правила фаз.
Пусть рассматриваемая система состоит из f - фаз и k - компонентов, причем каждый из k - компонентов находится в каком-то количестве в каждой из f - фаз.
Давление и температура одинаковы для всех фаз данной системы, т.е. имеется два общих параметра состояния.
Так как каждый компонент находится в каждой фазе, то возможные концентрации компонентов во всех фазах:
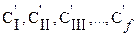 - для первого компонента;
- для первого компонента;
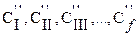 - для второго компонента;
- для второго компонента;
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
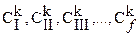 - для k - го компонента. (6.1)
- для k - го компонента. (6.1)
Число возможных концентраций компонентов составит величину k 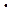 f . Итого, для рассматриваемой системы общее число параметров состояния равно (k
f . Итого, для рассматриваемой системы общее число параметров состояния равно (k  f + 2), где цифра учитывает число общих параметров для всех фаз данной системы - давление и температуру.
f + 2), где цифра учитывает число общих параметров для всех фаз данной системы - давление и температуру.
Для каждой из фаз имеется свое уравнение состояния.
Например, для первой фазы это уравнение таково:
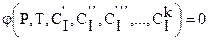 . (6.2)
. (6.2)
Таких уравнений столько, сколько фаз в системе, т.е. f - штук.
Система находится в состоянии термодинамического равновесия, что означает равенство химических потенциалов компонентов ( 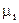 ) во всех фазах системы, т.е.:
) во всех фазах системы, т.е.:
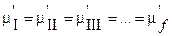 - для первого компонента;
- для первого компонента;
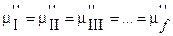 - для второго компонента;
- для второго компонента;
- - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - - -
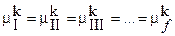 - для k - го компонента. (6.3)
- для k - го компонента. (6.3)
Число строк в матрице равно числу компонентов (k), а число столбцов равно (f - 1), тогда общее число уравнений составит:
k(f - 1).
Таким образом, общее число уравнений, связывающих значения химических потенциалов компонентов вычислится как
f + k(f - 1).
Согласно определению, число степеней свободы равно разности между общим числом параметров состояния и числом уравнений, связывающих эти параметры:
с = (k 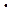 f + 2) - [f + k(f - 1)]
f + 2) - [f + k(f - 1)]
или
с = k - f + 2. (6.4)
т. е. число степеней свободы равно разности между числом компонентов и фаз плюс два.
В системах без участия в равновесии газообразной фазы, один из параметров, общий для всех фаз системы, а именно давление, не оказывает влияние на равновесие в системе, если изменяется в небольших пределах и поэтому исключается из числа общих параметров состояния. Это положение применимо, в частности, к металлическим расплавам и поэтому уравнение правила фаз записывается в виде:
с = k - f + 1. (6.5)
Равновесие нонвариантно (безвариантно), если с = 0, моновариантно (одновариантно), если с = 1 и дивариантно (двухвариантно), если с = 2.
Дата добавления: 2015-05-21; просмотров: 831;
