Системах и термодинамические условия равновесия.
Полные дифференциалы от F и G:
dF = dU - TdS - SdT и dG = dU - TdS - SdT + pdV + Vdp. (4.58)
Из соотношения (4.51):
dU 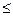 TdS - pdV. (4.59)
TdS - pdV. (4.59)
Тогда
dF 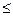 TdS - pdV - TdS - SdT и dG
TdS - pdV - TdS - SdT и dG 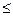 TdS - pdV - TdS - SdT + pdV + Vdp
TdS - pdV - TdS - SdT + pdV + Vdp
и окончательно:
dF 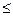 - SdT - pdV и dG
- SdT - pdV и dG 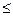 - SdT + Vdp. (4.60)
- SdT + Vdp. (4.60)
Полученные соотношения (4.60) показывают, что при V, T = const (изохорно - изотермические условия):
dF 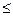 0, (4.61)
0, (4.61)
а при p, T = const (изобарно - изотермические условия):
dG 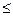 0, (4.62)
0, (4.62)
Таким образом в неизолированных системах, находящихся в условиях V, T = const самопроизвольно могут быть реализованы процессы, сопровождающиеся уменьшением энергии Гельмгольца, а в случае р, Т = const - уменьшением энергии Гиббса.
Пределом протекания процессов или состоянием термодинамического равновесия является достижение некоторого минимума этих функций для данных условий:
d(F, G) = 0 и d2(F, G) > 0. (4.63)
Дата добавления: 2015-05-21; просмотров: 689;
