Горение оксида углерода и углеводородов.
По разветвленным цепным реакциям протекает горение и других составляющих газообразных топлив: оксида углерода, метана и других углеводородов. На горение оксида углерода существенное влияние оказывает наличие в газе паров воды, которые участвуют в реакциях продолжения цепей. Поэтому в выражение для скорости горения оксида углерода входит концентрация паров воды:
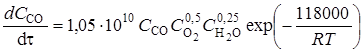 . (3.7)
. (3.7)
Как показывает эксперимент, сухой оксид углерода не горит. Это связано с тем, что в отсутствие радикалов Н и ОН горение СО не имеет разветвленного цепного механизма. При появлении атомарного кислорода
О2 + ν = 2О,
он тут же вступает в реакцию с оксидом углерода, что приводит к обрыву цепей
О + СО = СО2.
Появление в смеси радикалов Н и ОН приводит к образованию дополнительных радикалов О
Н + О2 = ОН + О.
Кроме того, при протекании реакции
ОН + СО = СО2 + Н
дополнительно генерируются радикалы Н, что приводит к разветвленному механизму горения СО.
Таким образом, при помощи водяных паров или водорода в пламени создаются радикалы Н и ОН, необходимые для реакций разветвления цепей.
Скорость горения углеводородов меньше, чем скорость горения водорода и оксида углерода. Горение их протекает по более сложным механизмам, одновременно с процессом горения углеводородов протекают реакции термического разложения с образованием сажистого углерода С. Полное описание горения метана предполагает рассмотрение более 400 реакций. Основные из них следующие:
- реакция отщепления первого атома водорода от метана в присутствии кислорода
СН4 + О2 ® СН3 + Н + О2,
- образование радикалов О и ОН
Н + О2 ® ОН + О,
- реакции образования и окисления метанола СН3ОН и диссоциация формальдегида НСНО с образованием водорода и оксида углерода
СН3 + ОН ® СН3ОН,
СН3ОН + О ® НСНО + Н2О,
НСНО ® Н2 + СО.
Далее водород и оксид углерода сгорают по своим цепным механизмам.
В отсутствии кислорода идет термическая диссоциация метана с образованием в конечном итоге сажистого углерода
СН4 = 2Н2 + С.
Дата добавления: 2015-05-13; просмотров: 2564;
