Влияние давления на скорость реакции
Концентрации реагирующих компонентов зависят от давлений прямопропорционально:
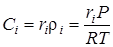 , (3.4)
, (3.4)
где ri – объемная доля реагирующего вещества в смеси;
Р – давление, Па;
R = 8314/m - газовая постоянная данного газа, Дж/(кг×К).
Учитывая, что скорость реакции горения W пропорциональна концентрации реагирующих веществ, получим:
- для мономолекулярной реакции (Н2О = Н2 + 0,5О2) скорость реакции пропорциональна давлению
W~P ,
- для бимолекулярной реакции (CO + H2O = CO2 + H2) скорость пропорциональна квадрату давления
W~P2,
- для тримолекулярной реакции (СН4 + 2О2 = СО2 + 2Н2О) скорость пропорциональная кубу давления
W~P3.
Следовательно: скорость реакции пропорциональна давлению в степени, равной порядку реакции ν, который представляет собой сумму стехиометрических коэффициентов исходных веществ в уравнении реакции (ν=1, ν=2, ν=3 и т.д.).
Дата добавления: 2015-05-13; просмотров: 1231;
