Факторы, влияющие на скорость химических реакций
Основные факторы, влияющие на скорость химических реакций, - это концентрация реагирующих веществ, температура, наличие катализатора.
Концентрация. Увеличение концентрации взаимодействующих веществ – один из самых распространенных приемов интенсификации процессов. Зависимость скорости химических реакций от концентрации определяется законом действия масс. Согласно этому закону скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ в степени, равной стехиометрическому коэффициенту, стоящему перед формулой вещества в уравнении реакции. Например, в производстве патоки для реакции нейтрализации хлороводородной кислоты карбонатом натрия скорость может быть вычислена по уравнению:
2НСI + Na2CO3 = 2NaCI + H2O + CO2
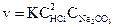
Закон действия масс в общем виде:
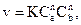
где К – коэффициент пропорциональности, который иначе называется константой скорости реакции; Ca и Cb – концентрация вещества a и b, участвующих в химической реакции; n и m - стехиометрические коэффициенты.
Если принять, что Ca и Cb = 1, то v = К, т.е. константа скорости реакции численно равна скорости реакции при концентрации реагирующих веществ, равной единице. Константа скорости зависит от природы реагирующих веществ, температуры, наличия катализатора и не зависит от концентрации веществ, участвующих в химической реакции. Константа скорости реакции при данной скорости и температуре постоянна.
Для определения констант скорости реакции в зависимости от молекулярности и порядка реакции выведены соответствующие формулы.
Молекулярность реакции определяется числом молекул, участвующих в элементарном акте химического взаимодействия. Если для этого требуется одна молекула, то реакции называются мономолекулярными. Примером такой реакции может служить реакция разложения CaCO3 под действием высокой температуры при обжиге известняка в печах на свеклосахарных заводах:
CaCO3 = CaO + CO2
Реакции при участии двух молекул называются бимолекулярными, трех - тримолекулярными. Это могут быть молекулы одного или разных веществ. Реакция взаимодействия хлороводородной кислоты с карбонатом натрия, приведенная выше, является три-молекулярной.
Порядок реакции - это сумма показателей степеней при концентрациях веществ в уравнении закона действия масс. Скорость реакции первого порядка пропорциональна концентрации в первой степени, скорости реакций второго и третьего порядков пропорциональны соответственно концентрациям во второй и третьей степени. Однако порядок реакции может быть ниже ее молекулярности, если какое-либо вещество находится в избытке и поэтому его концентрацию можно практически считать неизменной.
Температура - важный фактор, определяющий скорость реакции. С повышением температуры скорость реакции возрастает, что связано с увеличением константы скорости реакции. Согласно правилу Вант-Гоффа, повышение температуры на 100С увеличивает скорость реакции в 2-4 раза (в среднем в 3 раза). Это правило приближенно и применимо к реакциям, протекающим в области температур от 0 до 3000С и в небольшом температурном интервале.
Характер влияния температуры и концентрации реагирующих веществ на скорость химических реакций можно объяснить теорией активных столкновений. Согласно этой теории химическое взаимодействие между молекулами возможно только при их столкновении, однако к химическим реакциям приводят эффективные столкновения, т.е. в реакцию вступают не все сталкивающиеся молекулы, а только те молекулы, которые обладают определенной энергией, избыточной по сравнению со средней. Молекулы, обладающие такой энергией, называются активными. Избыточная энергия молекул называется энергией активации и зависит от природы вступающих в реакцию веществ.
Для протекания химических реакций необходимо разорвать внутримолекулярные связи в молекулах реагирующих веществ. Если сталкивающиеся молекулы обладают большой энергией и ее достаточно для разрыва связей, то реакция пойдет; если энергия молекул меньше необходимой, то столкновение будет неэффективным и реакция не пойдет.
При повышении температуры количество активных молекул увеличивается, число столкновений между ними возрастает, в результате чего растет скорость реакции. С увеличением концентрации реагирующих веществ общее число столкновений, в том числе эффективных, также возрастает, в результате увеличивается скорость реакции.
Катализатор - это вещество, которое резко изменяет скорость реакции. В присутствии катализаторов реакции ускоряются в тысячи раз, могут протекать при более низких температурах, что экономически выгодно. Велико значение катализаторов в органическом синтезе - в процессах окисления, гидрирования, дегидрирования, гидратации и др. Чем активнее катализатор, тем быстрее идут каталитические реакции. Катализаторы могут ускорять одну реакцию, группу реакций или реакции разных типов, т.е. они обладают индивидуальной или групповой специфичностью, а некоторые из них пригодны для многих реакций. Например, ионы водорода ускоряют реакции гидролиза белков, крахмала и других соединений.
Существуют каталитические реакции, в которых катализатором является один из промежуточных или конечных продуктов реакции. Эти реакции идут с малой скоростью в начальный период и с возрастающей - в последующий.
Катализаторами служат преимущественно металлы в чистом виде (никель, кобальт, железо, платина) и в виде оксидов или солей (соединения железа, магния, кальция, меди и т.п.). Неорганические катализаторы термостабильны и реакции с ними протекают при сравнительно высоких температурах.
Наличие посторонних веществ в среде, где протекает реакция, влияет на катализатор по-разному: одни нейтральны, другие усиливают действие катализатора, третьи его ослабляют или подавляют. Вещества, отравляющие катализатор, называются каталитическими ядами.
В зависимости от того, находится катализатор в той же фазе, что и реагирующие вещества, будучи равномерно распределенным в реакционной среде, или образует самостоятельную фазу, говорят о гомогенном или гетерогенном катализе. В гетерогенном катализе реагирующие вещества, как правило, находятся в жидком или газообразном состоянии, а катализатор - в твердом, при этом реакция протекает на границе двух фаз, т.е. на поверхности твердого катализатора. Например, каталитическая реакция гидрирования жиров трехфазная: катализатор (металлический никель) образует твердую фазу, водород - газообразную, а жир - жидкую. Поэтому в данном случае речь идет о гетерогенном катализе.
При гетерогенном катализе большое значение имеют способ получения катализатора, условия проведения процесса, состав примесей и т.д. Катализаторы должны обладать значительной селективностью, активностью и сохранять эти свойства длительное время.
Для того, чтобы объяснить механизм гомогенного катализа, пользуются теорией промежуточных соединений. При внесении катализатора реакция проходит через несколько промежуточных стадий, требующих меньшей энергии активации, чем прямая реакция без катализатора, что приводит к колоссальному возрастанию скорости реакции.
Медленный процесс, например, реакция
А + В = АВ,
в присутствии катализатора К протекает в две стадии:
А + К = АК (промежуточное соединение);
АК + В = АВ + К.
Каждая из этих стадий идет с малой энергией активации и, следовательно, с большой скоростью. Катализатор образует промежуточное соединение, которое при взаимодействии с другим веществом регенерирует катализатор.
Многие гомогенные реакции катализируются действием ионов Н+ и ОН-. К таким реакциям относятся инверсия сахарозы, гидролиз сложных эфиров, в том числе жиров. Ионы металлов катализируют реакции окисления, гидролиза. Например, медь катализирует окисление аскорбиновой кислоты, поэтому оборудование для переработки плодов и овощей нельзя изготавливать из меди и ее сплавов. Окисление пищевых жиров ускоряется под действием ионов меди, железа, марганца, поэтому жиры нельзя хранить в металлической таре.
Основным недостатком гомогенного катализа является трудность выделения катализатора из конечной смеси (жидкости или газа), в результате чего часть его безвозвратно теряется, а продукт загрязняется им. Гетерогенный катализ не страдает этим недостатком, что служит одной из важнейших причин его большого распространения в промышленности. Этот вид катализа сопровождается образованием промежуточных соединений. Они формируются на отдельных участках поверхности катализатора в так называемых активных центрах, занимающих небольшую часть его поверхности. Если активные центры блокировать, например, каталитическими ядами, то катализатор теряет свою активность. Для увеличения поверхности и, следовательно, количества активных центров катализатора его измельчают. Чтобы катализатор не уносился током газа, его наносят на инертный носитель с развитой поверхностью (силикагель, асбест, пемзу и т.п.).
Большинство каталитических реакций положительно, т.е. в присутствии катализатора их скорость возрастает. Однако встречается отрицательный катализ, когда катализатор замедляет скорость реакции. В данном случае катализатор называют ингибитором. Если ингибитор тормозит процесс окисления, его называют антиокислителем или антиоксидантом.
Дата добавления: 2015-05-05; просмотров: 2945;
