Виконання роботи. На рис. 7 зображена схема установки для кулонометричного титрування.
На рис. 7 зображена схема установки для кулонометричного титрування.
Установку готують до роботи згідно з інструкцією до неї.

| 1- джерело пост. ел-ного струму; 2- вимірюючий пристрій; 3- стакан для електролізу: 4- допоміжна камера; 5- катод (Pt); 6- анод у вигляді сітки (Pt); 7- скляна перегородка; 8- магнітна мішалка. |
| Рис. 7. Схема установки для кулонометричного титрування |
В стакан для електролізу місткістю 150 мл (анодний простір) вносять певний об’єм розчину натрій тіосульфату, 10 мл 0,1 М розчину КІ, 30 мл 0,15 М розчину Na2SO4, 30 мл фосфатного буферного розчину, 3 мл розчину крохмалю і опускають магнітик для перемішування.
Циліндричний посуд з пористим дном і прикріпленим ззовні сітчастим платиновим електродом (анодом) заповнюють сумішшю Na2SO4 і фосфатного буферного розчину, взятих у співвідношенні 1:1 (достатньо 5 мл : 5 мл) та опускають в нього платиновий електрод (катод). Стакан з розчином ставлять на магнітну мішалку. В стакан занурюють посуд з пористим дном і електродами так, щоб вони не торкались магнітика, який знаходиться на дні стакана. Під’єднують електроди до клем приладу відповідно до їх полярності (анод до „+”, катод до „–”). Вмикають магнітну мішалку, встановлюють середню швидкість перемішування. Одночасно вмикають секундомір і переводять тумблер з положення „Калібр” в положення „Вимір”. Як тільки з’явиться слабке синє забарвлення розчину в стакані, вимикають секундомір і припиняють електроліз, переводячи тумблер в положення „Калібр”. Записують тривалість електролізу t1. Вимикають магнітну мішалку, виймають і промивають ззовні посудину з пористим дном і сітчастий електрод, не виливаючи з посудини розчин. Із стакана розчин виливають, промивають його і магнітик дистильованою водою.
Для виключення індикаторної похибки (час електролізу, що затрачений на виділення індикаторної кількості йоду) ведуть повторно електроліз при цій же силі струму з такими ж кількостями всіх реактивів, за винятком натрій тіосульфату. Замість натрій тіосульфату в стакан додають 10 мл дистильованої води. Проводять дослід аналогічно попередньому і записують час t2, який витрачається на ґенерування на аноді індикаторної кількості йоду. Вимикають прилад у зворотньому порядку. Вимикають магнітну мішалку, промивають дистильованою водою електроди, посудину з пористим дном і стакан.
Масу натрій тіосульфату в розчині розраховують за формулою:
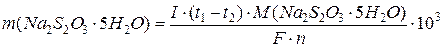 ,
,
де m ― маса натрій тіосульфату, мг; М(Na2S2O3·5 Н2О)= 248,19 г/моль; І ― сила струму, А; t1, t2 ― тривалість електролізу в присутності натрій тіосульфату і без нього, відповідно, с; F = 96500 Кл/моль; n = 1 ― число електронів; 103 ― множник для перерахунку маси з грамів у міліграми.
Дата добавления: 2015-02-28; просмотров: 1443;
