Виконання роботи. Масу наважки солі Мора беруть з такого розрахунку, щоб на титрування витрачалося ~ 6 мл 0,05 н розчину К2Сr2О7:
Масу наважки солі Мора беруть з такого розрахунку, щоб на титрування витрачалося ~ 6 мл 0,05 н розчину К2Сr2О7:
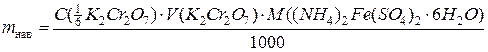 ,
,
де mнав― маса наважки солі Мора, г; С( 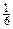 К2Сr2О7) = 0,05 н; V ― об’єм розчину К2Сr2О7 (~6 мл); М((NH4)2Fe(SO4)2·6H2O) = 392,11 (г/моль-екв) ― молярна маса екв. солі Мора.
К2Сr2О7) = 0,05 н; V ― об’єм розчину К2Сr2О7 (~6 мл); М((NH4)2Fe(SO4)2·6H2O) = 392,11 (г/моль-екв) ― молярна маса екв. солі Мора.
Розраховану наважку солі Мора зважують на аналітичних терезах, переносять у стакан, розчиняють у 20 мл Н2О, додають 20 мл Н2SO4 (1:4) і 1–2 мл 30 %-ного розчину Н3РО4.
Стакан з досліджуваним розчином ставлять на магнітну мішалку, занурюють в стакан магнітик, Рt-електрод і сполучають електролітичним ключем з насиченим каломельним електродом (НКЕ), який знаходиться в стакані. Вмикають магнітну мішалку. Електроди під’єднують до рН-метра та вимірюють значення потенціалу, як описано в інструкції до приладу.
В досліджуваний розчин приливають з мікробюретки по 1 мл розчину К2Сr2О7 і через рівні проміжки часу (1,0 або 1,5 хв) визначають значення потенціалу. Коли різниця потенціалів між наступним і попереднім визначеннями перевищить 8–10 мВ, не враховуючи різниці між початковим значенням і значенням потенціалу після першої порції титранта, добавляють його по 0,1 мл. Якщо різниця потенціалів між сусідніми визначеннями знову перевищить 8–10 мВ, титрант додають по одній краплі, точно вимірюючи об’єм бюреткою. Після досягнення точки еквівалентності (різка зміна потенціалу) додають титрант ще декілька разів по одній краплі, потім ― по 0,1 мл і, нарешті, двічі ― по 0,5 мл.
Результати визначень заносять в таблицю.
Таблиця
| V(К2Сr2О7), мл | φ, мВ | Δφ | ΔV | Δφ/ΔV |
За даними таблиці будують графіки залежності φ = ¦(V) і Δφ/ΔV = ¦(V) та знаходять точку еквівалентності.
Обчислюють масову частку феруму (ІІ) в зразку солі Мора у відсотках:
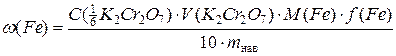 ,
,
де mнав ― маса наважки солі Мора, г; М(Fе) ― 55,84, г/моль; f(Fe)=1; С( 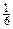 К2Сr2О7) = 0,05 н; V(К2Сr2O7) ― об’єм титранту, мл.
К2Сr2О7) = 0,05 н; V(К2Сr2O7) ― об’єм титранту, мл.
Дата добавления: 2015-02-28; просмотров: 1410;
