НАРУШЕНИЯ ЖИРОВОГО ОБМЕНА
Липиды являются важнейшим источником энергии, поступающей в организм. Их калорийность почти в 2 раза выше калорийности углеводов и белков. Сейчас установлено, что роль жира не граничивается поставкой энергии животному организму. В составе липидов находятся полиненасыщенные жирные кислоты, не синтезируемые в организме. Они служат предшественниками простагландинов, предотвращают отложение холестерина в стенках кровеносных сосудов, поддерживают жидкое состояние билипидного слоя клеточных мембран. Эссенциальные, жизненно необходимые полиненасыщенные жирные кислоты (арахидоновая, линолевая, линоленовая) обеспечивают рост и развитие молодых животных, спермиогенез и овуляцию у взрослых животных, их продуктивность. Вместе с жирами в организм поступают жирорастворимые витамины. Липиды являются источником эндогенной воды.
Расстройство обмена жира может возникать на всех этапах его ассимиляции: при переваривании и всасывании, транспортировке, межуточном обмене, депонировании.
Нарушение переваривания и всасывания жиров. Гидролиз жиров осуществляется в полости кишки и на мембранах щеточной каймы энтероцитов. Нарушение полостного переваривания может быть обусловлено недостаточным поступлением желчи, поджелудочной и кишечной липазы. При гипохолии утилизация липидов затруднена из-за недостатка жирных кислот, необходимых для эмульгирования жиров, активации панкреатической липазы, нейтрализации кислотного содержимого, его механического перемещения. Чем менее эмульгирован жир, тем меньше площадь его контакта с энзимами. Полостное пищеварение может быть нарушено уменьшением поступления панкреатической липазы (панкреатит, механические препятствия, генетический дефицит), недостаточной активностью фермента (ахолия), его инактивацией (кислая среда).
Пристеночное переваривание осуществляется преимущественно в проксимальном отделе тонкой кишки под влиянием моноглицеридлипазы, с ее же участием в присутствии желчных кислот и моноглицеридов образуются всасывающиеся мицеллы. Поэтому недостаточность трансмембранного переноса липидов чаще всего вызвана гипо- или ахолией, нарушением структуры желчных кислот, избытком кальция в корме. Кальциевые соли жирных кислот плохо подвергаются метаболизации.
Поступивший в энтероциты жир подвергается ресинтезу, включается в состав хиломикронов (триглицериды, фосфатиды, холестерин, белок). Нарушение этой фазы всасывания может быть обусловлено подавлением функциональной активности энтероцитов при авитаминозах, особенно нехватке ретинола, кобаламина; энтеритах; дисбактериозе; токсикозах. Завершается всасывание поступлением в лимфу хиломикронов и тонко эмульгированных моноглицеридов, а в кровь — жирных кислот с короткой цепью (у жвачных — уксусная, пропионовая, масляная). У птиц липиды сразу поступают через портальную систему в печень и общий кровоток.
Нарушение переваривания и всасывания сопровождается потерей жира, его выделением с фекальными массами. Хронизация патологии ведет к жировому и витаминному голоданию, кахексии.
Дефицит эссенциальных жирных кислот у моногастричных животных тормозит рост и развитие молодняка; приводит к нарушению состава липидов клеточных мембран, синтеза простагландинов, дистрофическим изменениям внутренних органов, кожных покровов. Жвачные животные не испытывают дефицита высоконепредельных жирных кислот.
Всосавшийся и ресинтезированный жир в виде хиломикронов (99 % триглицеридов, 1 % белка) через лимфатические сосуды, грудной лимфатический проток поступают в большой круг кровообращения. Часть из них депонируется легкими. Легкие обладают способностью регулировать поступление жира в артериальную кровь. Функциональное состояние легких влияет на липемию. Ускорение тока крови приводит к гиперлипемии, повышенному отложению липидов в жировую ткань. Ограничение дыхательной поверхности легких (ателектаз) сопровождается задержкой хиломикронов легочной тканью.
Общее содержание липидов в крови зависит от их поступления извне, уровня потребления тканями и мобилизации из печени и жировых депо.
После приема корма содержание жира в крови начинает повышаться и к 6—7-му часу достигает максимальных величин. Возникает алиментарная гиперлипемия, ее выраженность и продолжительность зависят от состава кормового жира, его количества, переваривания, всасывания, поступления в жировые депо и участия в межуточном обмене. Возможна транспортная гиперлипемия, если повышается потребность использования жира как источника энергии. Мобилизация жира стимулируется симпатикоадреналовой системой, повышенным выбросом катехоламинов. Жир транспортируется в виде неэстерифицированных жирных кислот (НЭЖК) и липопротеидов, к которым относятся хил омикроны, содержащие пищевые триглицериды, липопротеиды очень низкой плотности (ЛОНП); в их составе эндогенные триглицериды, липопротеиды низкой плотности (ЛНП) и липопротеиды высокой плотности (ЛВП). Основные липидные компоненты последних представлены эндогенными эфирами холестерина. Жирные кислоты хиломикрона могут использовать любые ткани, имеющие активную, стимулированную гепарином липопротеидлипазу (фактор просветления). Липопротеидлипаза эндотелиоцитов кровеносных сосудов, находящаяся в связанном состоянии, активируется также гепарином. Его недостаточность (гепатит, гепатоз, цирроз) способствует отложению хиломикронов в неизмененном виде. ЛОНП переносят к тканям триглицериды, синтезируемые печенью. ЛНП (бета-липопро-теиды) переносят холестерин плазмы в различные ткани, стенки кровеносных сосудов. ЛВП (альфа-липопротеиды) транспортируют холестерин из тканей и из стенок сосудов. Нарушение соотношений этих фракций липопротеидов является одной из причин расстройств обмена холестерина. Гиперхолестеринемия — важнейший фактор риска атеросклероза. Возникает как результат недостатка в плазме крови липопротеидов высокой плотности, длительного избыточного поступления холестерина с кормами, торможения расщепления эфиров холестерина, нарушения процессов его этерификации. Гиперхолестеринемию наблюдают при болезнях печени, нарушениях обмена веществ, лихорадочных состояниях.
Нарушение межуточного обмена жира. Основой межуточного обмена жира являются такие процессы, как липолиз триглицеридов с освобождением жирных кислот, биосинтез липопротеидов, фосфатидов, триглицеридов, жирных кислот. Высшие жирные» кислоты представляют основной субстрат межуточного обмена, иэд уровень неизменно поддерживается за счет липопротеидов и триглицеридов жировых депо. Путем последовательного бета-окисления жирных кислот с образованием ацетилкоэнзима А (ацетил-КоА) молекулы жирных кислот укорачиваются до тех пор, пока вся цепь не распадется до ацетил-КоА. Он поступает в цикл Кребса и подвергается окислению до воды и диоксида углерода. Часть ацетил-КоА превращается в печени в кетоновые тела или используется для ресинтеза жира.
У здорового крупного рогатого скота в крови содержится 1 — 6 мг/100 мл кетоновых тел, у овец — 3—7 мг/100 мл.
Наиболее значимым для состояния здоровья животных нарушением является образование избытка кетоновых тел в крови — кетоз. Содержание кетоновых тел зависит от уровня поступления в организм углеводов, количества жирных кислот, поступающих в печень, активности их ресинтеза, интенсивности окисления ацетил-КоА в цикле трикарбоновых кислот.
Углеводное голодание, характеризующееся низким (0,2—0,6 : 1) относительно оптимального (1—1,5 : 1) сахаро-протеиновым соотношением в рационе дойных коров, сопровождается сниженным образованием щавелевоуксусной кислоты в гепатоцитах. Она не связывает ацетил-КоА для включения в цикл Кребса. Ацетил-КоА конденсируется в ацетоацетил-КоА, который путем гидролиза превращается в ацетоуксусную кислоту. Часть ее декарбоксилируется в ацетон, часть под влиянием дегидрогеназы трансформируется в бета-оксимасляную кислоту.
Избыточно образованные кетоновые тела (ацетон, ацетоуксусная и бета-оксимасляная кислоты) вызывают тяжелое заболевание — кетоз.
Увеличение кетоновых тел (гиперкетонемию) наблюдают не только при углеводном голодании. Гиперкетонемию выявляют при голодании, сахарном диабете, тиреотоксикозе, тяжелых заболеваниях, сопровождающихся расстройствами окислительных процессов в организме, усиленным распадом липидов, жировой инфильтрации печени (гепатозе). Наиболее часто кетозом болеют высокопродуктивные коровы. Выделяют кетозы первичного (кетоз молочных коров) и вторичного происхождений, наблюдаемые у животных при атониях, переполнении рубца, родильном парезе, эндометритах, гепатозах, кормовых отравлениях.
Гиперкетонемия сопровождается токсикозом, нарушением функции центральной нервной системы. Развиваются дистрофические процессы в печени, сердце, почках, поджелудочной железе, яичниках. Кетоновые тела появляются в моче (кетонурия), молоке (кетонолактия), выдыхаемом воздухе. Содержание кетоновых тел в крови и молоке возрастает до 40 мг/100 мл и более, а в моче — до 500 мг/100 мл. Количество же сахара (глюкозы) в крови падает с 40—70 мг/100 мл до 30—18 мг/100 мл.
У заболевших кетозом коров снижается молочная продуктивность, что нередко является причиной их выбраковки.
Кроме кетоза нарушение межуточного обмена жира может проявиться накоплением продуктов перекисного окисления. Интенсивное окисление ненасыщенных жирных кислот по перекисному механизму, вызванному недостатком токоферолов, селена, отравлением СН4, гипероксией, ионизирующим излучением, ведет к накоплению метаболитов, обладающих высокой биологической активностью. Продукты перекисного окисления липидов интенсивно образуются и накапливаются, если ингибированы антиоксидантные системы. Перекисям жиров придают большое значение в патогенезе многих заболеваний.
Нарушение депонирования жира. Нарушение содержания депонированного жира определяется либо как повышенная инфильтрация жира в ткани с последующим ожирением, либо как усиленный липолиз.
Под жировой инфильтрацией понимают длительное повышение содержания липидов в тканях (кроме жировой), когда триглицериды не подвергаются расщеплению, окислению или выведению.
Ожирение представляет собой результат усиленного поступления липидов в жировую ткань и недостаточной утилизации их как источника энергии. Усиленное отложение жира определяется следующими патогенетическими факторами:
ξ повышенной калорийностью рациона, превосходящей энергетические потребности организма. Ожирение алиментарного происхождения наблюдают при повышенной возбудимости пищевого центра (булимия с полифагией), избыточном поступлении высококалорийных кормов в сочетании с недостаточной мышечной нагрузкой (адинамией);
ξ уменьшением использования депонированного жира для энергетических целей. Мобилизация этого источника энергии находится под контролем нервной и эндокринной систем. Торможение симпатического влияния, ингибиция активности эндокринных желез, секретирующих гормоны, способствующие липолизу (тироксин, СТГ, ТТГ, тестостерон), приведут к ожирению. Повышенный выброс инсулина, тормозящего липолиз, также приведет к накоплению жира в жировых депо;
ξ избыточным синтезом липидов из углеводов. Метаболическое ожирение обязано интенсивному переходу пируват-ацетил-КоА в жирные кислоты. Стимулируется некоторыми гормонами (пролактин). Патология может быть наследственно обусловленной;
ξ генетическими аномалиями, описанным у коров липоматозом. Липомы различного размера и места расположения выявляют у айрширских коров, голштино-фризов, других пород. Липомы увеличиваются с возрастом и могут достигать размеров 23 х 20 х 5 см.
У больных животных отмечают характерные признаки нарушения липидного, белкового и углеводного обменов. В крови выявляют повышение концентрации общих липидов, холестерина, фосфолипидов, триглицеридов, бета-липопротеидов, НЭЖК. Снижены окислительные процессы, тормозится липолиз.
Ожирение животных сочетается с жировой инфильтрацией и жировой дистрофией печени (рис. 17). Содержание жира в сухом веществе органа может достигать 20—30 % и более, тогда как у здоровых животных оно колеблется в пределах 8—12 %. Нарушаются все функции печени, снижаются желчеобразование и желчевыведение.
Ожирение коров служит предрасполагающим фактором для заболевания кетозом. Такие животные заболевают гораздо чаще, чем коровы средней упитанности. У ожиревших животных снижается половая потенция, задерживается созревание яйцеклеток, нарушается половой цикл, коровы часто остаются бесплодными. Телята, ягнята, поросята, щенки от ожиревших матерей рождаются ослабленными, физиологически неполноценными, склонными к заболеваниям.
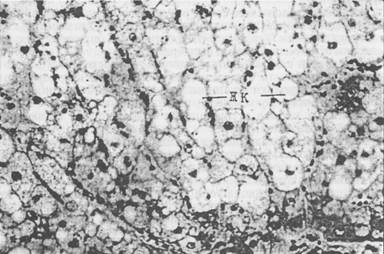
Рис. 17. Жировая дистрофия печени коровы. Накопление жира в гепатоцитах с образованием жировых кист (ЖК). Ув. 220 (по Байматову, 1999).
В противоположность ожирению возможно усиление процессов липолиза. Оно наблюдается при сахарном диабете вследствие недостатка инсулина, при голодании, эмоциональном стрессе, гипотермии, повышенной физической нагрузке, стимуляции симпатических нервов, иннервирующих жировую ткань, при усиленном выбросе мозговым слоем надпочечников катехоламинов (адреналин, норадреналин, дофамин). Липолитический эффект усиливают и другие гормоны, повышая аденилатциклазную активность: АКТГ, СТГ, ТТГ, тироксин, тестостерон, глюкагон.
Освобождающиеся за счет усиленного липолиза жирные кислоты поступают в кровь и используются для обеспечения повышенных потребностей мышечной и других тканей в энергии.
Дата добавления: 2015-02-10; просмотров: 4241;
