Денатурация глобулярных белков
Денатурацию глобулярных белков вызывают: нагревание, воздействие ультразвуком, радиационное воздействие, рН, состав растворителя.
Экспериментально было показано, что денатурацию вызывают слабополярные органические растворители. Их действие связано с контактами с гидрофобными группами белка. Было обнаружено, что денатурирующее действие спиртов на белки возрастает с увеличением размера алифатического радикала.
Глобула имеет фиксированную пространственную структуру и переход “глобула клубок” отличен от перехода “спираль - клубок” потому, что он происходит в трехмерной системе. С другой стороны, кооперативность перехода (которая определяет величину изменения температуры (интервал ΔT, в котором происходит переход), а ΔT примерно одинаково при плавлении α-спирали и глобулярного белка) связана не только с взаимодействием ближнего порядка, но и дальнего. Показательны денатурационные превращения в зависимости от рН. При уменьшении рН уменьшается изменение энтальпии и температура перехода.
Например, для химотрипсиногена:
| рН | Тm, 0С | ΔН, ккал/моль |
| 2.3 | ||
| 2.8 | ||
| 3.4 | ||
| 5.0 |
Конформационные переходы белковых молекул связаны с разворачиванием полипептидной цепи и часто происходят малые, локальные и трудно наблюдаемые изменения, которые не сопровождаются сильными изменениями теплоемкости. Когда изменения теплоемкости при денатурации нативных белков велики, их связывают с нарушением гидрофобных взаимодействий. По существенным изменениям теплоемкости можно судить о характере перехода. Т.к. при денатурации глобулярных белков изменяется структура молекулы, то исследования могут способствовать установлению факторов, стабилизирующих белковую глобулу.
Факторы:
1) В ходе денатурации белки характеризуются большей поворотной гибкостью цепи, и поэтому среднее изменение энтропии Δ 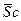 является первой существенной составляющей свободной энергии для дестабилизации глобулярных белков. В расчете на стабильный (развернутый) остаток Δ
является первой существенной составляющей свободной энергии для дестабилизации глобулярных белков. В расчете на стабильный (развернутый) остаток Δ 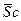
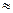 2-6
2-6 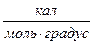 .
.
2) Изменение энтальпии Δ 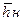 (связано с разрушением водородных связей). Δ
(связано с разрушением водородных связей). Δ 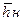
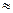 2
2 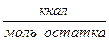 .
.
3) Изменение свободной энергии Δ 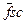 при нарушении гидрофобного взаимодействия в ходе денатурации.
при нарушении гидрофобного взаимодействия в ходе денатурации.
4) Реакции денатурации белка сильно зависят от рН. Факторы, определяющие эту зависимость, делят на две группы:
а) дальнодействие электростатического взаимодействия;
б) аномальные группы и эффекты, связанные с титрованием.
Многие белки содержат ионизированные группы, рК которых отличаются на несколько единиц от нормального значения рК для этих групп в развёрнутом состоянии. В ходе денатурации происходит нормализация рК этих групп, т.е. изменяется связывание протонов с этими группами. Это приводит к появлению титрационной составляющей изменения свободной энергии (ΔFтитр.).
ΔFg = p(N 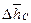 - NT Δ
- NT Δ 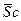 +
+ 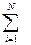 Δ
Δ 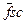 i) + ΔFэл + ΔFтитр..
i) + ΔFэл + ΔFтитр..
р – доля пептидной цепи, развернутой в ходе денатурации, или степень разворачивания.
N – число звеньев в молекуле.
Дата добавления: 2015-02-07; просмотров: 1687;
