МИОГЛОБИН
Миоглобин - сложный белок третьего уровня структурной организации. Состоит из одной полипептидной цепи (153 остатка). Третичная структура белка образована, главным образом, альфа-спиралями вторичной структуры, на которые приходится около 70 процентов АКО, остальные - на повороты и начальный и конечный участки. Белок содержит в себе так называемый ГЕМ- комплекс порфирина и иона железа в степени окисления +2.

Ион железа встроен в кольцо порфирина таким образом, что четыре координационные связи из шести затрачены на образование связей с атомами азота, еще одна связана с азотом имидазольного остатка ГИС полипептидной цепи (проксимальный Гистидин F8), а другая - также с имидазольным остатком другого ГИС (дистальный ГИС Е7). Молекула кислорода присоединяется между остатком дистального ГИС и железом. Изменения степени окисления железа при этом не происходит. Порфириновое кольцо (ГЕМ) частично погружено в молекулу белка. Молекула кислорода присоединяется к нему, входя как бы через открывающуюся дверцу. Пока остается неясным, дожидается молекула кислорода случайного открывания двери, или существует какой-то механизм, пропускающий кислород к нему.
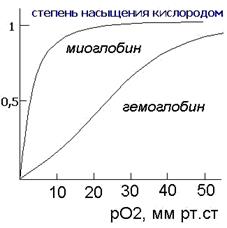
Миоглобин сосредоточен, главным образом, в мышцах и его главной функцией является хранение кислорода. Скорость насыщения миоглобина кислородом намного превышает таковую для гемоглобина. Миоглобин мало приспособлен для транспортировки кислорода из легких в ткани, поскольку скорость отдачи кислорода в тканях невелика (при давлении 1 мм рт. ст. примерно половина миоглобина все еще не отдает кислород).
Вопросы транспортировки кислорода решаются при участии гемоглобина.
Дата добавления: 2015-02-07; просмотров: 1190;
