Глава 3. Физика белка.
3.1. Общая характеристика белков
Белки - это сложные макромолекулярные структуры, нерегулярные полимеры, построенные из остатков аминокислот. В общем виде, в водном растворе при нейтральном рН, аминокислоты имеют вид типа:
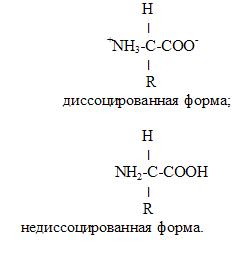
Их структура и структура надмолекулярных комплексов определяется ковалентными химическими связями и слабыми взаимодействиями.
Нативные белки никогда не являются статистическими клубками. Физики их считают апериодическими кристаллами сложной структуры. Их поведение зависит от положения и свойств всех элементов молекул, т.е. существенно зависит от той конформации, в которой находится белковая молекула. В организме человека ~105 видов белков. Это странно, т.к. число генов приблизительно несколько десятков тысяч (один белок кодируется одним геном).
Изучая химический состав белков, мы узнаем, из каких химических элементов они состоят. Анализ показал: во всех белках примерно 50-55% углерода, 21-23% кислорода, 15-17% азота, 6-7% водорода, 0.3-2.5% серы. В составе больших белков обнаружены: фосфор, йод, железо и др. макро- и микроэлементы в разных количествах. Содержание основных химических элементов белка может различаться за исключением азота, т.к. концентрация азота постоянна и равна примерно 16%. Содержание азота в других органических веществах мало, поэтому предложили определять количество белка по входящему в его состав азоту. Зная, что 1г азота содержится в 6.25г белка, найденное количество азота умножают на 6.25.
Для определения химической природы белка, его разделяют на мономеры и выясняют их химический состав. Расщепление белка на составные части производят с помощью гидролиза (кислотного или щелочного). Кислотный гидролиз – это длительное кипячение белка с сильными кислотами. Чаще всего кипятят белок с HCL при 100ºС в течение 24 часов.
2-ой этап: хроматография – это разделение веществ, входящих в состав гидролизата. Аминокислотный состав определяют с помощью анализа радикалов (гораздо сложнее определить их последовательность).
Функционирование белка связано с определенной конформацией. Нарушение в одном звене молекулы белка обязательно приведет к изменению её конформации. Денатурация – это необратимое разрушение белка. Ренатурация - это восстановление белка.
Задачи физики белков.
1) изучение структуры белка и надмолекулярных комплексов.
2) исследование динамического поведения белков (в том числе изучение денатурации).
3) установление связи между первичной структурой и структурами белков более высокого порядка.
4) изучение взаимодействия белков с нуклеиновыми кислотами.
5) изучение физики возникновения и эволюции белков.
6) изучение физических аспектов белковой изомерии.
7) изучение методов получения белков с заданными свойствами
8) изучение физических механизмов, лежащих в основе различных биологических функций.
Дата добавления: 2015-02-07; просмотров: 1847;
