Контроль правильности измерений концентрации
Химический анализ отличается от целого ряда других видов измерений тем, что измерение концентрации представляет собой только один из этапов количественного анализа. В связи с этим для обеспечения достоверности результатов химического анализа большое значение приобретает контроль и устранение влияния неслучайных факторов, проявляющихся на этапах пробоотбора и пробоподготовки. Наличие таких факторов приводит к отклонениям результатов анализа от истинных, т. е. к появлению так называемых систематических погрешностей. Устранение систематических погрешностей в данном случае осуществляется, как правило, внесением соответствующих изменений в методики пробоотбора или пробоподготовки, значительно реже путем введения соответствующих поправок. Поэтому в отличие от подхода к получению достоверных результатов измерений, основанного прежде всего на учете и введении поправок, который имеет преимущества, когда речь идет уже об обработке результатов измерений, при рассмотрении вопросов обеспечения достоверности результатов химического анализа целесообразен подход, использующий понятие систематических погрешностей. С учетом этого систематические погрешности результата анализа можно разделить на две группы:
1) систематические погрешности, обусловленные собственно измерениями;
2) систематические погрешности, обусловленные этапами пробоотбора и пробоподготовки.
Рассмотрим систематические погрешности первой группы. Из-за влияния матрицы контроль правильности измерения концентрации не может быть ограничен этапом разработки методики, а должен проводиться постоянно непосредственно при проведении рабочих измерений.
Систематические погрешности, возникающие при измерениях, в свою очередь, можно разделить на две группы:
постоянные (аддитивные) и пропорциональные (мультипликативные) . Соответственно различают и два вида поправок:
аддитивные и мультипликативные.
Наличие отличающихся терминов для поправок каждой из этих двух групп обусловлено тем, что в наименованиях этих поправок отражены их качественные особенности.
Так, обозначение поправки как аддитивной призвано подчеркнуть, что этот вид поправки имеет ту же размерность что и измеряемая величина. Следовательно, они могут быть непосредственно учтены путем алгебраического сложения. Вместе с тем, этот же вид поправок характеризуется своим постоянством в процессе измерения и не зависит от величины измеряемого физического свойства.
Другой вид поправок, наоборот, характеризуется своей зависимостью от величины измеряемого физического свойства. Поэтому они получили обозначение как пропорциональные. В то же время именно эта особенность является причиной того, что для внесения соответствующих поправок они должны быть представлены в виде поправочного множителя, умножаемого на значение измеренного физического свойства. Отсюда следует как их обозначение в виде мультипликативных, так и отсутствие у данного вида поправок размерности.
Особенности каждой из поправок нагляднее всего проявляются на градуировочных характеристиках, что можно проиллюстрировать рис. 152.
 Суммарную поправку (Qå) можно представить в виде:
Суммарную поправку (Qå) можно представить в виде:
Qå=Qa+Qm 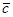
где 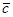 — среднее арифметическое значение концентрации;
— среднее арифметическое значение концентрации;
Qa — аддитивная поправка;
Qм — мультипликативная поправка.
Способы введения поправок, обусловленных влиянием неслучайных факторов на этапе измерений при проведении химического анализа, не отличаются существенно от способов учета аналогичных поправок, рассмотренных в предыдущих разделах (см. разд. 2.3.2). Поэтому ограничимся рассмотрением только некоторых дополнительных положений.
Сопоставление результатов, полученных принципиально разными методами анализа, часто рассматривают как способ контроля правильности не только измерения концентрации, но и результата анализа. Такой способ оправдывает себя только в том случае, если разные методы анализа имеют и разные систематические погрешности. Совпадение результатов анализа, полученных разными методами, означает тогда, что эти систематические погрешности малы. Как правило, среднее значение результатов, полученных разными методами, принимают в качестве наиболее достоверного. В то же время опыт показывает, что не существует лучшего метода анализа. Каждый метод имеет свои оптимальные границы. Склонность к завышению или занижению результатов анализа определяется не только самим методом анализа, но зависит и от состава анализируемой смеси. В каждом конкретном случае лучшим методом анализа является один. Поэтому усреднение результатов, полученных разными методами, в общем случае не увеличивает достоверность анализа.
Для контроля правильности можно использовать и такое косвенное доказательство, как соответствие результатов анализа физическим свойствам материалов
Дата добавления: 2015-02-05; просмотров: 1407;
