Как изменяется скорость химической реакции в зависимости от температуры, давления, природных катализаторов, концентрации
Известно, что одни химические реакции протекают за малые доли секунды, другие же — за минуты, часы, дни. Например, практически мгновенно протекают реакции, которые сопровождаются взрывным эффектом: горение пороха, воспламенение горючей смеси в двигателе внутреннего сгорания автомобиля. При сливании растворов хлорида бария и серной кислоты мгновенно образуется белый осадок сульфата бария:
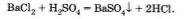
Наоборот, реакция ржавления железа (коррозия) идет так медленно, что проследить за ее результатами можно лишь по истечении длительного времени.
Одна и та же реакция может в одних условиях протекать быстро, а в других — медленно. Например, процесс окисления серебра или меди на воздухе тянется годами, а в присутствии озона проходит чрезвычайно быстро. Чтобы характеризовать быстроту течения химической реакции, пользуются понятием скорость химической реакции, которая обозначается латинской буквой v.
Скорость химической реакции определяется изменением концентрации одного из реагирующих веществ или одного из продуктов реакции в единицу времени.
Запишем формулу, по которой можно найтн скорость реакции:
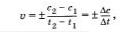
где с2 и с1 — молярные концентрации реагирующих или образующихся веществ, соответственно, в момент времени t2, t1. Если скорость реакции характеризуют изменением молярной концентрации исходных (реагарующих) веществ, то t2>t1, а с2<с1 (концентрация исходного вещества убывает по мере протекания реакции). Так как скорость реакции имеет положительное значение, перед дробью следует поставить знак минус.
Количество вещества в единице объема называется его молярной концентрацией. Она измеряется в моль/л. Так как время измеряется в секундах (минутах, часах), то можно вывести и единицы измерения скорости химической реакции: 1 моль/л * с; 1 кмоль/м3 • мин и т. д.Следовательно, чтобы определить, с какой скоростью протекает химическая реакция, нужно знать: а) какое количество вещества образуется (для продукта реакции) или расходуется (для исходного вещества); б) за какое время это происходит и в) в каком объеме протекает реакция.
Знание скоростей химических реакций имеет очень большое практическое и научное значение. Например, в химической промышленности от скорости химической реакции зависят размеры и производительность аппаратуры, количество вырабатываемого продукта и, в конечном итоге, зарплата работников и себестоимость продукции.
Раздел химии, изучающий скорость химической реакции, называется кинетикой. Зная ее законы, человек получает возможность управлять химическими процессами, им требуемую скорость.
При рассмотрении вопросa о скорости реакции необходимо помнить, что реакции в химии делятся на гомогенные и гетерогенные.
Реакции, которые протекают в однородной среде (нет поверхности раздела реагирующих веществ), например в си газов или в растворах, называются гомогенными (от греч. голо — «равный, одинаковый»).
Гетерогенными называются реакции, которые идут между веществами в неоднородной среде (есть поверхность раздела реагирующих веществ). Например.
На поверхности соприкосновения твердого вещества и жидкости, газа и жидкости, твердого вещества и газа и т. д. (от греч. гетеро - «разный, другой»).
Данное выше определение и соответствующая ему формула скорости химической реакции справедливы для гомогенных реакций.
Если реакция гетерогенная, то она может идти только на поверхности раздела реагирующих веществ. В этом случае скорость химической реакции Будет определяться площадью поверхности соприкосновения реагирующих веществ.Следовательно, для гетерогенных реакций одним из факторов, которые определяют скорость химической реакции, является величина площади поверхности соприкосновения реагирующих веществ.
Поэтому на производстве столь часто проводятся химические реакции в "кипящем слое". Твердое вещество для этой цели мелко дробят.
Измельчают почти до состояния пыли, а затем черед него пропускают снизу второе вещество, как правило, газ. Прохождение его через мелкораздробленное первое вещество-peaгент сопровождается иллюзией кипения. Например, в «кипящем слое» осуществляется обжиг мелко измельченного серного колчедана при производстве серкой кислоты.
Дата добавления: 2015-01-10; просмотров: 1327;
