Лечение фоновых и предраковых заболеваний шейки матки
Терапия фоновых и предраковых состояний ШМ проводится в 5 этапов.
1-й этап — этиопатогенетическое лечение.
А. Антибактериальная и противовирусная терапия проводится при клинических и лабораторных признаках воспалительного процесса во влагалище и шейке матки. Особое внимание следует уделить лечению ИППП, ко-
322_________________________________________ Практическая гинекология
торое проводится в зависимости от конкретного выявленного возбудителя (глава 2.2). Б. Гормонотерапия проводится при обнаружении эктопии цилиндрического эпителия дисгормонального характера с использованием КОК. При сопутствующих гормо-нозависимых гинекологических заболеваниях (эндомет-риоз, миома матки) лечение проводится соответственно нозологической форме.
У женщин репродуктивного возраста эстроген-гес-тагенные препараты применяют с 5 по 25-й день менструального цикла с последующим семидневным перерывом:
• марвелон (дезогестрел 150 мкг, этинилэстрадиол — 30 мкг);
• логест (20 мкг этинилэстрадиола и 75 мкг гесто-дена);
• фемоден (этинилэстрадиол — 30 мкг, гестоден — 75 мкг);
• ригевидон (150 мкг левоноргестрела и 30 мкг этинилэстрадиола);
• мерсилон (дезогестрел — 150 мкг, этинилэстрадиол 20 мкг).
Гестагены назначают с 16-го по 25-й день менструального цикла:
• прогестерон 1 мл 2,5 % раствора в/м ежедневно;
• 17-ОПК1 мл 12,5 % раствор в/м однократно;
• дуфастон (дидрогестерон) по 10—20 мг в сутки;
• норэтистерон (норколут) по 0,005—0,01 г в сутки;
• прегнин по 0,02 г 2 раз/сут., сублингвально;
• оргаметрил (линестрол) по 0,005 г в сутки;
• утрожестан по 200—300 мг в сутки (1 капсула утром и 1—2 капсулы вечером через час после еды).
При возрастной дистрофии вульвы используют препараты эстриола:
• эстриол по 4—8 мг 1 раз/сут. в течение 2—3 недель, затем дозу постепенно снижают до 1—2 мг в сутки;
• овестин по 4—8 мг (4—8 таблеток) в течение 2—3 недель, затем дозу постепенно понижают до 0,25-2 мг в сутки.
Глава 7. Фоновые и предраковые заболевания__________ 323
• Эстрогены комбинируют с кортикостероидами в ви
де мазей: фторокорт (триамцинолона ацетат) по 5 г
мази тонким слоем нанести на пораженный участок,
3 раз/сут.
В. Иммуномодуляторы (см. приложение 3). Г. Десенсибилизирующие препараты:
• астемизол по 1 таб. (0,01 г) 1 раз/сут;
• тавегил (клемастин) по 1 табл. (0,001 г) 2 раза/сут.;
• авил (фенирамин) по 1 табл. (0,025 г) 2-3 раза/сут.;
• зиртек (цетиризин) по 1 табл. (0,01 г) 1 раз/сут.;
• кларитин (лоратадин) по 1 табл. (0,01 г) 1 раз/сут. Д. Витаминотерапия:
• витамин В1 по 0,002 г 3 раз/сут.;
• витамин В6 1 мл 5 % раствора в/м;
• аскорбиновая кислота по 200 мг/сут.;
• рутин по 0,02г 3 раз/сут.;
• токоферола ацетат по 1 капсуле (100 мг) 2 раз/сут.
2-й этап — коррекция нарушений биоценоза влагалища.
Проводится санация влагалища антибактериальными препаратами с последующим восстановлением его биоценоза (глава 2.3. «Кольпит»). Для устойчивого эффекта необходимо одновременно восстановить биоценоз не только влагалища, но и кишечника:
• бификол -внутрь3—5 доз 2 раз/сут.;
• лиофилизированная культура молочнокислых бактерий по 4—6 доз 2 раз/сут., в течение 3—4 недель;
• колибактерин по 2-4 дозы 3-4 раз/сут. за час до еды, 4—6 недель;
• лактовит по 1 капсуле 2 раз/сут.;
• хилак по 20—40 капель 3 раз/сут. с небольшим количеством жидкости;
• бифиформ по 1 капсуле 2 раз/сут., 15—30 дней.
3-й этап — хирургическое лечение
Включает следующие методы:
I. Локальная деструкция: диатермохирургический метод, криодеструкция, лазерная деструкция, химическая деструкция.
324 Практическая гинекология
11. Радикальное хирургическое вмешательство: эксцизия шейки матки, ампутация шейки матки, реконструктив-но-пластический метод, гистерэктомия.
1. Диатермокоагуляция — деструкция электрическим током. Может быть моноактивной (с одним электродом), биполярной (с двумя электродами, объединенными в один биполярный) и биоактивной (в растворе электролита). Различают поверхностную и глубокую (послойную) диатермокоагуля-цию. На месте воздействия электрического тока развивается язва, которая затем покрывается нормальным эпителием. Таким образом лечится псевдоэрозия и различные деформации ШМ. Операцию проводят в лютеиновую фазу цикла. После операции к ШМ прикладывают антибактериальные мази.
Показания: доброкачественные фоновые процессы без выраженной деформации и гипертрофии шейки матки.
Противопоказания: острые и подострые воспалительные заболевания женских половых органов; активный генитальный туберкулез, циклические кровянистые выделения из половых путей; доброкачественные фоновые процессы в сочетании с выраженной деформацией и гипертрофией шейки матки, особенно у женщин старше 40 лет.
Отрицательные стороны: болезненная процедура, нередко струп отпадает на 7—10-е сутки ипоявляется кровотечение; образуется рубец, по которому может идти разрыв в родах; нет материала для гистологического исследования.
2.Криодеструкция — применение низких температур, вызывающих некроз патологических тканей. Холодовой агент — жидкий азот. Существуют следующие разновидности данного метода:
♦ криокоагуляция (криоконизация);
♦ криолазеротерапия — криовоздействие (первый этап) идействие гелий-неоновым лазером через 3 дня (второй этап);
♦ комбинированная криодеструкция (криолазеротерапия и криоультразвукотерапия). Криодеструкция осуществляется в первую фазу цикла. Применяют одно-, двух-,
Глава 7. Фоновые и предраковые заболевания 325
и трехэтапное замораживание с экспозицией от 3 до 8-Ю минут.
Преимущества метода: атравматичность, бескровоность, более быстрое заживление без грубых рубцов, снижение частоты осложнений, простота использования, безопасность для больной и медперсонала, возможность применения в амбулаторных условиях.
Показания: доброкачественные патологические процессы ЦІМ (эктопия цилиндрического эпителия посттравматического характера, доброкачественная зона трансформации — законченная и незаконченная, субэпителиальный эндометри-оз); предраковые процессы ШМ (простая лейкоплакия, поля дисплазии, папиллярная зона дисплазии, предопухолевая зона трансформации); кондиломы и полипы ШМ.
Противопоказания: сопутствующие острые инфекционные заболевания; острые и подострые воспалительные заболевания внутренних половых органов; чистота влагалищной флоры III—IV степени; венерические заболевания; истинная эрозия ШМ; опухоли женских половых органов с подозрением на малигнизацию; тяжелые соматические заболевания в стадии декомпенсации.
3. Лазерная деструкция (вапоризация). Используют высокоэнергетические лазеры: углекислый, аргоновый, неоновый, рубиновый.
Преимущества метода: некротизация тканей минимальна, стеноза канала ШМ не наблюдается, а выздоровление наступает скорее, чем при других методах физической деструкции ШМ. Положительной стороной лечения лазером является отсутствие воспалительных осложнений и кровотечений. В отличие от электрокоагуляции и криодеструкции, после лечения дисплазии лазером место стыка между плоским и цилиндрическим эпителием не перемещается в канал ШМ, а остается в области эктоцервикса, что облегчает последующий эндоскопический контроль.
Показания: фоновые заболевания шейки матки (псевдоэрозия, эрозированный эктропион, распространенная форма простой лейкоплакии, эндометриоз, кондиломы, полипы, ретенционные кисты); предраковые процессы (лейкоплакия
326_________________________________________ Практическая гинекология
с атипией, эритроплакия, дисплазия I—IIIст.); прединвазив-ный рак шейки матки с локализацией на влагалищной части; рецидивирующие формы заболеваний при неэффективности консервативного лечения и других видов деструкции.
Противопоказания: острые воспалительные заболевания любой локализации; злокачественные заболевания; распространение патологического процесса до 2/3 Длины цервикаль-ного канала; патологические выделения из половых путей.
Недостатки метода: болевые ощущения при лечении лазером более выражены, частота неудач при лечении дисплазии несколько выше, чем при криодеструкции, вероятность реци-дивирования процесса достигает 20 %. Лечение лазером более сложный и дорогостоящий метод по сравнению с криодеструк-цией.
4. Химическая деструкция. Для лечения доброкачественных процессов на ШМ нерожавшим женщинам с успехом применяют солковагин — водный раствор, который содержит азотную, уксусную, щавелевую кислоты и цитрат цинка, которым обрабатывается эрозия; контроль через 3—5 дней. Если не произошло заживление, место эрозии обрабатывается повторно два раза с контролем через 4 недели. Ваготил (поликрезулен) — 36 % раствор, 2-3 раза в неделю, на три минуты приложить тампон на область эрозии, количество процедур 10-12.
5.Диатермоэлектроэксцизия (конизация) — электрохирургическое конусовидное иссечение патологически измененной ткани ШМ в виде конуса, вершина которого обращена к внутреннему зеву. Осложнения идентичны таковым при диа-термокоагуляции, однако характеризуются большей степенью выраженности. При возникновении кровотечения в момент операции накладывают лигатуры. Применяют для лечения экт-ропиона, лейкоплакии, дисплазии.
Показания: сочетание доброкачественных и/или предраковых процессов шейки матки с гипертрофией и деформацией; наличие дисплазии у больных, которым раньше проводилась деструкция шейки матки, вызвавшая смещение зоны трансформации в цервикальный канал, или же это смещение обусловлено возрастом женщины (после 40 лет); рецидивы дисплазии после электрокоагуляции, криодеструкции, лазерной вапори-
Глава 7. Фоновые и предраковые заболевания 327
зации; интрацервикальная локализация дисплазии; тяжелая форма дисплазии.
Противопоказания: воспалительные процессы женских половых органов; повреждения шейки матки, которые переходят на свод и стенки влагалища; значительная посттравматическая деформация шейки матки, распространяющаяся на свод влагалища; тяжелые соматические заболевания.
Преимущества метода: радикальное удаление патологически измененных тканей ШМ в пределах здоровых тканей, возможность тщательного гистологического исследования удаленного препарата.
Осложнения: кровотечение, нарушение менструального цикла, эндометриоз, укорочение ШМ и цервикального канала, метаплазии.
6.Ампутация ШМ (проводится при тяжелой степени дисплазии).
7.Реконструктивно-пластический метод — восстанавливает нормальное анатомическое строение ШМ, способствует сохранению менструального цикла.
8. Гистерэктомия
Показания: CIN-III с локализацией в цервикальном канале; техническая невозможность проведения электроэксцизии в связи с анатомическими особенностями; сочетание с миомой матки или опухолями яичников; рецидивы после криотерапии или лазерной терапии.
При распространении процесса на своды влагалища показана экстирпация матки с верхней 1/3 влагалища.
4-й этап — послеоперационная терапия, коррекция имеющихся нарушений
На этом этапе выполняется обработка влагалища и ШМ антисептиками и антибиотиками.
5-й этап —диспансеризация и реабилитация
(оценка общего состояния, менструальной
функции, иммунного гомеостаза)
Снимают с диспансерного учета при доброкачественных (фоновых) патологических процессах через 1—2 года после ле-
328 Практическая гинекология
чения. Для контроля проводят колыгоцервикоскопию, цитологию и бактериоскопию.
После радикального лечения предраковых процессов в обязательном порядке проводят бактериоскопический, коль-поцервикоскопический и цитологический контроль (через 1—2—6 мес. и год). Снимают с учета только после получения соответствующих результатов эндоскопического и цитологического исследований через 2 года после лечения, так как рецидивы дисплазии отмечаются преимущественно в конце 1-го и на 2-м году наблюдения.
7.1.6. Клиническая тактика ведения больных
с различными формами фоновых
и предраковых заболеваний
шейки матки
Эктопия цилиндрического эпителия посттравматического генеза
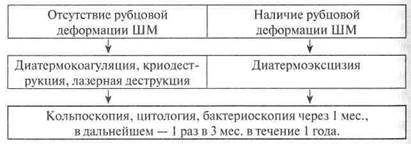
При эктопии цилиндрического эпителия дисгормонального генеза без сопутствующей гинекологической патологии назначают трехфазные оральные контрацептивы. При отсутствии эффекта показана крио- или лазерная деструкция, химическая коагуляция.
Доброкачественные полиповидные разрастания являются показанием к диагностическому выскабливанию,полипэктомии.
При экзо- и эндоцервицитах проводится этиотропная терапия (антибактериальная, антипротозойная, антимикотическая, противовирусная) в зависимости от вида возбудителя.
Глава 7. Фоновые и предраковые заболевания_______________ 329
Доброкачественная зона трансформации
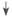
| Незаконченная зона трансформации | Законченная зона трансформации | |||
| 
| 
| ||
| Крио- или лазерная деструкция, химическая коагуляция, электрокоагуляция | Наблюдение 1 раз в год. | При размерах ретен-ционной кисты 2 см и более — диатермо-эксцизия. | ||
При дисплазии метод лечения выбирают с учетом результатов комплексного клинико-эндоскопического, цитологического, бактериоскопического, бактериологического исследований канала ШМ и морфологического исследования материала прицельной биопсии, а также показателей гормонального фона. Результаты исследований свидетельствуют о том, что диспла-зия метаплазированного эпителия, которая в виде полей, папиллярной зоны и предопухолевой трансформации определяется на фоне эндоцервикозов, обусловлена инфицированием. Поэтому лечение дисплазии метаплазированного эпителия необходимо начинать с санации влагалища и ШМ. Рекомендуется этиотропная терапия. После санации в значительной части случаев дисплазия не определяется.
При дисплазии эпителия шейки матки (CIN І-П) при отсутствии рубцовой деформации проводят крио- или лазерную деструкцию, при наличии рубцовой деформации — диатермо-конизацию.
При простой лейкоплакии проводят коррекцию гормональных нарушений; при ее неэффективности показана лазерная или криодеструкция, диатермокоагуляция.
При кондиломатозе обычно выявляют инфекцию вирусного характера (папилломавирус человека), что подтверждается наличием койлоцитарнои атипии в цервикальном мазке. Лечение должно быть комбинированным: общим (иммуномодуляторы), этиотропным и местным, направленным на деструкцию очага. Деструкцию очага можно осуществить с помощью подофилина или солкодерма, наносимых местно, а также криогенным или лазерным методом, с помощью диатермоэксцизии.
330 Практическая гинекология
Дисплазия многослойного плоского эпителия (лейкоплакия, поля и папиллярная зона трансформации) в большинстве случаев развивается на фоне гормональных нарушений (гиперпродукция эстрогенов, ановуляторный менструальный цикл, недостаточность второй фазы). Поэтому положительный эффект возможен при сочетании С02 — лазерной деструкции, криодеструкции или электроэксцизии с гормонотерапией. Доза и режим ее зависят от возраста, МЦ, сопутствующих заболеваний больной.
Преинвазивный рак шейки матки. Методом выбора является конусовидная электроэксцизия. Показания к экстирпации матки: возраст старше 50 лет; преимущественная локализация опухоли в шеечном канале; распространенный анапластичес-кий вариант с врастанием в железы; отсутствие в препарате, удаленном во время предшествующей конизации, участков, свободных от опухолевых клеток; невозможность проведения широкой эксцизии; сочетание преинвазивного рака с другими заболеваниями половых органов, требующими хирургического вмешательства; рецидив опухоли.
Микроинвазивный рак шейки матки. Методом выбора в лечении микрокарциномы является экстрафасциальная экстирпация матки, при наличии противопоказаний к оперативному вмешательству — внутриполостная у-терапия.
Инвазивный рак шейки матки:
16 стадия — комбинированное лечение в двух вариантах: дистанционное или внутриполостное облучение с последующей расширенной экстирпацией матки с придатками или расширенная экстирпация матки с последующей дистанционной у-терапией. При наличии противопоказаний к хирургическому вмешательству — сочетанная лучевая терапия (дистанционное и внутриполостное облучение).
II стадия — в большинстве случаев применяется сочетанный
лучевой метод; хирургическое лечение показано тем больным,
у которых лучевая терапия не может быть проведена в полном
объеме, а степень местного распространения опухоли позволя
ет произвести радикальное оперативное вмешательство.
III стадия — лучевая терапия в сочетании с общеукрепляющим и дезинтоксикационным лечением.
IV стадия — симптоматическое лечение.
Глава 7. Фоновые и предраковые заболевания 331
7.2. Гиперпластические процессы эндометрия
Гиперпластические процессы эндометрия (ГПЭ)— доброкачественная патология эндометрия, характеризующаяся прогре-сированием клинико-морфологических проявлений (от простой и комплексной гиперплазии к атипическим предраковым состояниям эндометрия) и возникающая на фоне хронической ановуляции, когда при отсутствии или недостаточном антипро-лиферативном влиянии прогестерона возникает абсолютная или относительная гиперэстрогения.
7.2.1. Этиопатогенез ГПЭ
Причины и механизмы развития ГПЭ рассматривают как варианты отклонения от нормального функционирования эндокринной системы: патология биосинтеза, ритма и цикличности, выброса и нарушения соотношений в содержании гормонов; нарушение функции рецепторной системы клеток, особенно органов-мишеней; патология генетически детерминированной системы «гормон-рецептор»; «срыв» иммунологического контроля за элиминацией патологически трансформированных клеток; нарушение метаболизма половых гормонов при патологии гепатобилиарной системы и желудочно-кишечного тракта; нарушение функции щитовидной железы.
Формирование ГПЭ происходит в условиях стойкой гипе-рэстрогении на фоне пониженной продукции прогестерона. Причины гиперэстрогении: дисфункция яичников (персистен-ция или атрезия фолликулов); фолликулярные кисты; стро-мальная гиперплазия; опухоли тека-клеток; гиперплазия коры надпочечников; нарушение гонадотропной функции гипофиза; некорректное применение эстрогенов; изменения в метаболизме гормонов (ожирение, цирроз печени, гипотиреоз).
Возникновение гиперэстрогении связано как с ановуляцией в репродуктивном периоде и пременопаузе, так и с ожирением, приводящим к повышенному превращению андростендиола в эстрон в жировой ткани.
В развитии ГПЭ большую роль играет состояние рецепторного аппарата эндометрия. В норме содержание цитоплазмен-

 332 Практическая гинекология
332 Практическая гинекология
ных рецепторов прогестерона и эстрадиола в эндометрии под влиянием эстрогенов повышается, а под влиянием прогестерона— снижается. При прогрессировании ГПЭ количество прогестероновых рецепторов уменьшается. Отмечается прямая зависимость дифференцировки опухоли от состояния рецепторного аппарата: чем ниже степень дифференцировки, тем меньше рецепторов эндометрия к эстрогенам, прогестеронам и андрогенам и наоборот.
Среди дисгормональных состояний, обусловливающих формирование ГПЭ, выделяют нарушение физиологической секреции тиреоидных гормонов, являющихся модулятором действия эстрогенов.
В регуляции процессов клеточной пролиферации принимают участие не только эстрогены, но и биологические амины, вырабатываемые клетками АПУД-системы. В злокачественных нейроэндокринных опухолях обнаружено многократное увеличение их концентрации.
Ожирение — характерная особенность для больных раком тела матки. Нарушение жирового и углеводного обмена предрасполагают к развитию ГПЭ. Отмечается высокая частота сахарного диабета у больных железистой гиперплазией, атипической гиперплазией и особенно раком эндометрия.
В патогенезе предопухолевых процессов эндометрия огромное значение имеет нарушение иммунной системы. Наблюдается снижение количества и функциональной активности Т-лимфоцитов, периферических В-клеток, часто отмечается лимфопения.
Имеются сведения о воспалительном генезе ГПЭ. Длительные морфологические и функциональные изменения в слизистой оболочке тела матки при хроническом эндометрите обусловливают возможность патологической афферентации в структуры ЦНС, регулирующих деятельность гипоталамо-ги-пофизарной системы. Нарушение в ней ведут к развитию вторичной гипофункции яичников, формированию ановуляции по типу абсолютной или относительной гиперэстрогении и, следовательно ГПЭ.
В развитии ГПЭ велика роль наследственных факторов [29].
Глава 7. Фоновые и предраковые заболевания________________________ 333
Дата добавления: 2014-12-16; просмотров: 1443;
