Лекция 2. Количественно скорость химической реакции w выражается числом единиц массы одного из продуктов или реагентов
Количественно скорость химической реакции w выражается числом единиц массы одного из продуктов или реагентов, которые образуются или прореагируют в единицу времени t в единице объема системы V.
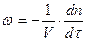 (7)
(7)
где n- число частиц (молекул) реагентов.
При постоянном объеме
 (8)
(8)
Таким образом скорость химической реакции можно выразить как бесконечно малое изменение концентрации одного из компонентов реакции, отнесенное к бесконечно малому промежутку времени и к объему системы.
Скорость гетерогенных химических реакций относят не к единице объема, а к единице поверхности реагирования или к пропорциональным ей величинам.
Таким как, объем аппарата, объем газа при постоянном объеме аппарата.
Кинетическое уравнение – зависимость, выражающая в явной форме скорость реакции как функцию концентраций или парциальных давлений P компонентов реакции.
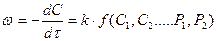 - гомогенные реакции (9)
- гомогенные реакции (9)
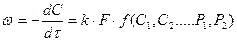 - гетерогенные реакции (10)
- гетерогенные реакции (10)
где F- площадь поверхности.
 Коэффициент пропорциональности – КС для каждой реакции при t = const является величиной постоянной и называется константой скорости реакции или удельной скоростью реакции. Физический смысл КС можно представить, если принять концентрацию компонента равной единице, тогда w = КС. В действительности эта константа, согласно закону Аррениуса, является функцией температуры.
Коэффициент пропорциональности – КС для каждой реакции при t = const является величиной постоянной и называется константой скорости реакции или удельной скоростью реакции. Физический смысл КС можно представить, если принять концентрацию компонента равной единице, тогда w = КС. В действительности эта константа, согласно закону Аррениуса, является функцией температуры.
Дата добавления: 2014-12-26; просмотров: 810;
