Реакции электрофильного замещения
Фуран легко вступает в реакции электрофильного замещения,легче, чем бензол. По сравнению с другими рассматриваемыми в данной главе гетероциклами – пирролом и тиофеном, фуран наименее ароматичен. Это объясняется тем, что этот гетероцикл включает в кольцо наиболее электроотрицательный атом кислороды по сравнению с пирролом и тиофеном. По этой причине кислород труднее отдает свою свободную электронную пару на образование ароматического секстета. Попутно отметим, что охотнее всего электроны для этой цели поставляет атом серы, поэтому наиболее ароматичным оказывается тиофен, а пиррол занимает промежуточное положение.
Не все положения в фурановом кольце равнозначны – α-положения богаче электронной плотностью и предпочтительны для электрофильной атаки
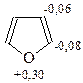
Поэтому в результате реакций электрофильного замещения с участием фурана преимущественно образуются α-замещенные фураны. Интересно, если в этих реакциях участвуют фураны с занятыми α-положениями, то реакция идет по β-положениям, т.е. фуран менее разборчив к месту вступления нового заместителя в кольцо.
Галогенирование. Галогенирование фурана проходит даже при низкой температуре, но в начале как реакция 1,4-присоединения. Образующиеся продукты легко дегидрогалогенируются с образованием 2-замещенных фуранов
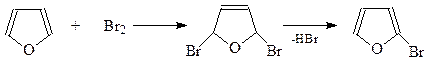
Нитрование. Нитровать фуран азотной кислотой или нитрующей смесью не удается. Под действием кислот фурановое кольцо разрушается. Однако удалось найти реагент, позволяющий успешно вводить в гетероциклическое кольцо нитрогруппу. Это ацетилнитрат (реагент Терентьева) – смешанный ангидрид уксусной – и азотной кислот
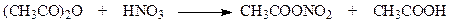
Под действием ацетилнитрата нитрование фурана идет следующим образом
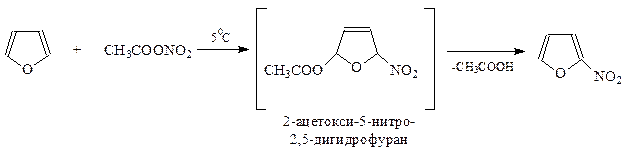
При низкой температуре (-10оС) промежуточный продукт присоединения удается даже выделить, но уже при +5оС реакция идет дальше – до 2-нитрофурана, получающегося с высоким выходом.
Рассматриваемая реакция используется при синтезе одного из эффективных бактерицидных препаратов – фурацилина
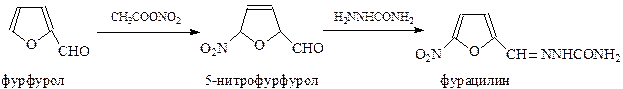
Сульфирование. При сульфировании фурана мягкодействующим сульфирующим агентом – пиридинсульфотриоксидом – с высоким выходом получается фуран-2-сульфокислота (Терентьев, 1947 г.)
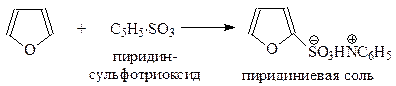
Ацилирование. Фуран ацилируется обычными ацилирующими средствами достаточно легко. О его высокой реакционной способности говорит тот факт, что реакцию можно проводить в растворе бензола, который при этом в реакцию не вступает. В реакции ацилирования фурановых соединений используются обычно ангидриды кислот, а в качестве конденсирующих агентов такие мягко действующие вещества как хлористый цинк, хлористое или хлорное олово и др., но не слишком активный в этой реакции хлорид алюминия. Продуктами реакции являются 2-ацилзамещенные фураны
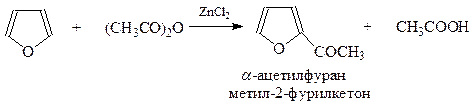
Хотя фуран и может алкилироваться, однако, эта реакция пока не находит применения в органическом синтезе, т.к. в условиях реакции фуран полимеризуется, осмоляется и полиалкилируется.
Дата добавления: 2014-12-24; просмотров: 5903;
