ТЕОРИЯ АКТИВИРОВАННОГО КОМПЛЕКСА (ТАК) ИЛИ ТЕОРИЯ ПЕРЕХОДНОГО СОСТОЯНИЯ (ТПС).
Основным представлением ТАК является положение о том, что всякая химическая реакция протекает через образование некоторого переходного состояния, которое затем распадается на продукты данной реакции.
Основные положения теории:
1. В ходе процесса молекулы постепенно приближаются друг к другу, в результате чего меняются межъядерные расстояния.
2. В ходе реакции образуется активированный комплекс, когда один из атомов становится как бы обобществленным, и межъядерное расстояние становится одинаковым.
3. Активированный комплекс превращается в продукты реакции.
Например, реакцию разложения йодоводорода можно представить следующим образом:
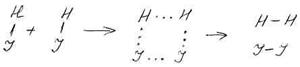
Сначала две молекулы HJ расположены достаточно далеко друг от друга. При этом существует взаимодействие лишь между атомами в молекуле. После сближения на достаточно короткое расстояние начинают возникать связи между атомами, входящими в состав разных молекул, и связи H – J становятся более слабыми. В дальнейшем они ещё более ослабевают и полностью разрываются, а новые связи H – H и J – J, наоборот, упрочняются. В результате происходит перегруппировка атомов и вместо исходных молекул НJ образуются молекулы Н2 и J2. В процессе сближения и перегруппировки атомов молекулы образуют некоторый малоустойчивый активированный комплекс из двух молекул водорода и двух молекул йода; комплекс существует очень недолго и в дальнейшем распадается на молекулы продуктов. На его образование необходима затрата энергии, равная энергии активации.
Представление об активированном комплексе и об энергии активации подтверждается с помощью энергетических диаграмм, построение которых используется в ТАК.
Активированный комплекс всегда имеет избыток энергии по сравнению с энергией реагирующих частиц.
А–В+D 
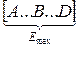 → A+B–D
→ A+B–D
переходное состояние
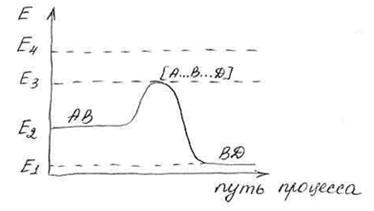
Е1 – энергия связи BD без А.
Е2 – энергия связи АB без D.
Е3 – энергия связи переходного состояния.
Е4 – энергия свободных атомов.
Е3 – Е2 = Е активации прямой реакции.
Е2 – Е1 = ∆Н тепловой эффект реакции.
Е4 – Е2 – энергия разрыва связи АВ.
Е4 – Е1 – энергия разрыва связи ВD.
Так как энергия разрыва связей Е4 >> Е активации, то реакция протекает с образованием активированного комплекса без предварительного разрыва связей.
Дата добавления: 2019-10-16; просмотров: 770;
