Кинетические кривые для последовательных реакций.
КИНЕТИКА ПОСЛЕДОВАТЕЛЬНЫХ РЕАКЦИЙ.
Последовательныминазываются реакции, состоящие из нескольких стадий, следующих друг за другом, например, гидролиз трисахаридов в кислой среде:
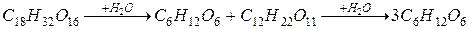
Рассмотрим реакцию, состоящую из двух мономолекулярных стадий:
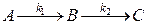
Вещество В в данной реакции является промежуточным веществом.
Обозначим через а – начальную концентрацию вещества А ( 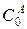 = а). Тогда концентрация реагента А в момент времени
= а). Тогда концентрация реагента А в момент времени 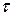 равна
равна 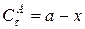 , реагента В в момент времени
, реагента В в момент времени 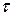
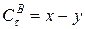 , реагента С в момент времени
, реагента С в момент времени 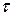
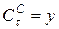 . Т. е. в начале реакции идет образование вещества В, пока концентрация реагента А достаточна велика. Одновременно реагент В расходуется на образование вещества С.
. Т. е. в начале реакции идет образование вещества В, пока концентрация реагента А достаточна велика. Одновременно реагент В расходуется на образование вещества С.
Напишем кинетические уравнения последовательной реакции.
Скорость реакции по изменению концентрации реагента А запишется (I ступень):
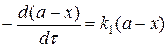
Скорость реакции по изменению концентрации реагента В (II ступень) запишется:
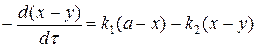
Скорость реакции по приросту концентрации реагента С (III ступень) запишется:
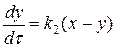
Кинетические кривые для последовательных реакций.
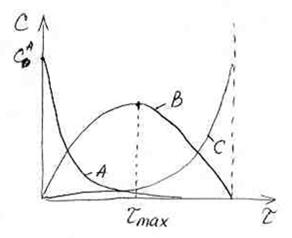
Концентрация вещества А с течением времени плавно уменьшается до нуля, что отображает кинетическая кривая для реагента А.
Концентрация реагента С в ходе реакции плавно возрастает, пока не достигнет своего максимального значения, что также отображается ходом кинетической кривой для данного реагента.
Кинетическая кривая для реагента В имеет максимум. Он обусловлен тем, что в начале процесса, пока концентрация вещества А достаточна большая, расходование вещества В компенсируется расходованием вещества А. На кинетической кривой – рост. Когда вещества А становится очень мало, то оно уже не может компенсировать расход вещества В на II ступени, поэтому на кинетической кривой наблюдается спад.
Время, за которое достигается максимальное значение концентрации вещества В, называют 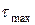 , оно зависит от соотношения констант скоростей стадий
, оно зависит от соотношения констант скоростей стадий 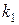 и
и 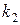 .
.
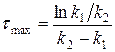
Рассмотрим два случая относительно разности значений констант скоростей 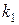 и
и 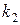 .
.
1. Когда скорость первой стадии намного больше скорости второй стадии: 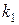 >
> 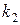 .
.
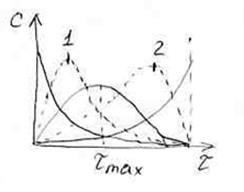
В этом случае достижение максимальной концентрации промежуточного вещества В происходит быстро. Максимум, соответствующий 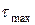 ,смещается к началу координат.
,смещается к началу координат.
2.Когда скорость первой стадии намного меньше скорости второй стадии: 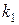 <
< 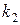 .
.
В этом случае накопление промежуточного вещества В идет медленно,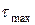 смещается дальше от начала координат. После достижения максимального времени идет быстрый расход компонента В.
смещается дальше от начала координат. После достижения максимального времени идет быстрый расход компонента В.
Дата добавления: 2019-10-16; просмотров: 1148;
