Молекулярные кристаллы
В узлах кристаллической решетки молекулярных кристаллов располагаются молекулы. Связь между ними осуществляется за счет сравнительно слабых, короткодействующих сил межмолекулярного взаимодействия (силы Ван-дер-Ваальса) и водородных связей. Расположение частиц подчиняется законам плотнейшей упаковки с учетом геометрии самих молекул и ориентирующим эффектом ориентационного и индукционного взаимодействия диполей. Межмолекулярное расстояние существенно больше, чем внутримолекулярное (длина связи в молекулах меньше, чем расстояние между молекулами). В ряде случаев из молекулярных кристаллов в отдельную группу выделяют кристаллы с преимущественно водородной связью между молекулами. Отличительной особенностью строения этих кристаллов (например, кристаллов льда) является расположение молекул в пространстве и число ближайших соседей, обусловленное водородными связями между молекулами.
Пример. В кристаллах йода длина ковалентной связи в молекуле I2 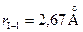 , а расстояние между молекулами I2-I2
, а расстояние между молекулами I2-I2 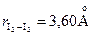 и
и 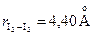 в зависимости от направления в кристаллической решетке.
в зависимости от направления в кристаллической решетке.
Подобным образом кристаллизуются многие органические вещества, H2O, CO2, N2, Xe, Kr, H2 и т.д. Кристаллы обладают сравнительно низкой температурой плавления, низкой твердостью, неэлектропроводны.
Дата добавления: 2017-02-20; просмотров: 695;
