Химические свойства
Реакции оксогруппы
Окисление.В зависимости от типа окислителя и условий реакции моносахариды могут окисляться с образованием различных продуктов:
А.В реакциях с мягкими окислителями (аммиакат серебра, реактив Фелинга, бромная вода) альдозы окисляются с участием альдегидной группы с образованием альдоновых кислот.
Окисление аммиакатом серебра (реакция серебряного зеркала). Глюкоза окисляется до глюконовой кислоты в виде аммониевой соли с выделением металлического серебра в виде зеркала:
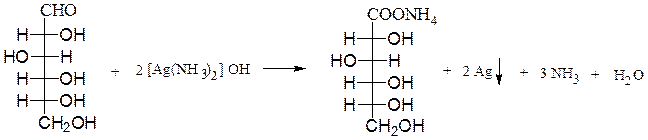
аммониевая соль
D-глюкоза D-глюконовой кислоты
Окисление реагентом Фелинга, содержащего в виде комплексного соединения двухвалентную медь в щелочной среде. При окислении альдегид-ной группы сахарида реагент восстанавливается при нагревании до красного осадка оксида меди (I); глюкоза окисляется в глюконовую кислоту:
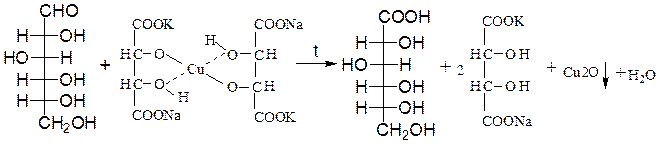
D-глюкоза D-глюконовая кислота
Благодаря способности восстанавливать ионы Сu2+ или Аg+, моносахариды или их производные, содержащие альдегидную группу, называют восстанавливающими. Обе реакции применяются для качественного и количественного определения моносахаридов в биологических средах.
Окисление бромной водой. Реакциясопровождаетсяобесцвечиванием бромной воды, так как молекулярный бром восстанавливается в бесцветный бромид-анион.
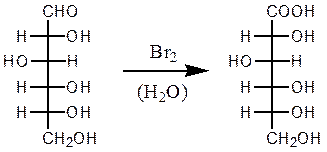
D-глюкоза D-глюконовая кислота
Кетозы бромной водой не окисляются, поэтому реакция применяется для отличия кетоз от альдоз. Так как реакции с аммиакатом серебра и жидкостью Бенедикта–Фелинга проводятся в щелочной среде, в которой устанавливается равновесие между эпимерами (см. ниже), то они положительные и для кетоз.
Б. В присутствии сильных окислителей, например, концентрированной азотной кислоты, помимо альдегидной группы, окисляется первичная спиртовая группа с образованием дикарбоновых полигидроксикислот, называемых альдаровыми кислотами (гликаровые, сахарные кислоты). Так, при окислении D-глюкозы концентрированной HNO3 получают глюкаровую кислоту, при окислении галактозы – галактаровую (слизевую) кислоту.
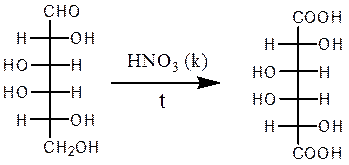
D-галактоза галактаровая (слизевая) кислота
В. Окисление йодной кислотой.При обработке соединений, содержащих две и более групп –OH или = О, находящихся у соседних атомов углерода, иодной кислотой (реакция Малапрада) протекает реакция окисления с расщеплением С–С связи по следующим схемам:
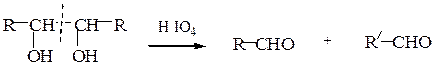
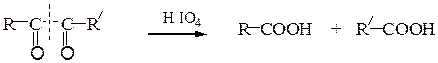
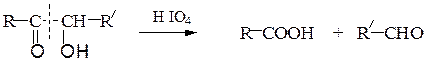
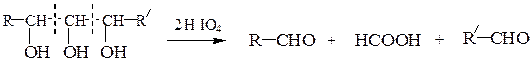
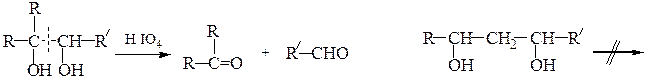
Каждая концевая группа СН2ОН, отщепляясь, образует молекулу формаль-дегида, а каждая отщепляющаяся группа –СНОН – молекулу муравьиной кислоты:
HOCH2 – (CHOH)n – CH2OH
↓ ↓ ↓
HCHO n HCOOH HCHO
На основании данных о продуктах реакции, их соотношении и по количеству израсходованной HIO4 делают выводы о структуре окисленного вещества. Для моносахаридов различного строения окислительное расщепление под действием йодной кислоты протекает по следующим схемам:
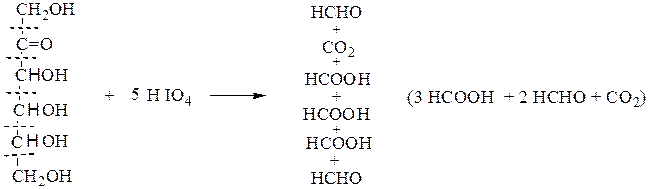 кетогексоза
кетогексоза
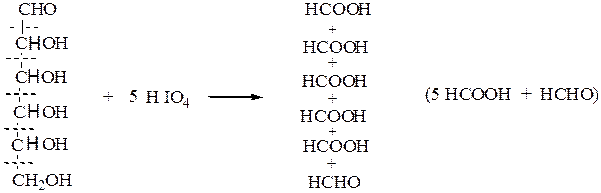
альдогексоза
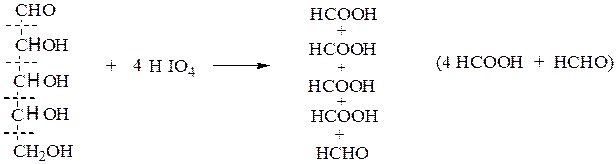
альдопентоза
Г. Для окисления только первичной спиртовой группы в молекуле моносахарида, альдегидную группу первоначально защищают путем образования метилгликозида, который на последующей стадии подвергают гидролизу и получают уроновые (альдуроновые) кислоты:
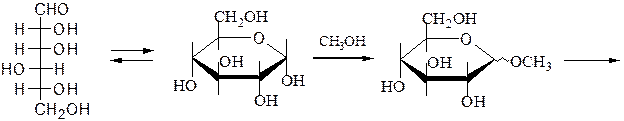 метилгликозид
метилгликозид
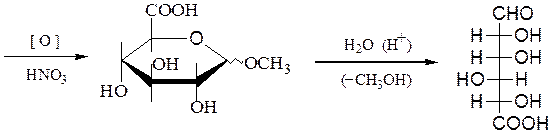
Уроновые кислоты способны превращаться в лактоны и декарбоксили-роваться до пентоз, а также окисляться и восстанавливаться:
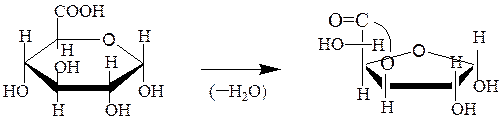
D-глюкуроновая кислота γ-лактон D-глюкуроновой кислоты
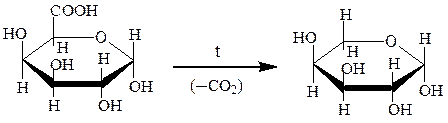
D-галактуроновая кислота L-арабиноза
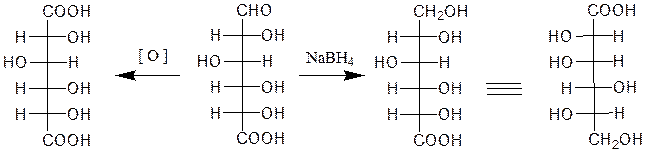 D-глюкаровая D-глюкуроновая L-гулоновая кислота
D-глюкаровая D-глюкуроновая L-гулоновая кислота
кислота кислота
Восстановление моносахаридов амальгамой натрия или комплексными гидридами металлов (боргидрид натрия NaBH4, алюмогидрид лития LiAlH4) приводит к получению соответствующих многоатомных спиртов:
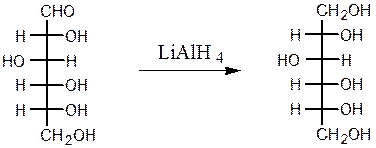
D-глюкоза D-сорбит
Привосстановлении кетоз, например D-фруктозы, возникает новый асимметрический углеродный атом, что приводит к образованию двух многоатомных спиртов:
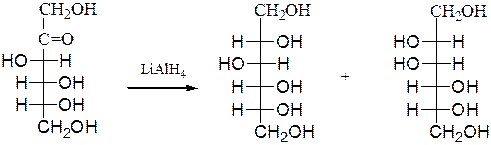
D-фруктоза D-сорбит D-маннит
Удлинение углеродной цепи моноз на один атом углерода осуществляют с помощью последовательных реакций по Фишеру-Килиани:
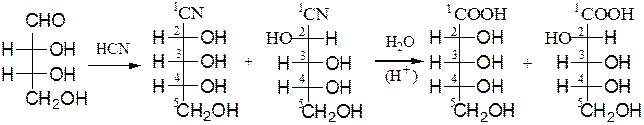
D-эритроза два диастереоизомера, т.к. две диастереоизомерные
возникает новый асиммет- альдоновые кислоты
рический центр при С2
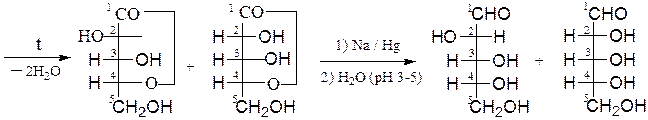 g-лактоны D-арабиноза D-рибоза
g-лактоны D-арабиноза D-рибоза
(две диастереоизомерные пентозы)
Дата добавления: 2017-09-19; просмотров: 5741;
