Влияние атмосферных газов на свойства цветных металлов
Медь при взаимодействии с кислородом дает стабильный оксид Сu2О, растворимый в жидкой меди:
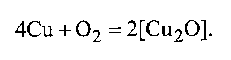 (9.24)
(9.24)
В расплаве оксид меди Сu2О весьма устойчив, но при кристаллизации вследствие ликвации образуется эвтектика Сu- Сu2О и фаза Сu2О теряет свою устойчивость, вызывая под воздействием О2и Н2так называемую «водородную болезнь» меди, которая приводит к разрушению металла и является результатом последовательного взаимодействия меди с кислородом по реакции (9.24), а затем с водородом по следующей реакции:
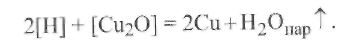 (9.25)
(9.25)
И 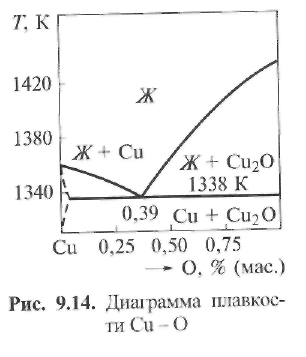 ными словами, водород, растворенный в окисленном металле, взаимодействует с оксидом Сu2О, находящимся в эвтектике и восстанавливает его до Сu, но образующиеся при этом пары воды не диффундируют через металл и разрушают его по границам зерен.
ными словами, водород, растворенный в окисленном металле, взаимодействует с оксидом Сu2О, находящимся в эвтектике и восстанавливает его до Сu, но образующиеся при этом пары воды не диффундируют через металл и разрушают его по границам зерен.
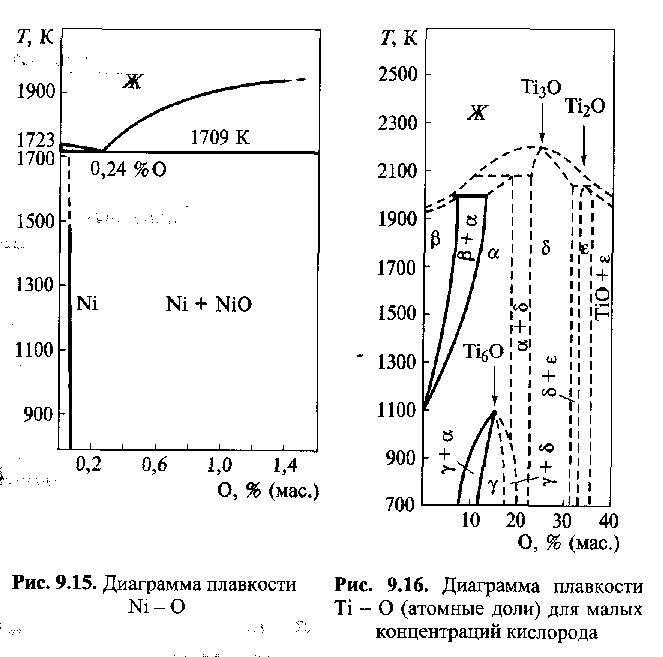
Равновесная диаграмма плавкости Сu-О приведена на рис. 9.14. Как следует из диаграммы, в области температур ниже 1065 °С (1338 К) существует раствор Сu+ Сu2О, но растворимость Сu2О в твердой фазе ничтожно мала. Таким образом, при сварке меди и ее сплавов необходимо принимать все меры для снижения степени ее окисления или вводить раскислители.
Аналогичная ситуация имеет место при сварке деталей из никеля и его сплавов. Никель с О2образует два соединения:Ni2Оз иNiO. Первый из них неустойчив, является сильным окислителем (он применяется в щелочных аккумуляторах). Второй -NiO- устойчивый оксид. Он хорошо растворим в жидком никеле, но не растворим в твердом никеле. Диаграмма плавкости, приведенная на рис. 9.15, показывает, что содержащиеся в металле оксиды никеля при нагревании выше 1700 К легко диссоциируют, выделяя кислород, который образует поры с водородом, находящимся в жидком металле, при его кристаллизации. Никель, в отличие от железа, не взаимодействует с азотом, который может служить для него так же, как и для Сu, защитной средой.
Титан является особо активным химическим элементом по отношению к кислороду, с которым он образует ряд устойчивых оксидов, обладающих различной степенью окисления. Кроме того, кислород растворяется в твердом металле. Оксиды, особенно имеющие низкую степень окисления: TiO,Ti2O3, ТiO2, обладают большим температурным интервалом гомогенности, т. е. существуют в однофазном твердом растворе при охлаждении до нормальной температуры (рис. 9.16).
 При температурах этого интервала наиболее устойчив оксид TiO. Для оксидов титана характерна ступенчатая диссоциация, которая идет по двум вариантам:
При температурах этого интервала наиболее устойчив оксид TiO. Для оксидов титана характерна ступенчатая диссоциация, которая идет по двум вариантам:
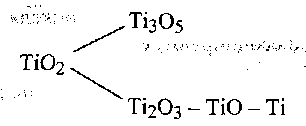 (9.26)
(9.26)
Из оксидов титана наименьшую температуру диссоциации имеет TiО2(∆G= 0 при 3500 К), диссоциация которого происходит согласно уравнению
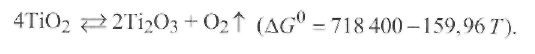 (9.27)
(9.27)
Титан также активно взаимодействует с азотом и водородом (см. рис. 9.7), образуя нитриды и гидриды, поэтому требуется особо тщательная защита его сплавов от атмосферы при сварке.
Алюминий соединяется с кислородом в устойчивый амфотерный оксид А12O3(корунд), образующий соли как в кислой, так и в щелочной среде. Оксид А12O3не растворим в алюминии и образует плотную оксидную пленку, имеющую весьма высокие температуру плавления (T> 2500 К) и плотность (выше, чем у металла). При сварке с окислением в шве образуются включенияAI2O3, т. е. шлаки, которые приводят к охрупчиванию металла шва. Кроме того, поверхностные пленки из А12O3склонны к адсорбции Н2O, т. е. к гидратации во влажной среде. Гидратная вода, входящая в А12O3•
п Н2O, при сварке диссоциирует и это приводит к повышению парциального давления водорода в столбе дуги. При охлаждении до температуры кристаллизации растворимость водорода резко снижается практически до нулевых значений (см. рис. 9.6,а) и при кристаллизации часть выделяющегося газа создает поры в шве. Второй продукт диссоциации - кислород - окисляет основу сплава или его главный легирующий компонент (Mg,Li) и тем самым увеличивает долю шлака в шве в виде легкоплавкой эвтектики.
Таким образом, попадание атмосферных газов в большей или меньшей степени в зону столба дуги вследствие несовершенства газовой защиты или в виде примесей в защитных газах оказывает вредное воздействие на конструкционные металлы и сплавы в шве и в зоне термического влияния, так как приводит к образованию в них горячих либо холодных трещин и пор, а также к снижению прочности и пластичности сварных соединений
Дата добавления: 2017-01-13; просмотров: 1136;
