Организмнің буферлiк жүйелерi. Бикарбонаттық және фосфаттық буферлiк ерiтiндiлердiң әсер ету механизмi
Организмде биологиялық орталардың қышқылдылығын тұрақты ұстап тұратын тең процестер болады. Олардың тұрактылығы буферлiк жүйелердiң әсер ету механизмiмен тiкелей байланысты.
Бикарбонаттық буферлiк жүйе қан плазмасының негiзгi жүйесi болып есептеледi. Бұл жүйе әлсіз көмiр қышқылынан (К = 3,3 10–7) және нaтрий бикарбонатынан тұрады.
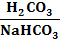
H2CO3 – протонның доноры;
HCO3– – протонның акцепторы.
Қандағы буферлiк қатынас мынадай: H2CO3 = 1
NaHCO3 = 20
Қышқыл заттар көп мөәлшерде қанға бөлiнгенде, сутегi иондары бикарбонат ионымен әрекеттесiп, әлсiз көмiр қышқылын түзедi:
H+ + HCO3– = H2CO3
Көмiр қышқылының артық мөлшерi карбоангидраза (КА) ферментiнiң әсерiнен ыдырайды (t=370C):
H2CO3 = CO2 + H2O
CO2 гипервентилляция нәтижесiнде өкпе арқылы сыртқа шығады.
Егер қандағы OH– иондардың концетрациясы жоғарыласа, олар әлсiз көмiр қышқылымен әрекеттеседi:
OH– + H2CO3 = HCO3– + H2O
Буферлiк жүйедегi қалыпты қатынас сақталу үшiн қышқылды-негiздiк теңдiктiң физиологиялық механизмдерi iске қосылады: өкпенiң гиповентилляциясы нәтижесiнде қанда аз мөлшерде болса да CO2 сақталады.
Оксигемоглобин – гемоглобин жүйесi қанның буферлiк сиымдылығының 75%-iн құрайды, ол гемоглобин ионы (Hb–) мен гемоглобиннiң (HHb) арасындағы тепе-теңдiкпен сипатталады:
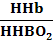
HHb – донор
Hb– – акцептор
Hb– + H+ = HHb
HHb + OH– = Hb– + H2O
Сол сияқты бұл жүйе оксигемоглобин ионы (HbO2–) мен окси–гемоглобиннiң (HHbO2) арасындағы тепе-теңдiкпен де сипатталады:
HHbO2 – протонның доноры
HbO2– – протонның акцепторы
HbO2– + H+ = HHbO2
HHbO2 + OH– = HbO2– + H2O
Екi тепе-теңдiктiң арасындағы байланыс мына теңдеумен көрсетiледi:
HHb + O2 = HHbO2
Фосфаттық буферлiк жүйе клетка iшiлiк және тканьдiк негiзгi жүйе болып есептеледi. Бүйректе жүретiн физиологиялық процестерде маңызды роль атқарады. Бұл жүйе 2 тұздан тұрады:
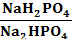
NaH2PO4 (H2PO4– - протонның доноры)
Na2HPO4 (HPO42– – протонның акцепторы)
H2PO4– = H+ + HPO42–
pH = 7,4 болғанда, NaH2PO4 = 4
Na2HPO4 = 1
Тканьдiк метаболизмнiң қышқыл туындылары гидрофосфатпен нейтралданады:
HPO42– + H+ = H2PO4–
Сiлтiлiк туындылар дигидрофосфатпен әрекеттеседi:
OH– + H2PO4– = HPO42– + H2O
Түзілген өнiмдер бүйректе жиналып, несеппен сыртқа шығады.
Дата добавления: 2016-12-16; просмотров: 2903;
