Лекция1. Физическая природа ионизирующих излучений
1.1 Радиоактивные превращения ядер
Радиоактивность – это свойство некоторых нестабильных атомов подвергаться спонтанному (самопроизвольному) распаду и изменению своего нуклонного состава (количество протонов и нейтронов в ядре) и (или) энергетического состояния с образованием новых более стабильных атомов и испусканием ионизирующих излучений с большей или меньшей проникающей способностью.
Радиоактивностью обладают некоторые нестабильные элементы, способные самопроизвольно распадаться или изменять свой нуклонный состав, испуская ионизирующие излучения.
Естественная радиоактивность урана была открыта в мае 1896 г. французским ученым физиком Анри Беккерелем. За полгода до него (8 ноября 1895 г.) физик Вюрцбургкого (Германия) университета Вильгельм Конрад Рентген открыл антропогенное излучение «катодной трубки» (Х – лучи). Оба в последующем стали лауреатами Нобелевской премии.
1898 г. ученица Беккереля Мария Складовская – Кюри (в последующем дважды лауреат Нобелевской премии) и ее муж Пьер Кюри обнаружили, что торий также испускает лучи Беккереля, названные ими «радиоактивностью». Они выделили еще два радиоактивных элемента – полоний и радий.
 Свойством радиоактивности обладают все элементы таблицы Менделеева тяжелее висмута – 83 (83Bi) и два более легких элемента: технеций – 43 (43Тс) и прометий – 61 (61Рт).
Свойством радиоактивности обладают все элементы таблицы Менделеева тяжелее висмута – 83 (83Bi) и два более легких элемента: технеций – 43 (43Тс) и прометий – 61 (61Рт).
Нестабильность атомов объясняется конкуренцией между притяжением нуклонов ядерными силами и кулоновским отталкиванием протонов. Если ядро содержит значительно больше протонов, чем нейтронов, то нестабильность обусловливается избытком энергии кулоновского взаимодействия. Ядра, содержащие избыток нейтронов над числом протонов, оказываются нестабильными, т.к. масса нейтрона превышает массу протона. Радиоактивность – самое древнее явление в природе. Оно существовало до возникновения Земли. Из имеющихся в природе почти 3 тыс. химических элементов стабильными являются около 300.
Атом состоит из ядра и вращающихся вокруг него электронов. Модель построения атома была предложена в 1913 году датским физиком Н. Бором, за основу которого была принята планетарная модель Э. Резерфорда.
Атом состоит из положительно заряженного ядра, вокруг которого движутся по строго определённым орбитам отрицательно заряженные электроны. Положительный заряд атома сосредоточен в малом по размерам ядре атома. Атомы имеют средний размер порядка 10 – 8 см и массу 10 – 27 кг. Размеры ядер приблизительно в 105 раз меньше диаметра всего атома. Электроны удалены от ядра на расстоянии ≈ 10 – 5 м.
Величина заряда электрона составляет 1,6 • 10 – 19 Кл, а масса больше ядра атома водорода в 1836 раз и составляет 9,1 • 10 – 31 кг. Основная масса атома сосредоточена в ядре, на долю электронов приходится менее 0,05% массы атома. Располагаясь на определенных расстояниях от атомного ядра, электроны образуют электронные слои (электронные оболочки), рисунок 1.2.
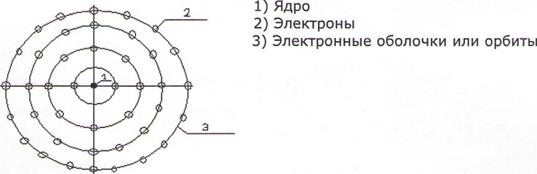
Рисунок 1.2 – Строение электронных оболочек атома
На ближайшей к ядру К – оболочке может располагаться не более 2 – х электронов ( 2К2), на следующей L – оболочке – 8 электронов, на М – оболочке – 16, на N – оболочке – 32 электрона и т.п. Отметим, что с увеличением Z идет последовательное заполнение электронных оболочек.
Если электроны заполняют свои орбиты, то атом находится в устойчивом состоянии.
Если орбитальный электрон получает дополнительную энергию извне, не превышающую энергию связи электрона с ядром, то он переходит на более удаленную орбиту (атом становится возбужденным).
Стремясь к равновесию, через некоторое время (примерно через 10 – 8 с) электрон вернётся на свою орбиту, при этом будет выделена электромагнитная энергия в виде фотона, равная Е =hv (пост. Планка h = 6,6262 • 10 – 34 Дж/сек, v – частота гамма – кванта).
Если электрон получает дополнительную энергию извне, превышающую энергию связи электрона с ядром, то последний покидает атом, превращая его в положительно заряженный ион.
Дата добавления: 2016-11-28; просмотров: 1541;
