Способы выражения содержания растворенного вещества в растворе
Концентрацией раствора называется величина, выражающая относительное содержание растворенного вещества в растворе.
Концентрация раствора имеет разные формы выражения: либо безразмерными единицами – долями или процентами, либо величинами размерными.
Важнейшие из них следующие.
Массовая доля растворенного вещества (ω) показывает, сколько едениц массы растворенного вещества содержится в 100 еденицах массы раствора. Массовая доля – безразмерная величина, ее выражают в долях единицы или процентах:
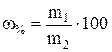 ,
,
где ω – массовая доля (%) растворенного вещества; m1 – масса растворенного вещества, г; m – масса раствора, г.
Масса раствора равна произведению объема раствора V на его плотность r:
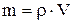 , тогда
, тогда 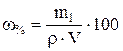 .
.
Молярная концентрация (молярность) раствора – показывает, сколько молей растворенного вещества содержится в 1л раствора.
Молярную концентрацию (моль на литр) выражают формулой
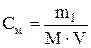 ,
,
где m1 – масса растворенного вещества, г; М – молярная масса растворенного вещества, г/моль; V – объем раствора, л.
Нормальная концентрация (нормальность раствора) показывает, сколько грамм-эквивалентов растворенного вещества содержится в 1 л раствора (моль на литр): 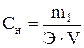 ,
,
где m1 – масса растворенного вещества, г; Э – молярная масса эквивалента растворенного вещества, г/моль; V – объем раствора, л.
Моляльность раствора Сm показывает количество растворенного вещества, находящееся в 1 кг растворителя:
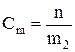 ,
,
где m2 – масса растворителя, кг; n – количество растворенного вещества, моль.
Титр раствора (Т) показывает массу (г) растворенного вещества, содержащегося в 1 мл раствора:
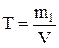 или
или 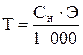 ,
,
где m1 – масса растворенного вещества, г; V – объем раствора, мл; Сн – нормальность раствора, моль/л; Э – молярная масса эквивалента, г/моль.
При выполнении заданий рекомендуется использовать методические указания [7].
Дата добавления: 2016-08-07; просмотров: 1190;
