Способы описания состояния вещества
Существуют три способа описания состояния вещества:
1) молекулярно-кинетический, основанный на рассмотрении движения и взаимодействия частиц (атомов и молекул), из которых состоит исследуемое вещество;
2) статистический, основанный на рассмотрении всей совокупности частиц вещества, образующих систему; свойства частиц определяются как средние для всей совокупности на основе функции распределения;
3) термодинамический, в котором не учитывается микроскопическое строение вещества, а его физические свойства рассматриваются через функции состояния в зависимости от термодинамических параметров (давления, температуры, массы вещества, объема системы) с помощью ряда аксиом (начала термодинамики).
В молекулярно-кинетическом способе рассматривают пару взаимодействующих частиц вещества. Определяют полную энергию 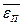 взаимодействия в зависимости от расстояния r между частицами как сумму кинетической энергии
взаимодействия в зависимости от расстояния r между частицами как сумму кинетической энергии 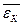 и потенциальной U(r) в расчете на частицу:
и потенциальной U(r) в расчете на частицу:
 .(15.1)
.(15.1)
Кинетическая энергия определяется тепловым хаотическим движением частиц и выступает как мера разупорядоченности структуры вещества.
Для определения величины U(r) необходимо выбрать одну из моделей взаимодействия пары частиц (молекул или атомов) вещества. Выбор модели базируется на основе значений параметров состояния, фазового состояния, строения молекул или атомов изучаемого вещества, достаточной точности результатов расчета и расчетных возможностей.
Наиболее распространенные физические модели потенциальных функций взаимодействия для пары частиц (молекул, атомов) приведены в прил. I.
Величина потенциальной энергии парного взаимодействия рассматривается как мера упорядоченности и ограниченности перемещения частиц вещества друг относительно друга.
Сопоставляя величины 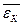 и U(r), можно судить о фазовых состояниях вещества:
и U(r), можно судить о фазовых состояниях вещества:
1) если 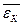 > |U(r)|, то вещество находится в газовом состоянии;
> |U(r)|, то вещество находится в газовом состоянии;
2) если 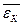 < |U(r)|, то вещество пребывает в твердом состоянии;
< |U(r)|, то вещество пребывает в твердом состоянии;
3) если 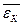 ~ U(r), то вещество — жидкость.
~ U(r), то вещество — жидкость.
Для твердого состояния тепловое движение частиц вещества ограничено колебаниями и вращениями, а поступательное движение отсутствует. Расстояние между частицами вещества в твердом состоянии постоянно; оно называется постоянной кристаллической решетки.
Для жидкого состояния при низких температурах преимущественными являются локализованные колебания, как у твердых тел. Скачкообразные поступательные перемещения отдельных частиц маловероятны. При высоких температурах в жидкостях доля частиц, которые могут совершать поступательные скачки на расстояние 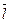 (где
(где 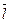 — средняя длина пробега), растет с ростом температуры Т, и при Т>ТК поступательная форма движения превалирует над колебательной.
— средняя длина пробега), растет с ростом температуры Т, и при Т>ТК поступательная форма движения превалирует над колебательной.
Для описания твердого состояния хороши модели потенциальных функций прямоугольной потенциальной ямы, гармонического осциллятора и модели Морзе (Ленарда—Джонса), для газообразного — модель идеального газа Сазерленда или потенциала Ленарда—Джонса (прил. II). Жидкости при низких температурах (близких к температуре замерзания) принято рассматривать как квазитвердое состояние с соответствующими модельными представлениями, а при высоких — как квазигазовое.
Энергетические характеристики вещества при молекулярно-кинетическом описании получают суммированием полной энергии (15.1) в расчете на одну частицу по числу частиц п, образующих систему:
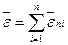 . (15.2)
. (15.2)
Эта величина используется для расчета теплоемкостей, поверхностного натяжения и т. д. Явления переноса (диффузия, вязкость, теплопроводность и т. д.) описываются, основываясь на особенностях движения частиц вещества в зависимости от фазового состояния, для каждой конкретной модели взаимодействия и значений параметров состояния (давления р и температуры Т).
Статистический способ описания является наиболее общим и универсальным способом описания состояния вещества. Он соединяет в себе как макроскопический, так и микроскопический (молекулярно-кинетический) подход. Основным понятием при статистическом подходе является функция распределения числа частиц по некоторому физическому параметру (чаще всего по энергиям, импульсам, либо скоростям движения). Функция распределения характеризует для частиц, образующих систему, вероятность того, что интересующий нас параметр имеет величину, лежащую в некотором определенном интервале значений, или характеризует долю от общего числа частиц, для которых значение интересующего нас параметра лежит в некотором определенном интервале.
Зная вид функции распределения, можно методами математической статистики определить средние значения физических величин, характеризующих вещество в целом.
Дата добавления: 2016-05-25; просмотров: 1242;
