Реакции ионного обмена — окислительно-восстановительная реакция, которая идет в направлении связывания ионов, но при которой не происходит изменения степеней окисления.
Условия течения реакций в растворах электролитов до конца:
1) в результате реакции выпадает осадок:
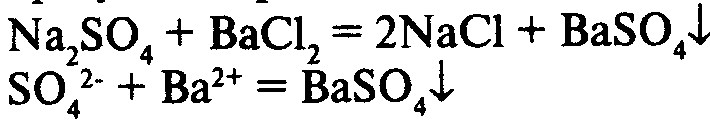
2) в результате реакции выделяется газ:
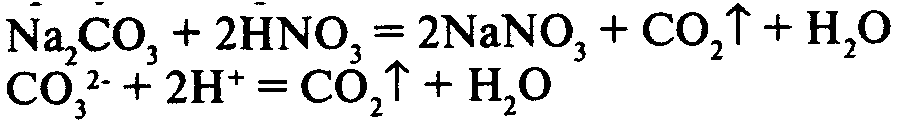
3) в результате реакции образуется малодиссоциирующее вещество:
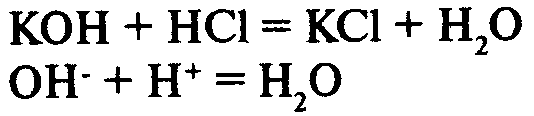
Ионный обмен – это процесс, в результате которого ионы, находящиеся в твердой фазе. обмениваются с ионами, находящимися в растворе. Нерастворимое твердое вещество может представлять собой какой-либо природный материал либо синтетическую смолу. Природные материалы, используемые для ионного обмена, включают цеолиты (комплексные алюмосиликаты натрия) и глауконитовый песок.
На поверхности этих твердых веществ имеются электрически заряженные центры, расположенные на более или менее регулярном расстоянии друг от друга. Эти центры удерживают на себе простые ионы с зарядами противоположного знака. Именно эти ионы обмениваются с другими ионами, содержащимися в растворе.
Катионообменники. Катионообменные материалы состоят из трех частей:
1) основная масса, или скелет, обычно обозначаемый символом R–;
2) активные центры (такие группы, как — 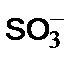 либо —
либо — 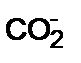 );
);
3) катионы, подлежащие обмену (обычно это ионы Н+ или Н3О+).
Когда твердый катионообменник приходит в соприкосновение с раствором, в котором содержатся какие-либо ионы, между ними устанавливается равновесие. Например,
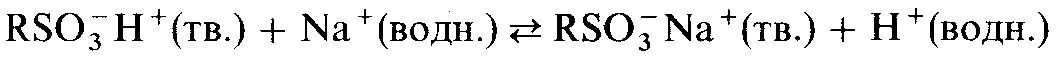
Если первоначально раствор содержит, например, хлорид натрия, то ионы натрия обмениваются с ионами водорода и из нижней части колонки вытекает разбавленный раствор соляной кислоты.
Ионообменный материал можно регенерировать (восстанавливать), промывая колонку разбавленной соляной кислотой. Это приводит к смещению влево рассматриваемого равновесия, в результате чего ионы натрия замещаются ионами водорода.
Анионообменники. Анионообменник удаляет из раствора анионы. Типичным примером анионного обмена является следующее равновесие:
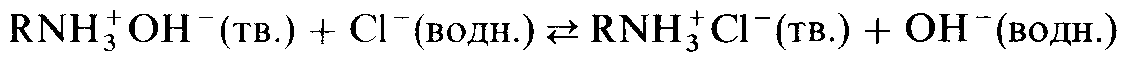
Для регенерации анионообменника может использоваться какое-либо основание, например раствор гидроксида натрия. Это сдвигает указанное равновесие влево.
Билет № 8
Сложные вещества состоят из двух или более химических элементов. Сложные вещества, или соединения, подразделяют на классы:
- Оксиды
- кислоты
- основания
- соли
Оксидами называют вещества, состоящие из двух элементов, один из которых кислород. Оксиды делят на оснóвные, кислотные, амфотерные, безразличные (несолеобразующие).
Оснóвным оксидам соответствуют основания. Это оксиды металлов, например натрия Na2O, кальция CaO. Основные оксиды реагируют с кислотами с образованием соли и воды.
Кислотным оксидам соответствуют кислоты. Это оксиды неметаллов, например, серы SO2, фосфора P2O5, или металлов в высшей степени окисления, например, оксид хрома (VI) CrO3. Кислотные оксиды реагируют со щелочами с образованием соли и воды.
Амфотерные оксиды реагируют и с кислотами, и со щелочами. Примером могут служить оксиды цинка и алюминия
.Несолеобразующие оксиды не реагируют ни с кислотами, ни со щелочами. К ним относятся некоторые оксиды неметаллов, например, оксид азота (II) NO.
Кислоты — это сложные вещества, состоящие из одного или нескольких атомов водорода и кислотного остатка.
Кислоты могут быть бескислородными, как соляная HCl, сероводородная H2S, или кислородсодержащими: азотная HNO3, серная H2SO4.
В зависимости от числа атомов водорода, кислоты делят на одноосно́вные, например, азотная HNO3, двухосно́вные — серная H2SO4, трехсно́вные — ортофосфорная (часто называют просто фосфорная) H3PO4.
С точки зрения теории электролитической диссоциации кислотами называются вещества, диссоциирующие в растворах с образованием ионов водорода:
HCl → H+ + Cl−
Основания — это сложные вещества, состоящие из металла и одной или нескольких гидроксогрупп (OH). Основания могут быть растворимыми в воде – щелочи: гидроксид натрия NaOH, гидроксид кальция Ca(OH)2, или нерастворимыми, как гидроксид меди (II) Cu(OH)2.
С точки зрения теории электролитической диссоциации основаниями являются вещества, диссоциирующие в растворах с образованием гидроксид-ионов, т.е. оснóвные гидроксиды:
NaOH → Na+ + OH−
С точки зрения протонной теории к основаниям относятся вещества, способные присоединять ионы водорода, например аммиак:
NH3 + HOH = NH4+ + OH−
Соли — это сложные вещества, в составе которых имеется металл (или сложный положительный ион) и кислотный остаток. Соли бывают:
• средние — в составе нет ионов водорода и гидроксогрупп, например, хлорид натрия NaCl, карбонат натрия Na2CO3
• кислые — содержат в своем составе ионы водорода, например, гидрокарбонат натрия NaHCO3, дигидрофосфат натрия NaH2PO4
• оснóвные — содержат в своем составе гидроксогруппы, например, основный карбонат меди (II) (CuOH)2CO3
Билет №9.
Металлы составляют большую часть химических элементов. Каждый период периодической системы (кроме 1-го) химических элементов начинается с металлов, причем с увеличением номера периода их становится все больше. Если во 2-м периоде металлов всего 2 (литий и бериллий), в 3-м — 3 (натрий, магний, алюминий), то уже в 4-м — 13, а в 7-м — 29.
Атомы металлов имеют сходство в строении внешнего электронного слоя, который образован небольшим числом электронов (в основном не больше трех).
Это утверждение можно проиллюстрировать на примерах Na, алюминия А1 и цинка Zn. Составляя схемы строения атомов, по желанию можно составлять электронные формулы и приводить примеры строения элементов больших периодов, например цинка.
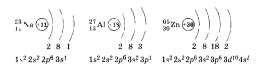
В связи с тем что электроны внешнего слоя атомов металлов слабо связаны с ядром, они могут быть «отданы» другим частицам, что и происходит при химических реакциях:
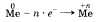
Свойство атомов металлов отдавать электроны явтяется их характерным химическим свойством и свидетельствует о том, что металлы проявляют восстановительные свойства.
При характеристике физических свойств металлов следует отметить их общие свойства: электрическую проводимость, теплопроводность, металлический блеск, пластичность, которые обусловлены единым видом химической связи — металлической, и металлической кристаллической решетки. Их особенностью является наличие свободноперемещаю-щихся обобществленных электронов между ион-атомами, находящимися в узлах кристаллической решетки.
При характеристике химических свойств важно подтвердить вывод о том, что во всех реакциях металлы проявляют свойства восстановителей, и проиллюстрировать это записью уравнений реакции. Особое внимание следует обратить на взаимодействие металлов с кислотами и растворами солей, при этом необходимо обратиться к ряду напряжений металлов (ряд стандартных электродных потенциалов).
Примеры взаимодействия металлов с простыми веществами (неметаллами): 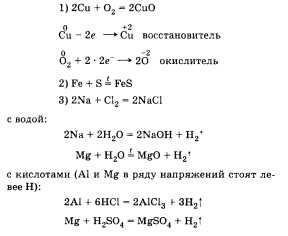
с солями (Zn в ряду напряжений стоит левее Сu): Zn + СuС12 = ZnCl2 + Сu!
Таким образом, несмотря на большое многообразие металлов, все они обладают общими физическими и химическими свойствами, что объясняется сходством в строении атомов и строении простых веществ.
Билет №10.
Ответ следует начать с характеристики положения неметаллов в периодической системе: если провести воображаемую диагональ от бериллия Be к астату At, то неметаллы расположатся в главных подгруппах выше диагонали (т. е. в верхнем правом углу). К неметаллам относятся также водород Н и инертные газы.
Далее важно отметить, что для общей характеристики неметаллов необходимо обратить внимание на строение их атомов, на то, как распределяются электроны по электронным слоям и сколько электронов приходится на внешний электронный слой. Можно привести строение атомов углерода С, азота N, кислорода О, фтора F. Это позволит сделать вывод о том, что по мере увеличения порядковых номеров атомов элементов и накопления электронов на внешнем слое у неметаллов одного периода усиливается способность принимать электроны от других атомов на свой внешний слой, т. е. неметаллические свойства элементов в периодах увеличиваются.
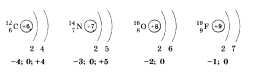
Рассматривая изменение свойств неметаллов при движении по группе, следует отметить, что они ослабевают. Это связано с увеличением расстояния от ядра до внешнего слоя, а следовательно, уменьшением способности ядра притягивать к себе электроны от других атомов. Для подтверждения этого вывода рассмотрим VI группу. В начале ее расположен кислород О — типичный неметалл, а заканчивается группа полонием Ро, обладающим свойствами металла.
Далее следует перейти к рассмотрению физических свойств неметаллов. Следует отметить, что простые вещества — неметаллы могут иметь как атомное (Si, В), так и молекулярное (Н2, N2, Br2) строение. Поэтому среди неметаллов есть газы (О2, С12), жидкости (Вг2), твердые вещества (С, 12). Большинство неметаллов не электропроводны, имеют низкую теплопроводность, а твердые вещества непластичны.
Переходя к характеристике химических свойств, необходимо отметить, что более типичным для неметаллов является процесс принятия электронов. В этом отличие химических свойств неметаллов от химических свойств металлов. Это положение можно подтвердить взаимодействием неметаллов с простыми веществами. При этом следует записать уравнения соответствующих химических реакций и объяснить их сущность с точки зрения процессов окисления — восстановления. Следует отметить, что неметаллы могут проявлять свойства как окислителей, так и восстановителей. Приведем примеры.

Можно добавить, что некоторые неметаллы могут реагировать и со сложными веществами (оксидами, кислотами, солями). Следующие уравнения учащийся приводит по желанию:
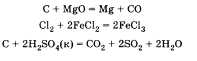
Билет №11.
Аллотропия веществ, состав, строение, свойства аллотропных модификаций.
Если какой-либо элемент может существовать в двух или нескольких твердых формах (кристаллических либо аморфных), то считается, что он проявляет аллотропию. Различные формы одного элемента называются аллотропами. Аллотропы существуют приблизительно у половины всех элементов.
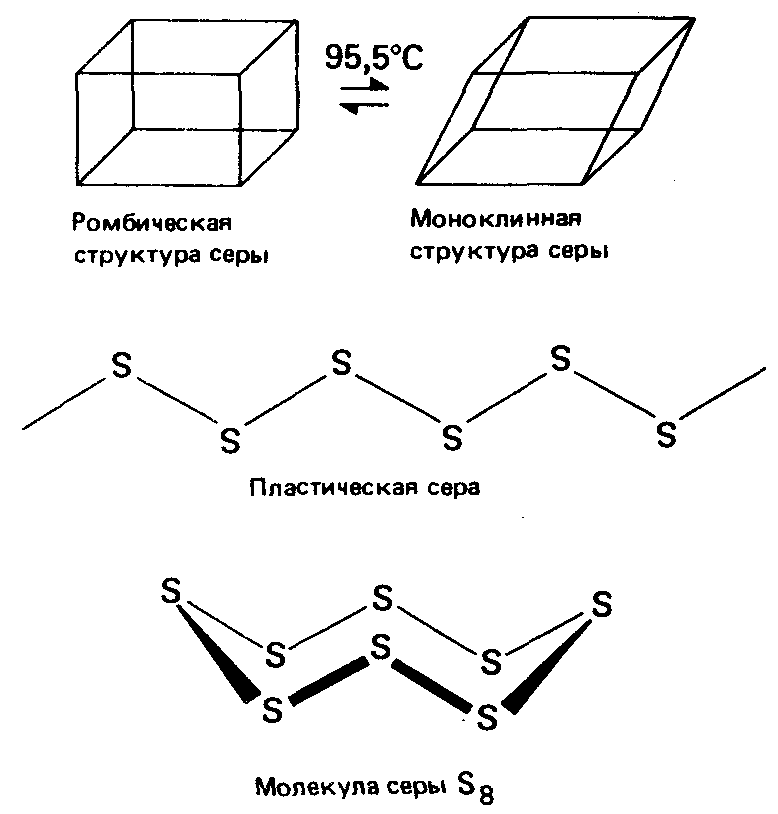
Например, углерод существует в виде алмаза либо графита. Сера существует в двух кристаллических формах - ромбической и моноклинной - в зависимости от температуры. Обе ее кристаллические формы являются примерами молекулярных кристаллов. Молекулы в них представляют собой гофрированные циклы, в каждом из которых содержится по восемь ковалентно связанных атомов серы. Твердая сера может существовать еще в третьей аллотропной форме как пластическая сера. Эта форма серы неустойчива. Она состоит из длинных цепочек атомов серы, которые при комнатной температуре разрушаются и снова образуют молекулы S8, кристаллизующиеся в ромбическую решетку.
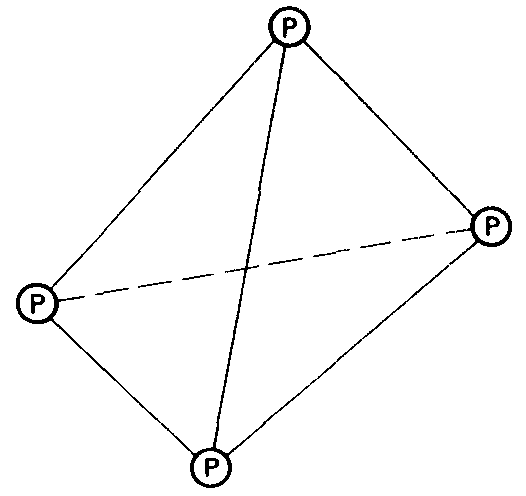
Фосфор может существовать в трех аллотропных формах. Наиболее устойчивая из них-красный фосфор. Красный фосфор имеет каркасную кристаллическую структуру, в которой каждый атом ковалентно связан с тремя другими атомами фосфора. Белый фосфор представляет собой молекулярный кристалл. Каждая его молекула содержит четыре атома фосфора, ковалентно связанных в тетраэдричес-кую структуру. Третий аллотроп - черный фосфор - образуется только при высоких давлениях. Он существует в виде макромолекулярной слоистой структуры.
Билет №12.
Электрохимический ряд напряжений - вытеснение водорода металлами.
Металлы различаются химической активностью. Металлы расположены в порядке убывания активности в ряду напряжений:
Li, К, Ca, Na, Mg, Al, Mn, Zn, Fe, Co, Ni, Sn, Pb, H2, Cu, Hg, Ag, Au
Активные металлы (от лития до свинца) восстанавливают водород из кислот, неактивные (от меди до золота) – не восстанавливают.
Испытаем четыре металла: магний Mg, алюминий Al, железо Fe и медь Cu. Приготовим пробирки с раствором соляной кислоты (HCl) и погрузим в них металлы. Медь не реагирует с раствором соляной кислоты. Железо медленно восстанавливает водород из раствора кислоты. Алюминий более активно реагирует с раствором соляной кислоты, восстанавливая водород.
Наиболее энергично восстанавливает водород из соляной кислоты магний. Мы увидели, что металлы, стоящие в электрохимическом ряду напряжений до водорода (железо, алюминий и магний), восстанавливают его из растворов кислот.
Металлы, стоящие в ряду после водорода (в нашем опыте – медь), не восстанавливают его из кислот. Наиболее активным металлом в нашем опыте оказался магний, наименее активным ‑ медь.
2 HCl + Mg = MgC12 + H2
2 HCl + Fe = FeC12 + H2
6 HCl + 2Al = 2 A1C13 + 3H2
Активные металлы вытесняют менее активные из растворов их солей. В первой пробирке – медь (Cu) и раствор соли менее активного металла – серебра (AgNO3). Вторая пара – железо (Fe) и раствор соли меди (CuSO4). Железо активнее меди. В третьей пробирке – цинк (Zn) и раствор соли менее активного свинца ‑ Pb(NO3)2. В пробирках начинаются реакции. Через некоторое время посмотрим, что получилось в пробирках. Медь покрылась белыми кристаллами серебра:
2AgNO3 + Cu = Cu(NO3)2 + 2 Ag
На железном гвозде появился розовый налет металлической меди:
CuSO4 + Fe = FeSO4 + Cu
Цинк покрылся рыхлым слоем металлического свинца:
Pb(NO3)2 + Zn = Pb + Zn (NO3)2
Мы убедились в том, что активные металлы вытесняют менее активные из растворов их солей.
Билет №13.
Дата добавления: 2016-05-11; просмотров: 1979;
