Виды химической связи и способы ее образования в неорганических соединениях: ковалентная (полярная, неполярная, простые и кратные связи), ионная, водородная.
Ковалентная связь образуется за счет перекрывания электронных облаков двух атомов. Каждый атом предоставляет один неспаренный электрон для образования одной химической связи, при этом происходит образование общей электронной пары. Если ковалентная связь образуется между двумя одинаковыми атомами, она называется неполярной.
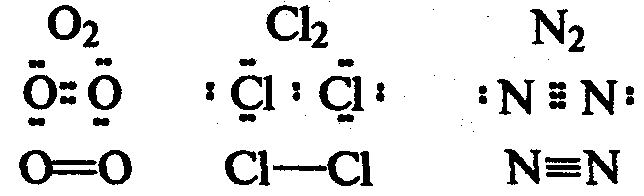
Если ковалентная связь образуется между двумя различными атомами, общая электронная пара смещайся к атому с большей электроотрицательностью (электроотрицательностью называется способность атома притягивать электроны). В этом случае возникает полярная ковалентная связь.
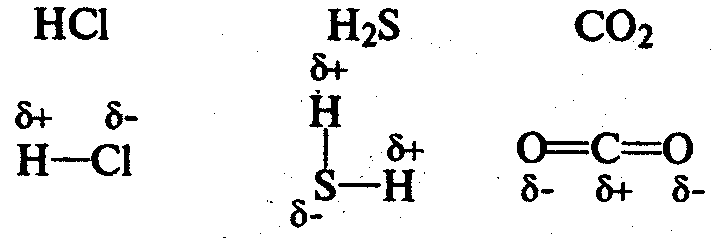
Частным случаем ковалентной связи является донорно-акцепторная связь. Для ее образованья у одного атома должна быть свободная орбиталь на внешнем электронном уровне, а у другого — пара электронов. Один атом (донор) предоставляет другому (акцептору) свою электронную пару, в результате она становится общей, образуется химическая связь. Пример — молекула СО:
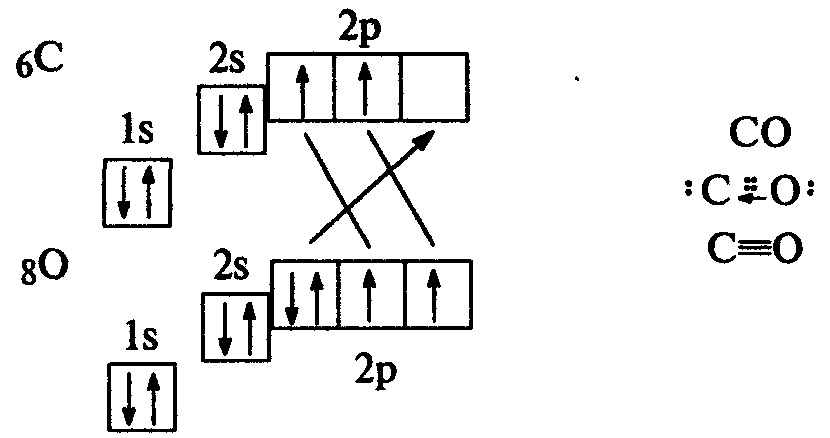
Ионная связь образуется между атомами с сильно отличающейся электроотрицательностью. При этом один атом отдает электроны и превращается в положительно заряженный ион, а атом, получивший электроны, в отрицательно заряженный. Ионы удерживаются вместе за счет сил электростатического притяжения.
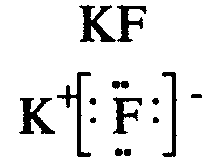
Водородная связь образуется между полярными молекулами (вода, спирты, аммиак) за счет притяжения разноименных зарядов.
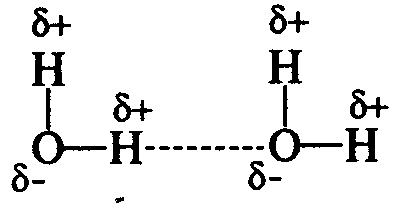
Прочность водородной связи существенно (~20 раз) меньше, чем ионной или ковалентной связи.
Дата добавления: 2016-05-11; просмотров: 3460;
