Законы, описывающие поведение идеальных газов — законы Бойля-Мариотта, Авогадро, Дальтона, Гей-Люссака.
 5. Закон Бойля-Мариотта.
5. Закон Бойля-Мариотта.
Для данной массы газа m при постоянной температуре Т произведение давления р на объем V есть величина постоянная: pV = const при Т = const и m = const
Кривая, изображающая зависимость между р и V, характеризующая свойства вещества при постоянной температуре, называется изотермой.Изотермы — гиперболы, расположенные на графике тем выше, чем выше температура происходящего процесса.
6. Закон Авогадро,
Количество вещества V— физическая величина, определяемая числом специфических структурных элементов — молекул, атомов или ионов, из которых состоит вещество.
Единица количества вещества — моль— количество вещества системы, содержащей столько же структурных элементов, сколько содержится в 0,012 кг изотопа углерода 12С.
| В одном моле различных веществ содержится одно и то же число молекул NА, называемое числомАвогадро. | 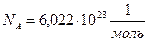
|
Закон Авогадро: моли любых газов при одинаковой температуре и давлении занимают одинаковые объемы.
| При нормальных условиях (Т = Т0, р = р0) этот объемVμ (молярный объем)равен: | 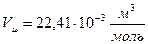
|
Молярная масса 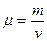 — это масса одного моля вещества. Отсюда:
— это масса одного моля вещества. Отсюда: 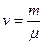
Дата добавления: 2016-04-22; просмотров: 963;
