Образование ацетиленидов металлов
Атом водорода в алкинах-1 обладает повышенной подвижностью и способен в присутствии сильных оснований отщепляться в виде протона и замещаться на ион металла. Образующиеся продукты замещения – ацетилениды металлов – выпадают в осадок, могут быть выделены, а действием раствора HCl исходный алкин регенерируется:
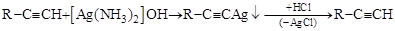 .
.
алкин-1 реактив ацетиленид алкин-1
Толленса серебра
Аналогично протекает такая реакция с аммиачным раствором CuCl.
Ацетилениды серебра и меди (1) применяются для разнообразных синтезов, например:

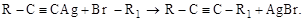
В сухом виде ацетилениды Ме взрываются от удара.
2. Присоединение ацетилена:
(а) к оксосоединениям – синтезы А.Е. Фаворского (1860–1945)




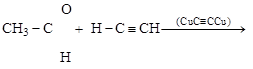
ацетальдегид






алкинол алкиндиол [гексин-3-диол-2,5]
Один из примеров промышленного применения синтеза Фаворского – получение изопрена из ацетилена и ацетона:
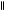





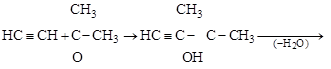
ацетилен ацетон [3-метилбутин-1-ол-3]

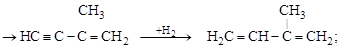
[2-метилбутен-1-ин-3] изопрен
(б) к диенам (диеновые синтезы Дильса–Альдера)
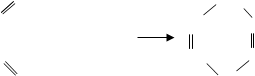
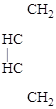 +
+ 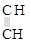
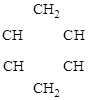 .
.
дивинил ацетилен [циклогексадиен-1,4]
 5.2.5. Реакции полимеризации
5.2.5. Реакции полимеризации
а) 
винилацетилен (димер)
Присоединение HCl к винилацетилену дает хлоропрен
H2C = CCl – CH = CH2, идущий на получение хлоропренового каучука.
 б)
б) 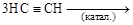 бензол (тример);
бензол (тример);
в) 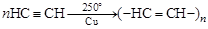 купрен (полимер).
купрен (полимер).
Купрен – желтый аморфный порошок с очень низкой теплопроводностью; применяется в качестве теплоизоляционного материала.
г) окислительная поликонденсация ацетилена объясняется повышенной подвижностью ацетиленидного водорода:
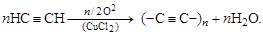
карбин
Карбин считают третьим (после графита и алмаза) аллотропным состоянием углерода. Выдерживает нагрев до 2500 ºС.
5.3. Получение алкинов
Карбидный способ
СаС2 + 2Н2О ® НС º СН + Са(ОН)2.
карбид кальция ацетилен
Реакция протекает энергично при стандартных условиях и широко используется в технике.
2. Термический крекинг углеводородов
Основное сырье – алканы (от метана до бутана включительно).
(а) 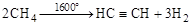 ;
;
(б) 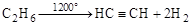 .
.
Дата добавления: 2016-04-14; просмотров: 1693;
