Кислородный эффект в радиобиологии и его механизмы.
Кислородным эффектом в радиобиологии называют явление усиления поражающего действия ионизирующего излучения в присутствии кислорода в момент облучения. То есть кислород проявляет радиосенсибилизирующее действие, является радиосенсибилизатором. Однако на практике часто приходится обсуждать не сенсибилизирующие свойства кислорода, а радиозащитное действие гипоксии. Кислородный эффект наблюдается при облучении различных объектов — целых организмов, клеток и простых модельных систем. Для количественной оценки кислородного эффекта используют величину ФИД (фактор изменения дозы), который в данном случае называют также коэффициентом кислородного усиления (ККУ). ККУ при облучении животных рассчитывается как отношение ЛД50 в условиях гипоксии к ЛД50 в нормальных условиях: (17.2.1) 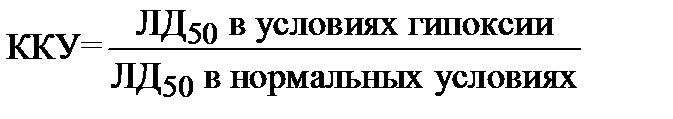 . Кривая гибели животных после облучения в условиях гипоксии сдвигается в область более высоких доз как показано. (17.2.2)
. Кривая гибели животных после облучения в условиях гипоксии сдвигается в область более высоких доз как показано. (17.2.2)
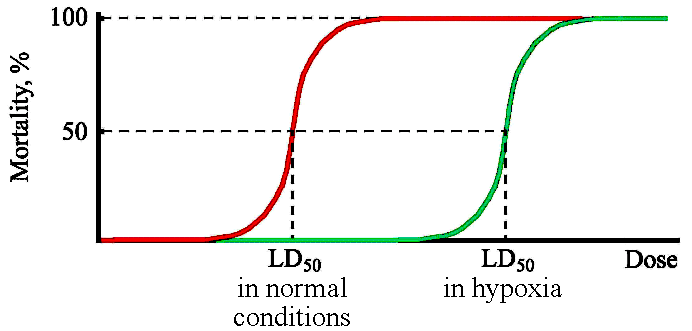
При облучении животных заметное снижение радиочувствительности, по сравнению с нормальным атмосферным воздухом, наблюдается примерно при 10%-ном содержании кислорода и ниже. Максимальный ФИД при гипоксии для животных не превышает 2. Длительность кислородного эффекта у животных невелика, т.е. защитное действие гипоксии снижается при длительном нахождении в гипоксических условиях. При облучении клеток, микроорганизмов и макромолекул ККУ рассчитывается как отношение доз, вызывающих одинаковый радиобиологический эффект в условиях гипоксии (или аноксии) и при нормальной аэрации. Часто для определения ККУ используется соотношение доз D0 в условиях гипоксии (или аноксии) к D0 в нормальных условиях: (17.2.3) 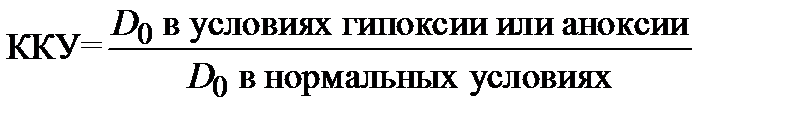 .
.
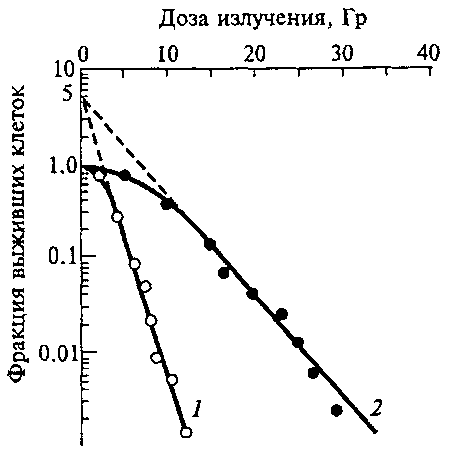
Кривые выживаемости клеток китайского хомячка, облученных на воздухе и в азоте. Как видно из рисунка, для снижения фракции выживших клеток до 0.01 (1%) от исходной при облучении на воздухе потребовалась доза 8.9 Гр, а при облучении в аноксии (отсутствие кислорода) – 25 Гр. Величина D0 равна 1.5 и 4.5 Гр, соответственно. Таким образом, кислород повысил радиочувствительность клеток в 2.8 раза (25/8.9 = 2.8), т.е. он сенсибилизировал клетки с ФИД = 2.8. (17.2.4)
Наиболее четко кислородный эффект наблюдается при облучении редкоионизирующими излучениями, т.е. когда линейная плотность ионизации (ЛПИ) низкая. С увеличением ЛПИ кислородный эффект быстро уменьшается и полностью отсутствует при α‑облучении, характеризующимся высокой ЛПИ. Представлены различные варианты проявления кислородного эффекта в зависимости от применяемого вида ионизирующего излучения. Как видно из рисунка, самая высокая величина ККУ = 2.5 наблюдается при действии рентгеновского излучения. (17.2.5)
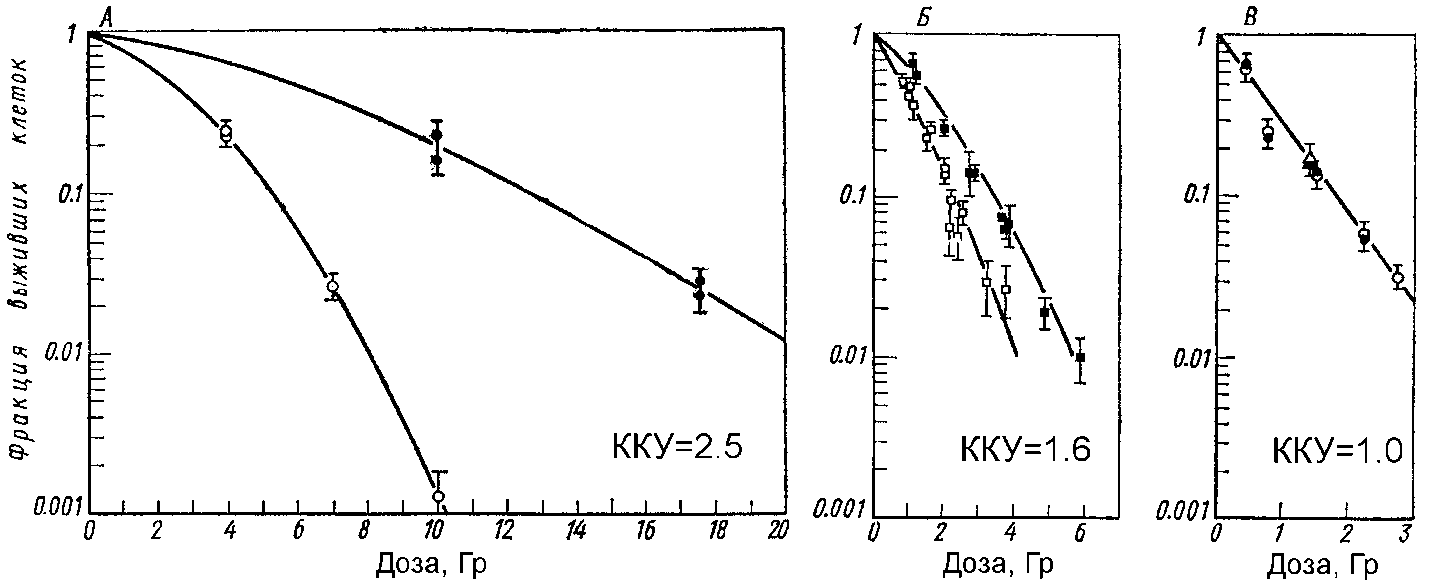
А – рентгеновское излучение, Б – нейтронное излучение (15 МэВ), В – a-излучение
Кислородный эффект был обнаружен не только на клеточном и организменном уровне, но и в экспериментах с биологическими макромолекулами. Основные результаты по кислородному эффекту были получены главным образом с ферментами и нуклеиновыми кислотами, причём наиболее важные и однозначные данные были получены по инактивации ферментов. Кислородный эффект почти всегда наблюдается при облучении сухих ферментов. Результаты по инактивации РНК-азы при g-облучении в вакууме и присутствии кислорода. В этих экспериментах ККУ = 2.1. (17.2.6)
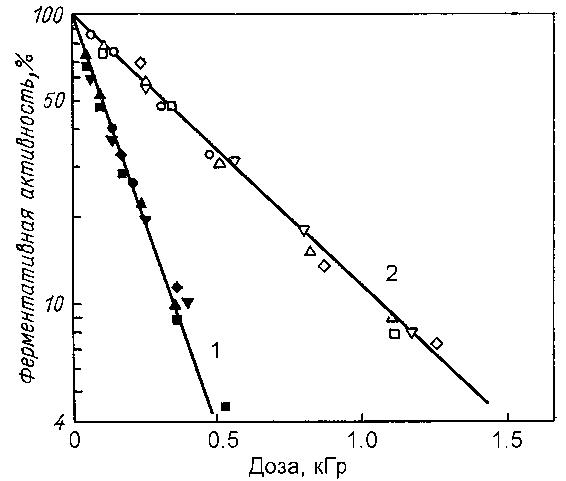
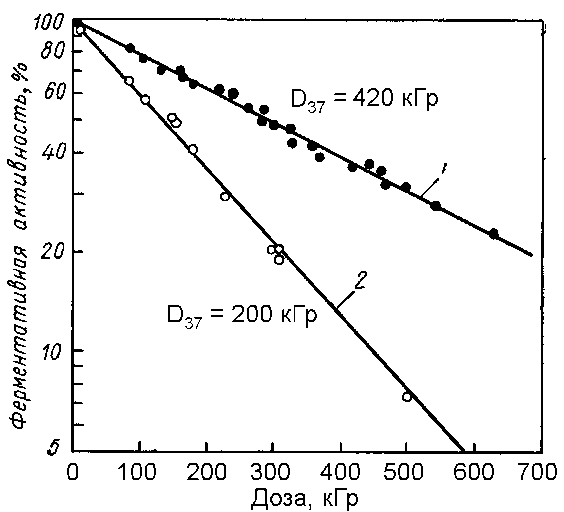 Однако, при облучении макромолекул в разбавленных водных растворах, т.е. в условиях, когда преобладает непрямое действие, кислородный эффект может быть очень слабым или полностью отсутствовать. Более того, в разбавленных растворах макромолекул возможен даже защитный эффект кислорода (т.н. обратный кислородный эффект), что было продемонстрировано, например, при облучении растворов трипсина: его радиочувствительность в атмосфере азота была в три раза выше, чем в кислородной среде: (17.2.7)
Однако, при облучении макромолекул в разбавленных водных растворах, т.е. в условиях, когда преобладает непрямое действие, кислородный эффект может быть очень слабым или полностью отсутствовать. Более того, в разбавленных растворах макромолекул возможен даже защитный эффект кислорода (т.н. обратный кислородный эффект), что было продемонстрировано, например, при облучении растворов трипсина: его радиочувствительность в атмосфере азота была в три раза выше, чем в кислородной среде: (17.2.7)
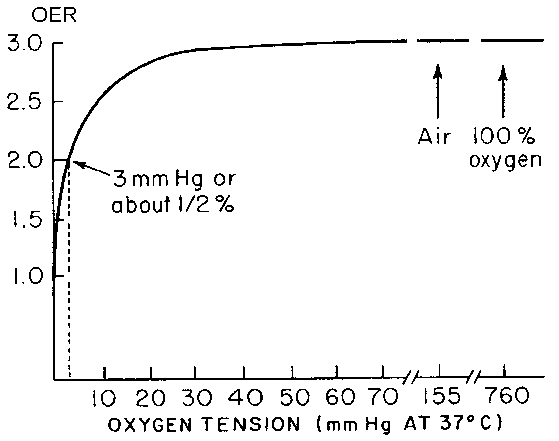
 На клеточном уровне зависимость кислородного эффекта от концентрации кислорода подробна была исследована Греем - эксперименты проводились на дрожжах, бактериях и клетках млекопитающих в культуре. Графическое изображение этой зависимости: по оси ординат откладывается ККУ, по оси абсцисс – парциальное давление кислорода. В воздухе ККУ равен примерно 3 (т.е. радиочувствительность уже максимальна) и не возрастает при повышении концентрации кислорода. При снижении концентрации кислорода со 159 мм рт. ст. (воздух) до 30 мм рт. ст. ККУ снижается очень незначительно. А вот в диапазоне от 20 мм рт. ст. до 0 мм рт. ст. ККУ снижается очень резко. При парциальном давлении кислорода 3 мм рт. ст. ККУ равен примерно 2. (17.2.8)
На клеточном уровне зависимость кислородного эффекта от концентрации кислорода подробна была исследована Греем - эксперименты проводились на дрожжах, бактериях и клетках млекопитающих в культуре. Графическое изображение этой зависимости: по оси ординат откладывается ККУ, по оси абсцисс – парциальное давление кислорода. В воздухе ККУ равен примерно 3 (т.е. радиочувствительность уже максимальна) и не возрастает при повышении концентрации кислорода. При снижении концентрации кислорода со 159 мм рт. ст. (воздух) до 30 мм рт. ст. ККУ снижается очень незначительно. А вот в диапазоне от 20 мм рт. ст. до 0 мм рт. ст. ККУ снижается очень резко. При парциальном давлении кислорода 3 мм рт. ст. ККУ равен примерно 2. (17.2.8)
В 1956 г. Альпер и Говард-Фландерс высказали гипотезу о механизме кислородного эффекта, включающую несколько положений: а) в результате облучения мишени образуется ее активированное состояние; б) это активированное состояние мишени существует в течение очень короткого времени (несколько миллисекунд, не превышает 20 мс), а затем мишень возвращается в стабильное состояние (т.е. восстанавливается); в) в активированном состоянии мишень является очень реакционноспособной по отношению к кислороду; г) если во время облучения в среде присутствует кислород, то мишень в активированном состоянии взаимодействует с ним с образованием перекиси (точнее — гидроперекиси), т.е. происходит пероксидация мишени, д) пероксидация мишени приводит к потере ее функциональных свойств (например, ферментативной активности и т.д.) и затрудняет ее репарацию или вовсе делает ее невозможной. Повреждение становится нерепарируемым. Иными словами, кислород закрепляет («фиксирует») повреждение мишени, в связи с чем описанную гипотезу о механизме кислородного эффекта называют также «гипотезой кислородной фиксации».
Схема механизма кислородного эффекта: (17.2.9)
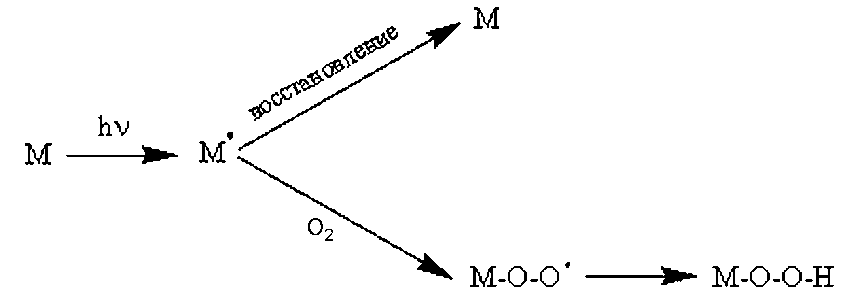
Как видно из рисунка, кислородный эффект отражает конкуренцию между процессами восстановления и необратимой пероксидаций первичных повреждений мишени. Нерепарируемые повреждения мишени могут возникать и без участия кислорода. Считают, что при действии облучения на мишень возможно появление 2‑х типов повреждений: а) повреждения I типа — потенциально летальные повреждения (скрытые), могут стать явными (летальными), если провзаимодействуют с кислородом и станут нерепарируемыми, т.е. лучевые повреждения фиксируются кислородом; б) повреждения II типа — летальные всегда, их образование не зависит от наличия кислорода. Основываясь на предложенной гипотезе кислородного эффекта вывели уравнение, которое описывает кривую зависимости ККУ от концентрации кислорода: (17.2.10)
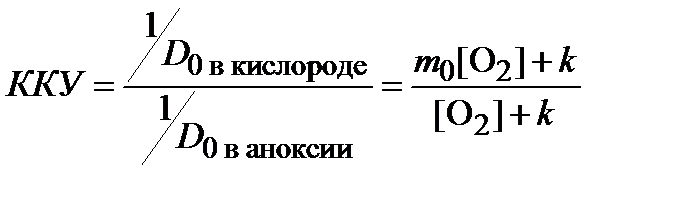 ,
,
где D0 в кислороде и D0 в аноксии – величины, характеризующие радиочувствительность при изучаемой концентрации кислорода [O2] и в аноксии, соответственно; m0 — максимальное значение ККУ, наблюдаемое при облучении клеток в условиях полной оксигенации; k — константа, зависящая от типа клеток.
Кислородный эффект не наблюдается в разбавленных водных растворах макромолекул или даже наблюдается обратный кислородный эффект, причина. В разбавленных водных растворах преобладает непрямое действие радиации на растворенные макромолекулы, т.е. макромолекулы повреждаются, в основном, радикалами воды, образующимися при ее радиолизе. В водных растворах О2 взаимодействует, главным образом, с радикалами водорода (Н•) и гидратированными электронами (е-aq), а не с радикалами макромолекул.
При этом возможны следующие варианты: а) если радикалы водорода Н• и гидратированные электроны е-aq вносят наибольший вклад в поражение макромолекулы, то их перехват кислородом снизит радиационный эффект, оказанный ими на макромолекулы — т.е. будет наблюдаться защитный эффект кислорода, т.н. обратный кислородный эффект; б) если макромолекулы повреждаются главным образом гидроксильным радикалом ОН•, то кислород, перехватывая радикалы водорода Н•, уменьшает рекомбинацию Н• + ОН• → Н2О и, таким образом, увеличивает концентрацию ОН• и усиливает радиационный эффект. Кислородный эффект при повышении ЛПИ излучения снижается потому, что повышается доля летальных повреждений, проявление которых не зависит уже от кислорода (повреждения II типа). Знание причин возрастания устойчивости клеток в условиях гипоксии имеет огромное значение при радиотерапии злокачественных образовании. Известно, что цель радиотерапии опухолей — убить опухолевые клетки и как можно меньше повредить нормальные ткани, окружающие опухоль. Однако в обычных условиях применению облучения для удаления опухоли препятствует тот факт, что опухолевая ткань является более устойчивой, чем нормальная ткань. Это связано с тем, что обычно в нормальных тканях парциальное напряжение кислорода (рО2) составляет 40‑60 мм рт.ст. В опухолях же, которые, как известно, снабжаются кровью значительно хуже, чем нормальные ткани, напряжение кислорода значительно ниже и поэтому и радиоустойчивость опухолей значительно выше, чем у нормальных тканей.
Однако в опухолевой ткани напряжение кислорода находится в той области, где даже при небольшом увеличении концентрации кислорода радиочувствительность может существенно повыситься : (17.2.11)
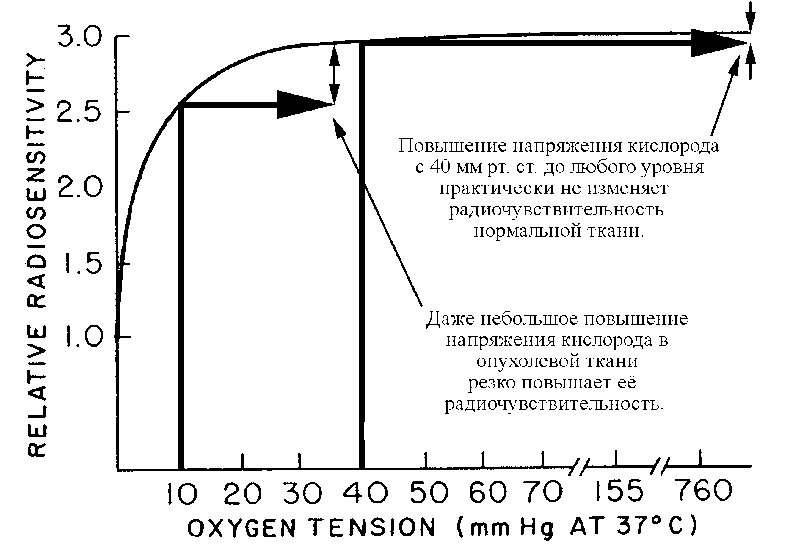 Именно этот эффект используется при радиотерапии опухолей. При повышении содержания О2 во вдыхаемом воздухе происходит увеличение концентрации О2 как в нормальных тканях, так и в опухоли. Однако повышение содержания кислорода практически не вызывает увеличение радиочувствительности нормальных тканей, но приводит к значительному увеличению радиочувствительности опухоли. Для этой цели применяют гипербарическую оксигенацию (вдыхание чистого кислорода под давлением 2‑3 атм.). Однако, надо отметить, что этот метод далеко не всегда повышает рО2 в опухолевой ткани. Другим подходом практического применения кислородного эффекта в радиотерапии опухолей является использование феномена реоксигенации опухолевых клеток. Ван Путтен и Каллман показали, что популяция опухолевых клеток состоит из гипоксических и аэрированных, т.е. негипоксических клеток. Обычно всего лишь 15% клеток являются гипоксическими. При действии облучения на такую популяцию гибнут в первую очередь аэрированные клетки, т.к. они более радиочувствительные. Однако в экспериментах было обнаружено, что через определённый интервал времени после облучения популяция опухолевых клеток восстанавливает соотношение гипоксических и оксигенированных клеток на первоначальном уровне, т.е опять доля гипоксических клеток снижается до 15%. Таким образом, происходит реоксигенация клеток и появление радиочувствительной аэрированной фракции клеток, что позволяет опять эффективно применить ионизирующее излучение для их уничтожения.
Именно этот эффект используется при радиотерапии опухолей. При повышении содержания О2 во вдыхаемом воздухе происходит увеличение концентрации О2 как в нормальных тканях, так и в опухоли. Однако повышение содержания кислорода практически не вызывает увеличение радиочувствительности нормальных тканей, но приводит к значительному увеличению радиочувствительности опухоли. Для этой цели применяют гипербарическую оксигенацию (вдыхание чистого кислорода под давлением 2‑3 атм.). Однако, надо отметить, что этот метод далеко не всегда повышает рО2 в опухолевой ткани. Другим подходом практического применения кислородного эффекта в радиотерапии опухолей является использование феномена реоксигенации опухолевых клеток. Ван Путтен и Каллман показали, что популяция опухолевых клеток состоит из гипоксических и аэрированных, т.е. негипоксических клеток. Обычно всего лишь 15% клеток являются гипоксическими. При действии облучения на такую популяцию гибнут в первую очередь аэрированные клетки, т.к. они более радиочувствительные. Однако в экспериментах было обнаружено, что через определённый интервал времени после облучения популяция опухолевых клеток восстанавливает соотношение гипоксических и оксигенированных клеток на первоначальном уровне, т.е опять доля гипоксических клеток снижается до 15%. Таким образом, происходит реоксигенация клеток и появление радиочувствительной аэрированной фракции клеток, что позволяет опять эффективно применить ионизирующее излучение для их уничтожения.
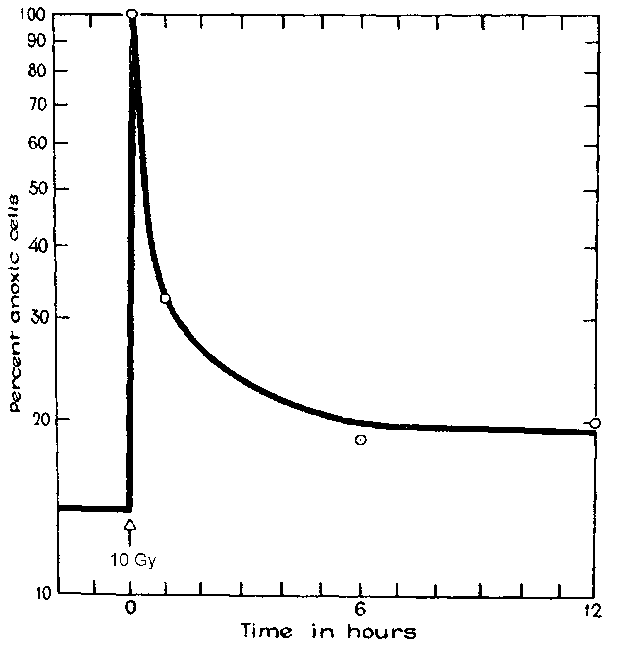
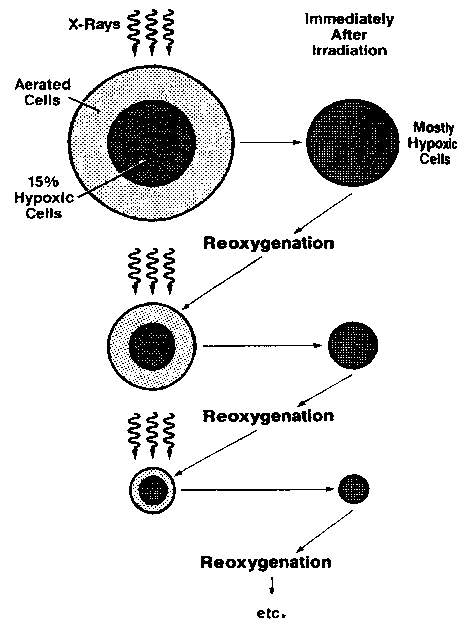
Надо отметить, что определяющим фактором для успешного применения ионизирующего излучения против опухолевых клеток является подбор того временного интервала, который необходим для реоксигенации клеток, т.е. выбрать достаточный промежуток времени между фракциями облучения. Показано, что время полной реоксигенации для различных видов опухолевых клеток может существенно различаться: для одних клеток – оно может быть около 6 часов и меньше (быстрая реоксигенация), а для других – 1-3 суток и более (медленная реоксигенация). Представлена зависимость процесса реоксигенации клеток саркомы у мышей от времени после облучения в дозе 10 Гр. Как видно, сразу после облучения в дозе 10 Гр популяция клеток состоит только из гипоксических клеток, однако через 6 часов в результате процесса реоксигенации доля гипоксических клеток в популяции значительно уменьшается и выходит на стационарный уровень. Таким образом, для данного вида опухолевых клеток повторное облучение можно проводить уже через 6 часов. Клиническими исследованиями было доказано, что у большинства опухолей процесс реоксигенации длится 1-2 суток, что и определяет график проведения фракционированного облучения. Еще представлена схема проведения фракционированного облучения опухолевых клеток с учётом процесса реоксигенации. (17.2.12) (17.2.13)
| 
|
Как видно из рисунка, ионизирующее излучение вызывает гибель аэрированных клеток, так как они более радиочувствительные, после чего в популяции остаются только устойчивые гипоксические клетки. Однако после процесса реоксигенации в опухоли восстанавливается первоначальное соотношение между аэрированными и гипоксическими клетками, что позволяет опять эффективно применить облучение. И так несколько раз до полного уничтожения опухоли. Доказано, что радиотерапия неэффективна в отношении тех опухолей, в которых процесс реоксигенации не наблюдается.
Дата добавления: 2016-04-11; просмотров: 5311;
