Вращательная и трансляционная подвижность фосфолипидов. Латеральная диффузия мембранных липидов.
Гидрофобный эффект, объединяющий молекулярные компоненты в мембранах, препятствует их выходу в водную фазу за пределы мембраны. В то же время силы межмолекулярного взаимодействия не мешают молекулам в мембранах обмениваться друг с другом местами, поскольку площадь контакта между водой и гидрофобными участками молекул при этом практически не изменяется. Вследствие этого молекулярные компоненты в мембранных системах сохраняют индивидуальную подвижность и могут диффузионным путем передвигаться в пределах мембран.
Условно выделяют три типа электростатических взаимодействий в мембранных системах: латеральное, или тангенциальное взаимодействие заряженных групп молекул, которые расположены в одном полуслое мембран; трансмембранное взаимодействие заряженных групп, расположенных по разные стороны мембраны; межмембранное взаимодействие заряженных групп, расположенных на поверхности 2 соседних мембран.
Дисперсионные вандерваальсовы взаимодействия между поверхностями мембран обнаруживаются на расстояниях до 1000 А. Это намного превышает расстояния, где проявляется электростатическое отталкивание. Суммарный эффект этих сил может привести к появлению минимума энергии взаимодействия на расстояниях 30 - 80 А и слиянию поверхностей клеточных мембран. Этот эффект лежит в основе объединения отдельных клеток в клеточные агрегаты. Компоненты клеточных мембран характеризуются определенной подвижностью.
Молекулы липидов легче всего совершают вращательное движение вокруг своей длинной оси. Время поворота на угол, равный 1 рад, в жидком состоянии ~ 10-9 с и увеличивается до 10-8 с при температуре ниже точки плавления жирнокислотных цепей липидов.
Диффузионное перемещение молекул липидов вдоль слоя, обычно называемое латеральной диффузией, также совершается достаточно быстро. Коэффициент латеральной диффузии молекул фосфолипидов, жирных кислот в природных мембранах составляет Д ~ 10-7 -10-8 с. Молекула липида за 1 с перемещается по мембране на расстояние порядка 5000 нм, т. е. может «обежать» всю плазматическую мембрану таких клеток, как эритроцит. Скорость латеральной диффузии зависит от липидного состава мембран и температуры. Так, холестерин, добавленный к яичному лецитину, снижает скорость латеральной диффузии более чем в два раза. При температурах ниже точки плавления углеводородных цепей липида константа латеральной диффузии снижается на порядок.
Молекулы белков в мембранах также проявляют диффузную подвижность. Однако вследствие большей массы они движутся существенно медленнее. Так, время корреляции вращения родопсина в фоторецепторных мембранах ~ 10-6 с.
Латеральная подвижность белков также существенно ниже, чем липидов. Коэффициенты латеральной диффузии белков в природных мембранах при комнатных температурах обычно находятся в пределах 10-10 -10-12 см2 /с.
Это свидетельствует, что при комнатной температуре мембраны проявляют свойства двумерной жидкости.
Вязкость: можно определить из уравнения Стокса – Эйнштейна, т е вязкость = константа Больцмана*Т/(6*пи*Д*r)
где r - радиус диффундирующей молекулы
Однако, поскольку мембраны неоднородны и асимметричны, скорость вращения или латеральной диффузии зондов в мембранах определяется микроструктурой их непосредственного окружения. Вследствие этого вязкость, рассматривают как «микровязкость». В зависимости от метода измерения подвижности, характера зонда и глубины его локализации в мембране значения микровязкости могут варьировать.
Вязкость углеводородной зоны мембран составляет, как правило, 1 - 2 пуаз, что говорит о жидкофазном состоянии мембраны, хотя это значение и превышает на два порядка вязкость воды.
При образовании поры (я не знаю, надо ли, физико-механические механизмы – это растяжимо):
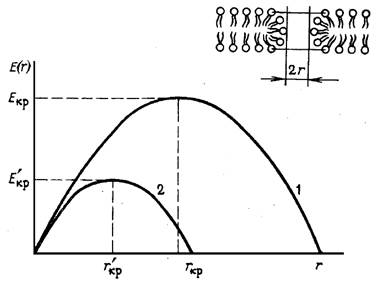
Прочность мембран зависит от химического состава, внешних условий и может нарушаться за счет локальных механических дефектов, возникающих при сжатии. Среднее время жизни БЛМ в электрическом поле падает при увеличении напряжения на мембране (электрический пробой мембраны). Энергия мембраны зависит от поверхностного натяжения, т. е. от работы, которую нужно затратить на образование 1 см поверхности липидного слоя. Если в мембране появляется дефект типа сквозной поры, то энергия мембраны будет зависеть от ее радиуса. Энергия уменьшится на величину, равную суммарному поверхностному натяжению на площади, занятой порой, а также за счет изменения электрической емкости мембраны при появлении в ней структурного дефекта. В результате оказывается, что зависимость энергии мембраны от радиуса дефекта имеет вид кривой с максимумом. Видно, что дефекты малого радиуса будут исчезать, однако дефекты с радиусом, большим критического (ф0), будут необратимо увеличиваться, приводя к разрыву мембраны. Величина критического радиуса уменьшается с ростом наложенной на мембрану разности потенциалов, чем и объясняется увеличение вероятности механического разрыва мембран в электрическом поле.
Зависимость энергии дефекта в мембране Е от его радиуса r отсутствии электрического поля и при наложении разности потенциалов ф,1 - при ф = 0 2 - при ф > 0; вверху справа -изображение поры в бислое:
Дата добавления: 2016-04-11; просмотров: 3506;
